MÉTODO PARA LA CONSERVACIÓN INDEFINIDA DE ESPERMA DE CEFALÓPODOS.
Método para la conservación indefinida de esperma de cefalópodos.
La presente invención reivindica un método de conservación a largo plazo del esperma de cefalópodos mediante la criopreservación de sus espermatóforos y espermatangios. La criopreservación se obtiene mediante el empleo de protocolos óptimos de incorporación y eliminación de crioprotectores permeables (alcoholes, sulfóxidos y formamidas en solución acuosa), y rampas de congelación y descongelación adecuadas. El método aquí descrito presenta una elevada utilidad en la cría en cautividad de especies de cefalópodos con interés comercial, en la conservación de especies en peligro de extinción y en investigaciones que desarrollan técnicas de fertilización in vitro en cefalópodos.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201130337.
Solicitante: UNIVERSIDAD DE LEON.
Nacionalidad solicitante: España.
Inventor/es: ROBLES RODRÍGUEZ,Vanesa, MARTÍNEZ PASTOR,Felipe, VILLANUEVA LÓPEZ,Roger.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01N1/02 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 1/00 Conservación de cuerpos humanos o animales, o partes de ellos. › Conservación de partes vivas.
- C12N5/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
- C12N5/07 C12N 5/00 […] › Células o tejidos animales.
PDF original: ES-2388086_A1.pdf
Fragmento de la descripción:
MÉTODO PARA LA CONSERVACIÓN INDEFINIDA DE ESPERMA DE CEFALÓPODOS
La presente invención se engloba en el sector técnico de la preservación de células vivas de invertebrados. También pertenece al sector de la preservación de partes vivas de animales. En cuanto a la aplicación de la invención, pertenece al sector de la cría de invertebrados.
ESTADO DE LA TÉCNICA ANTERIOR
La presente invención presenta un método para la conservación de espermatozoides de cefalópodo, en suspensión o mantenidos en el interior de espermatóforos y/o espermatangios, los cuales pueden conservarse enteros o seccionados en porciones.
Los cefalópodos constituyen un grupo de invertebrados marinos de gran interés para la industria alimentaria y así como con aplicaciones en industria farmacéutica y cosmética; e.g., patentes KR20080086751, KR1 00659040, US2005129739) , o para investigación en biomedicina (Lee et al. 1994) . Los cefalópodos se obtienen principalmente mediante actividades pesqueras, capturándose 4.313.51 O toneladas en el año 2007, con un valor de 7.351 millones de US$ (FAO 2009) , principalmente calamares de los géneros Dosidicus, l//ex y Todadores. No obstante, al contrario que otras especies acuáticas, la producción mediante acuicultura es aún muy reducida, produciéndose sólo 30 toneladas. Aún así informes de expertos indican que los esfuerzos para establecer cultivos intensivos y semi-intensivos de estos animales deberían intensificarse, debido a las características propias de este grupo de rápido crecimiento y riqueza en proteína, su importancia económica actual, el estado de las pesquerías y la proyección futura de su creciente consumo (Sykes et al., 2006; Pierce et al. 201 0) .
La incipiente acuicultura de cefalópodos se ha desarrollado principalmente con los géneros Sepia y Octopus (Vaz-Pires et al. 2004; Sykes et al., 2006) . En la última década se han realizado engordes de ejemplares subadultos de pulpo (Octopus vulgaris) con fines comerciales en el noroeste de la Península Ibérica (Chapela et al. 2006; Rodríguez et al., 2006) . Existen varias patentes orientadas a la cría de cefalópodos, especialmente relacionadas con estructuras y métodos para el mantenimiento y engorde de individuos subadultos y adultos (e.g., CN201163931, ES2121700, JP2002360105, CN201160421, JP9023782, CN201204867, CN101268767, CN101491226, CN101637141) . El principal problema actualmente consiste en la cría de paralarvas y juveniles, habiéndose realizado progresos significativos en los últimos años (Iglesias et al., 2007; Villanueva & Norman 2008; Jones et al., 201 O; Uriarte et al., 201 0) , reflejados en algunas patentes para la cría de paralarvas (CN101317551, CN101455188) y fertilización in vitro en cefalópodos (CN101703013, CN101427658) . La patente CN101703034 propone un sistema para la cría de pulpo que incluye entornos para el apareamiento de los adultos, la puesta de huevos y la separación y cría de las paralarvas.
El esfuerzo realizado en investigación y su transferencia en tecnología permite augurar un rápido crecimiento de la acuicultura de cefalópodos, y un incremento de su importancia relativa en la producción destinada a su consumo o utilización industrial. Al mismo tiempo que se mejoran las técnicas de cultivo de cefalópodos y se incrementa el rendimiento de las instalaciones, se pretende mantener el ciclo vital completo de las especies en cautividad. La presente invención se encuadra en este contexto. La aplicación de tecnologías reproductivas ha permitido mejorar la gestión, reducir costes y facilitar programas de selección genética en otras especies (Gosden et al., 2002) . Dentro de estas tecnologías, la congelación de esperma, extendiendo su vida útil indefinidamente, tiene una importancia crucial, ya que ha permitido la extensión de programas de inseminación artificial, e incluso el comercio de dosis seminales. La aplicación de esta tecnología en cefalópodos sería muy beneficiosa para mejorar el rendimiento de cultivos de especies oceánicas mediante fertilización in vitro (Sakurai et al. 1995) , para la selección de stocks de progenitores (Iglesias et al. 2007) , así como para la conservación de especies en peligro de extinción (Freeman et al., 201 0) .
En la actualidad no existe publicado ningún estudio científico ni ninguna patente en relación con la congelación de espermatozoides ni espermatóforos o espermatangios en cefalópodos. Existen varios estudios relacionados con la estructura y características morfológicas de los espermatozoides de varias especies (Diaspro et al., 1997; Giménez-Bonafé et al., 2002; Giménez-Bonafé et al., 2004; Cuccu et al., 2007; Li et al., 2010) , así como con la fisiología de los espermatóforos de cefalópodos (Austin et al., 1964; Mann et al., 1981; Naud et al., 2006; Wada et al., 201 O) .
Los espermatóforos constituyen estructuras características de cada especie y por ello tienen importancia taxonómica. Todas las especies de cefalópodos presentan estas estructuras, variando entre ellos el tamaño y la forma de los mismos. Generalmente son de forma tubular y encapsulan en su interior una masa espermática (Austin et al., 1964) . Los espermatóforos de los cefalópodos son más elaborados que los de otros moluscos, y poseen la peculiaridad de poseer un mecanismo que, bajo ciertos estímulos mecánicos y durante la cópula, ejecuta la llamada reacción espermatofórica, durante la cual, el espermatóforo se evierte y forma un espermatangio que permanecerá anclado en diferentes superficies del cuerpo de la hembra. Los espermatozoides se forman en el testículo, vasos deferentes y espermiducto. Los espermatóforos, ya con esperma en su interior se almacenan finalmente en la bolsa de Needham del macho. Son transferidos a la hembra durante la cópula, generalmente mediante un brazo modificado denominado hectocótilo y/o un órgano similar a un pene denominado órgano terminal. Dependiendo de las especies los espermatangios pueden ser almacenados en receptáculos seminales de la hembra situados alrededor de la membrana bucal, o implantados directamente en el interior o exterior de la superficie del manto, cartílago nucal, la superficie de brazos y cabeza, o incluidos directamente en los oviductos distales e incluso llegar hasta el ovario. Días, semanas o meses después de la cópula, las hembras fertilizan sus oocitos utilizando los espermatozoides provenientes de estos espermatangios.
La movilidad espermática se inicia por contacto con el agua de mar, pero dentro de los espermatóforos o de los espermatangios unidos a la hembra, los espermatozoides son quiescentes. Esto permite que los espermatozoides permanezcan viables durante largos periodos dentro de estas estructuras. Por lo tanto, los espermatóforos y espermatangios serían las estructuras adecuadas por sí mismas para criopreservar los espermatozoides de este grupo de moluscos, no siendo necesario congelar la masa espermática por sí sola. Una vez
descongelados, la masa espermática sería extraída de estas estructuras y utilizada para fertilizar los oocitos (por ejemplo, utilizando métodos como los descritos en CN1 01703013 o CN1 01427658) .
La criopreservación seminal es una técnica de gran utilidad para la conservación indefinida de material biológico. Las principales ventajas de la criopreservación se resumen a continuación: -posibilidad de preservar o conservar el material genético; -posibilidad de analizar y comparar el material genético, entre varios individuos de una misma especie; -ayuda o facilitación de cruces, comparado con el cruce de animales formados; -posibilidad de seleccionar el entrecruzamiento más óptimo en función de por ejemplo las condiciones ambientales; -posibilidad de comprobar la ausencia de contaminación por agentes infecciosos; -beneficio de preservar volúmenes reducidos de líquido, comparado con el mantenimiento de animales ya formados.
La técnica de criopreservación de espermatozoides se inició a mediados del siglo XX, y ha sido utilizada exitosamente en numerosas especies de mamíferos y, progresivamente, en otros órdenes de vertebrados. En invertebrados acuáticos, los estudios se han ido incrementando, pero están aún limitados a unas pocas especies de equinodermos (erizos de mar y estrellas de mar) , moluscos (ostras, oreja de mar y algunas almejas) , poliquetos y crustáceos decápodos de interés comercial. La creación de bancos de esperma en estas especies tiene un enorme potencial para los programas de hibridización, selección de razas o líneas... [Seguir leyendo]
Reivindicaciones:
1. Método para la criopreservación del esperma de cefalópodos que
comprende los siguientes pasos: a) obtención del esperma de los individuos seleccionados, b) preparación de la solución crioprotectora en una solución base a una concentración final entre 5% y 50%, e) exposición del esperma a un volumen de solución crioprotectora entre O, 1 ml y 1 O ml, a una temperatura entre O oc a 25 oc, de O a 2 h en un criovial, d) enfriamiento por rampa de congelación del criovial a una velocidad entre -1 oc/min y -100 oc/m in, desde una temperatura de +25 oc a por lo menos -20 °C.
2. Método para la criopreservación de esperma de cefalópodos según la reivindicación 1, caracterizado porque el esperma de cefalópodo está contenido dentro de espermatóforos o espermatangios.
3. Método para la criopreservación de esperma de cefalópodos según la reivindicación 2, caracterizado porque los espermatóforos o espermatangios se encuentran enteros o en secciones de entre 1 cm y 4 cm.
4. Método para la criopreservación de esperma de cefalópodos según una de las reivindicaciones 1 a 3, caracterizado porque dicha especie de cefalópodos pertenece a los Ordenes: Nautilida, Spirulida, Sepiida, Sepiolida, Teuthida, Octopodida y Vampyromorphida ..
5. Método para la criopreservación de esperma de cefalópodos según la reivindicación 4, caracterizado porque la especie de cefalópodo es l//ex coindetii Volador.
6. Método para la criopreservación de esperma de cefalópodos según una de las reivindicaciones 1 a 3, caracterizado porque en el paso a) se conserva el
esperma a una temperatura entre 4 oc y 1 O oc en una solución base que es agua de mar filtrada o agua de mar artificial.
7. Método para la criopreservación de esperma de cefalópodos según una de las reivindicaciones 1 a 3, caracterizado porque la solución crioprotectora del paso b) se selecciona entre: dimetilsulfóxido, compuestos del grupo de las amidas y alcoholes.
8. Método para la criopreservación de esperma de cefalópodos según la reivindicación 7, caracterizado porque la solución crioprotectora del paso b) se selecciona entre: DMSO, metanol, glicerol, propanodiol y etilenglicol.
9. Método para la criopreservación de esperma de cefalópodos según una de las reivindicaciones 1 a 3, caracterizado porque los pasos b) y e) se repiten con concentraciones finales crecientes a intervalos de 1 a 25% del diluyente y tiempos de equilibrado entre 1 min y 120 min del esperma diluido.
9. Método para la criopreservación de esperma de cefalópodos según una de las reivindicaciones 1 a 3, caracterizado porque el paso d) de enfriamiento por rampa de congelación está seleccionado del grupo que comprende: por exposición a vapores de nitrógeno líquido, en un congelador de -20 oc a -130 oc y en un dispositivo biocongelador.
1O. Método para la criopreservación de esperma de cefalópodos según la reivindicación 9, caracterizado porque la exposición a vapores de nitrógeno líquido se realiza situando un soporte flotante a una altura entre 0, 5 cm y 1 O cm de la superficie de nitrógeno líquido, por un periodo de tiempo entre 2 min y 120 m in.
11. Método para la criopreservación de esperma de cefalópodos según las reivindicaciones anteriores, caracterizado porque comprende los siguientes pasos adicionales:
e) descongelación del esperma criopreservado, a una temperatura entre 4 oc-80 oc, por un periodo de tiempo entre 2 s y 60 min, y
f) lavado del esperma descongelado con un volumen entre 0, 5 ml y 1 O ml
de una solución de lavado, por un periodo de tiempo de hasta 60 min y a
una temperatura de 4 oc a 25 oc.
12. Método para la criopreservación de esperma de cefalópodos según la reivindicación 11, caracterizado porque el paso f) se realiza al menos 1 vez.
13. Método para la criopreservación de esperma de cefalópodos según la
reivindicación 11 o 12, caracterizado porque la solución de lavado del paso f) es 10 agua de mar filtrada o agua de mar artificial.
14. Método para la criopreservación de esperma de cefalópodos según la reivindicación 11 o 12, caracterizado porque la solución de lavado del paso f) es solución crioprotectora diluida en solución base a una concentración menor que la
15 empleada en el paso b) .
Patentes similares o relacionadas:
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Estimulación de la vía wnt en la reprogramación de células somáticas, del 20 de Mayo de 2020, de WHITEHEAD INSTITUTE FOR BIOMEDICAL RESEARCH: Un método de reprogramación de una célula somática de mamífero, que comprende: (a) poner en contacto la célula somática de mamífero con un activador de la vía Wnt seleccionado […]
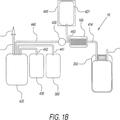 Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Ceramidasa y diferenciación celular, del 22 de Abril de 2020, de MOUNT SINAI SCHOOL OF MEDICINE: Un método in vitro para mejorar el fenotipo de una población de condrocitos, dicho método comprende: seleccionar una población de condrocitos de mamífero que […]
Medios de perfusión, del 1 de Abril de 2020, de Coherus Biosciences, Inc: Un método para la fabricación de una proteína que comprende la etapa de producir la proteína mediante el cultivo celular por perfusión de células […]
Andamios de biomatriz para la dispersión a escala industrial, del 11 de Marzo de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un metodo para producir un andamio de biomatriz a partir de tejido biologico seleccionado del grupo que comprende: pancreas, arbol biliar y duodeno para la […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en hepatocitos, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en hepatocitos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un medio […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en neuronas, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en neuronas, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un […]