VACUNA CONTRA TUMORES QUE COMPRENDE CÉLULAS TUMORALES ALOGÉNICAS O XENOGÉNICAS.
Una composición para el tratamiento o prevención de un tumor en un paciente,
que comprende (i) células tumorales alogénicas o xenogénicas; (ii) un lisado de células tumorales singénicas; y (iii) un excipiente farmacéuticamente aceptable, donde las células de (i) y (ii) se definen con referencia a las células del tumor del paciente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/050807.
Solicitante: STATHOPOULOS, APOSTOLOS.
Nacionalidad solicitante: Luxemburgo.
Dirección: 17, RUE BELLE-VUE 4974 DIPPACH LUXEMBURGO.
Inventor/es: Stathopoulos,Apostolos.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Enero de 2007.
Clasificación Internacional de Patentes:
- A61K35/30 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Nervios; Cerebro; Células de la córnea; Fluido Cerebroespinal; Células madre neuronales; Células precursoras neuronales; Células de la glia; Oligodentrocitos; Células de Schwann; Células de Schwann; Astroglia; Astrocitos; Plexo coroideo; Tejido de la médula espinal.
- A61K39/00D6
Clasificación PCT:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2358223_T3.pdf




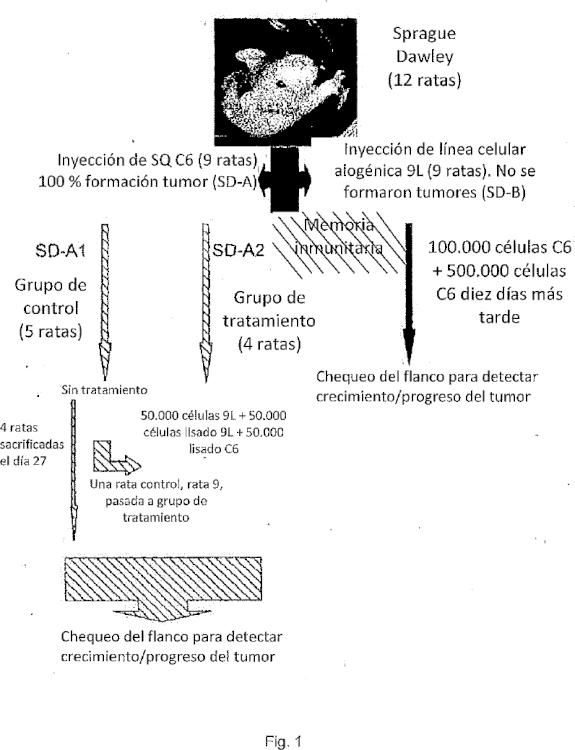
Fragmento de la descripción:
Campo de la invención
Esta invención se refiere al tratamiento de tumores. En particular, esta invención se refiere al tratamiento de los tumores mediado inmunológicamente.
Antecedentes de la invención 5
El sistema inmunitario consiste en dos ramas, que aunque separadas por velocidad y especificidad, están intrínsecamente ligadas, creando una respuesta rápida y directa frente a las agresiones tanto endógenas como exógenas16,21. El sistema inmunitario innato proporciona una defensa inmediata del hospedante frente a las agresiones físicas, químicas y microbiológicas16,21. Dicho sistema involucra a los neutrófilos, monocitos, macrófagos, complemento, citocinas y proteínas en fase aguda16,21. A pesar de la falta de especificidad de antígeno, el sistema inmunitario innato es 10 capaz de reconocer los péptidos propios de los péptidos no propios, extraños16,21. La inmunidad adaptativa, sin embargo, implica a los linfocitos B y T en una respuesta altamente específica dirigida al antígeno16,21. Una ventaja de la inmunidad adaptativa es la memoria inmunitaria potencial, que lleva a una respuesta más fuerte y más rápida en posteriores estimulaciones8,9.
La característica que define a la inmunidad adaptativa (inmunidad específica) es el uso de los linfocitos B y T 15 que llevan receptores específicos del antígeno, en una respuesta inmunitaria dirigida,21. Los principales efectores de células T son las células ayudadoras T que llevan receptores CD4, y las células citotóxicas T que llevan receptores CD816,21. Las células ayudadoras T interactúan con el MHC II, y son responsables de coordinar la respuesta inmunitaria, reconocer antígenos extraños, activar diferentes partes del sistema inmunitario y activar las células B. Las células citotóxicas T interactúan con los receptores MHC I y desempeñan un papel en la organización de una respuesta inmunitaria frente a patógenos exógenos16,21.
El complejo principal de histocompatibilidad (MHC) es una región genética que codifica proteínas que desempeñan un papel esencial en la regulación y modulación de la respuesta inmunitaria10,18. Los productos génicos del MHC se dividen en dos grupos separados, basados en la estructura y en las propiedades biológicas: MHC I y MHC II10,16. Los receptores MHC clase I, están presentes en todas las células nucleadas10,16. Estos receptores presentan péptidos sintetizados endógenamente y están íntimamente implicados en su autoidentificación. Los receptores MHC clase II, se encuentran solamente en las células implicadas en las respuestas inmunitarias y presentan proteínas derivadas exógenamente tales como las de producción bacteriana10,16. Clásicamente, se había creído que el MHC I estaba implicado en el rechazo de los tumores, pero más recientemente se ha encontrado que el MHC II desempeña un papel.
La diversidad de la unión al antígeno mediante las moléculas de MHC clase I se basa en tres principios básicos 30 e interrelacionados. En primer lugar, las moléculas de clase I tienen la habilidad de unirse a péptidos con muchas secuencias diferentes2,16. Estos complejos de MHC clase I:antígeno pueden ser reconocidos por los linfocitos T citotóxicos (CDS), llevando eventualmente a la destrucción de cualquier célula portadora de una proteína extraña similar2,16. En segundo lugar, cada organismo expresa muchos genes diferentes de clase I2,16. Finalmente, el MHC presenta polimorfismos con un número de alelos en cada locus2,16.23. En los seres humanos, el MHC I está representado en más de un 35 locus denominado el antígeno leucocitario humano (HLA), siendo los locus HLA-A, HLA-B y HLA-C, el más polimórfico de los cuales es HLA-B16,23. Estos factores implican un alto grado de especificidad individual y la necesidad de un regulador que ejerza una presión selectiva: el sistema celular inmunitario.
Es este alto grado de especificidad y de anulación de la presión selectiva lo que se explota en el trasplante de órganos y tejidos entre individuos23. Los gemelos idénticos y los miembros de una familia genéticamente cercanos son 40 menos propensos a rechazar el tejido trasplantado porque tienen locus HLA similares16. Esto se basa en el hecho de que los MHC I están expresados co-dominantemente y en la mayor parte de los casos se heredan intactos sin recombinación16,23. Por lo tanto, los individuos homocigóticos tales como los gemelos idénticos y las ratas singénicas podrían aceptar teóricamente un tumor cerebral procedente de su donante homocigótico. Aún más críticamente, ellos deberían rechazar un tumor cerebral procedente de un donante heterocigótico basándose en una respuesta inmunitaria específica y dirigida.
Como se indicó al principio, los receptores MHC clase I son glucoproteínas de superficie localizadas en la mayoría de las células que desempeñan un papel crucial en la respuesta inmunitaria. Estos MHC clase I se unen a los péptidos antigénicos e interactúan con las células NK y CD85,16.25. Estos péptidos se derivan de proteínas endógenas degradadas procedentes de células infectadas por virus y tumores5,16.25. La formación del antígeno es un mecanismo 50 complejo que incluye numerosas etapas. Un defecto en cualquiera de estas etapas puede llevar a la no expresión del complejo de MHC clase I::antígeno, y a librarse del reconocimiento y destrucción de las células T12. La pérdida o desregulación de los complejos MHC I es un mecanismo frecuente para evitar la destrucción procedente de CD812. Intuitivamente, se puede asumir que este marcador de “pérdida de lo propio” (“missing self”)17 podría llevar a un aumento del reconocimiento por las células NK, que son inhibidas por interactuar con el complejo MHCI I, y que son estimuladas por 55 las células con expresión de HLA-2/HA regulada por disminución18. Incluso con un sistema inmunitario que funcione completamente, es posible que los tumores eludan el reconocimiento mediante el uso de una estrategia de escape elusiva12. Aunque el mecanismo de escape se entiende difícilmente, algunos experimentos han descrito varios mecanismos que permiten que los tumores escapen del reconocimiento por el sistema inmunitario. Estos mecanismos varían desde la pérdida o mutación de los halotipos HLA hasta la falta de receptividad para los interferones12. Así mientras un cambio o pérdida de los receptores MHC clase I se asocia con la génesis de diferentes tumores, se ha demostrado que la presencia de moléculas de MHC clase I participa en la resistencia al cáncer.
Un ejemplo de los efectos anti-tumorígenos de una molécula de MHC clase I está en la vigilancia inmunitaria de 5 la integridad del ADN mitocondrial. En un estudio, uno de los papeles de las moléculas de MHC I fue eliminar las células que llevan una mutación mitocondrial13. Las células del glioma humano llevan múltiples mutaciones tanto del ADN mitocondrial como del complejo mitocondrial7. A partir de estos datos, es posible asumir que los gliomas del mismo tipo/grado histológico llevarán mutaciones similares en sus ADN y tendrán proteínas de superficie anormales similares asociadas tanto con las moléculas de MHC clase I como con la membrana celular. A la inversa, un sistema inmunitario 10 intacto puede permitir también el desarrollo y progreso de los tumores.
Se ha demostrado que el progreso de ciertos cánceres está asociado con la expresión de antígenos específicos del tumor y con una respuesta inmunitaria asociada15. Por lo tanto, no se puede alcanzar el rechazo eficaz del tumor ni la inmunidad únicamente por la autovacunación. A pesar de estas barreras, hay indicios crecientes de que el sistema inmunitario se puede utilizar para combatir el cáncer. Aunque tanto un sistema inmunitario no regulado como un sistema 15 inmunitario que funcione normalmente luchan contra el rechazo inmunitario del cáncer, se han publicado resultados del rechazo espontáneo de tumores malignos19,26. Curiosamente, se ha sugerido también que las enfermedades autoinmunes pueden contribuir a un mejor pronóstico en pacientes con tumores malignos6,19. En estos pacientes, la mayoría de las especificidades IgG identificadas comparten considerable homología con péptidos tanto humanos como microbianos14. Esto ha llevado a la hipótesis de que el mimetismo molecular puede iniciar la autoinmunidad tumoral observada. 20 Estudios relacionados con esto han demostrado la remisión a largo plazo de tumores malignos de cerebro después de infección intracraneana en cuatro pacientes4, y una mejor supervivencia de los pacientes de cáncer con infección microbiana20,22. Esto plantea la cuestión de si se puede usar para tratar tumores... [Seguir leyendo]
Reivindicaciones:
1. Una composición para el tratamiento o prevención de un tumor en un paciente, que comprende
(i) células tumorales alogénicas o xenogénicas;
(ii) un lisado de células tumorales singénicas; y
(iii) un excipiente farmacéuticamente aceptable,
donde las células de (i) y (ii) se definen con referencia a las células del tumor del paciente. 5
2. Una composición según la reivindicación 1, que comprende además un lisado de células alogénicas o xenogénicas.
3. Una composición según la reivindicación 1 o la reivindicación 2, en la que las células de (i) son células derivadas del cerebro.
4. Una composición según la reivindicación 3, en la que las células singénicas son células derivadas del cerebro.
5. Una composición según cualquiera de las reivindicaciones precedentes, en la que las células alogénicas o xenogénicas se derivan de los tumores de dos o más individuos heterocigóticos.
6. El uso de (i) células tumorales alogénicas o xenogénicas y (ii) un lisado de células singénicas, en la fabricación de un medicamento para el tratamiento de un tumor en un paciente. 15
7. El uso según la reivindicación 6, en el que el tumor del paciente es del mismo grado histológico que el tumor de las células alogénicas o xenogénicas.
8. El uso según la reivindicación 6 o la reivindicación 7, en el que las células alogénicas o xenogénicas se derivan de los tumores de dos o más individuos heterocigóticos.
Patentes similares o relacionadas:
Composición para el tratamiento de enfermedades isquémicas o trastornos inflamatorios neurogénicos, que contienen el secretoma de células progenitoras neurales como ingrediente activo, del 22 de Julio de 2020, de S-BIOMEDICS: Una composición para uso en el tratamiento de enfermedad cerebrovascular isquémica, cardiopatía isquémica, infarto de miocardio, enfermedad de Alzheimer, enfermedad […]
Diferenciación dirigida de astrocitos a partir de células madre pluripotentes humanas para uso en el cribado de medicamentos y el tratamiento de la esclerosis lateral amiotrófica (ELA), del 18 de Marzo de 2020, de Kadimastem Ltd: Un método de detección de un agente para prevenir o tratar la esclerosis lateral amiotrófica (ELA), el método comprende: (a) contactar a una […]
Métodos para inducir apoptosis parcial utilizando polipéptidos de caspasa, del 4 de Marzo de 2020, de Bellicum Pharmaceuticals, Inc: Un ligando multimérico para usar en un método para el tratamiento del cáncer; comprendiendo dicho método controlar la supervivencia de las células terapéuticas en un […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en neuronas, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en neuronas, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un […]
Composiciones y herramientas para tratar el glaucoma, del 12 de Febrero de 2020, de P&X Medical NV: Composición que comprende líquido cefalorraquídeo (LCR) o una composición similar al LCR para su uso en la prevención y/o el tratamiento del glaucoma, en donde la composición […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en osteoblastos, del 22 de Enero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en osteoblastos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava […]
Trasplante de células neurales humanas para el tratamiento de afecciones neurodegenerativas, del 8 de Enero de 2020, de Seneca Biopharma, Inc: Población de células madre neurales expandidas concentradas para utilizar en un procedimiento de tratamiento de una afección de espasticidad, rigidez o hiperactividad […]
Neuronas de dopamina (DA) del mesencéfalo para injerto, del 25 de Diciembre de 2019, de Memorial Sloan Kettering Cancer Center: Un método in vitro para diferenciar células pluripotentes en precursores de la placa del suelo del mesencéfalo, comprendiendo el método: exponer una pluralidad […]