SISTEMA DE SUMINISTRO GÉNICO SISTÉMICO VIRAL/LIGANDO Y TERAPIA GÉNICA.
Complejo virus-ligando que se dirige a una célula para el suministro de un virus a una célula diana en el interior de un animal huésped,
en el que dicho complejo virus-ligando está constituido por un ligando y un virus, y en el que el ligando está unido de manera no covalente al virus, y es la transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/027365.
Solicitante: GEORGETOWN UNIVERSITY
SYNERGENE THERAPEUTICS INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 37TH AND "O" STREETS, N.W. WASHINGTON, D.C. 20057 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ALEXANDER, WILLIAM, XU,LIANG, CHANG,ESTHER,H, PIROLLO,KATHLEEN.
Fecha de Publicación: .
Fecha Solicitud PCT: 19 de Noviembre de 1999.
Fecha Concesión Europea: 6 de Octubre de 2010.
Clasificación PCT:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K47/48
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/86 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores virales.
- C12N15/87 C12N 15/00 […] › Introducción de material genético extraño utilizando procedimientos no previstos en otro lugar, p. ej. cotransformación.
Clasificación antigua:
- A61K38/17 A61K 38/00 […] › que provienen de animales; que provienen de humanos.
- A61K47/48
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12N15/87 C12N 15/00 […] › Introducción de material genético extraño utilizando procedimientos no previstos en otro lugar, p. ej. cotransformación.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
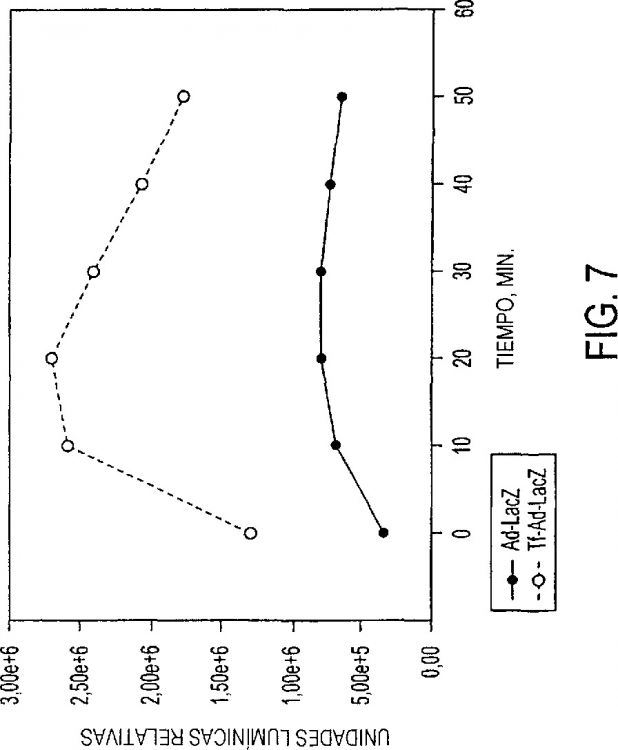
Fragmento de la descripción:
Sistema de suministro génico sistémico viral/ligando y terapia génica.
Antecedentes de la invención
La presente invención se refiere a mejoras en la transferencia génica y en la tecnología de la terapia génica. Más específicamente, la invención proporciona composiciones y procedimientos para el suministro vírico in vivo e in vitro de ácidos nucleicos en el hombre y en otros animales a un órgano, tejido, o tumor específicos. La utilización de esta invención para suministrar un gen terapéutico, por ejemplo, wtp53, puede conducir a un aumento de la sensibilidad a la radiación y a la quimioterapia convencionales.
El documento WO98/40508 describe vectores adenovíricos con tropismo modificado.
Miller y Vile (1998) dan a conocer vectores dirigidos para la terapia génica.
Snitkovsky y Young dan a conocer vectores víricos célulo-específicos mediados por una proteína retrovírica soluble (de fusión) receptor-ligando.
El suministro génico y la terapia génica utilizando vectores víricos han constituido el objeto de considerable investigación. Un objetivo duradero en la terapia génica para el cáncer es un sistema de suministro sistémico que se dirija selectivamente a las células tumorales, incluyendo las metástasis. Los ácidos nucleicos pueden introducirse en las células mediante vectores víricos para producir un efecto terapéutico deseado sobre estas células. Por ejemplo, un gen puede introducirse para reemplazar un gen defectuoso que interfiera en la función celular, por ejemplo, p53. Los ácidos nucleicos pueden también introducirse en las células para producir un efecto terapéutico deseado en el animal huésped, por ejemplo, para vacunación, inmunoterapia, o expresión antisentido.
Los vectores víricos se han desarrollado para aprovecharse de los mecanismos de entrada celular que utilizan los virus para transferir su ácidos nucleicos a las células huéspedes. Se han construido vectores retrovíricos y adenovíricos recombinantes utilizando esta estrategia, para obtener la transferencia in vitro e in vivo. Aproximadamente, el 80% de los protocolos de terapia génica que se han aprobado para ensayos clínicos utilizan vectores víricos (Wivel y Wilson, 1998). Los vectores adenovíricos ofrecen ventajas para algunas formas de terapia génica, porque pueden penetrar en las células que no se dividen y llevar a cabo una carga de pago relativamente voluminosa (>8 kb) de ADN extraño (Berkner, 1988). Además, las partículas adenovíricas pueden purificarse y producirse en títulos superiores a 1011 PFU/ml (Wivel y Wilson, 1998). Una desventaja de estos sistemas, sin embargo, es el limitado tropismo celular de los virus y el problema significativo que consiste en dirigir las partículas víricas, (que) tiene todavía que resolverse para alguno de los virus terapéuticos que se utilizan habitualmente en los ensayos clínicos para el cáncer. De acuerdo con esto, se han desarrollado procedimientos para alterar el tropismo celular y continúan investigándose.
Se ha descrito (Roux et al., 1989), un sistema que cambia el tropismo de los retrovirus mediante un conjugado bifuncional. El conjugado bifuncional contiene un anticuerpo dirigido contra la envuelta vírica y, por otra parte, un anticuerpo dirigido a un marcador específico de membrana celular para la célula diana.
Goud et al. (1988) describieron los conjugados bifuncionales que consisten en dos anticuerpos monoclonales (MAbs). Los MAbs se dirigieron contra la proteína gp70 de la envuelta del retrovirus Moloney y del receptor de la transferrina humana. Estos conjugados permitieron al retrovirus penetrar en las células diana de otro modo no tolerantes.
El documento WO 92/06180 (Wu et al., 1992), describe un procedimiento para cambiar el tropismo de un virus, proporcionando a la superficie de éste una molécula que se una a un receptor superficial de la célula diana, lo que da lugar a un virus con especificidad para células (que posean) el receptor superficial celular. En la exposición un retrovirus o un virus de la hepatitis B se modifica químicamente con moléculas de hidrato de carbono que se unen al receptor asialoglicoproteico. Wu et al. dan a conocer sólo procedimientos in vitro para la introducción de genes extraños en las células.
Los vectores adenovíricos ofrecen ventajas para algunas formas de terapia génica, porque pueden penetrar en las células que no se dividen y pueden transportar una secuencia de ADN extraño de aproximadamente 8 kb. Las partículas adenovíricas pueden purificarse y producir titulaciones superiores a 1011PFU/ml.
Un impedimento para la utilización de los adenovirus recombinantes es su limitada capacidad para impactar en tipos celulares específicos. Diversos estudios han informado de transferencia génica utilizando adenovirus no recombinantes con complejos de ADN, mediante endocitosis mediadas por receptores, proporcionando el adenovirus la capacidad para liberar el contenido de los endosomas (Cotten et al., 1992; Wagner et al., 1992). Estos procedimientos utilizan complejos transferrina-polilisina/ADN para internalizar los adenovirus unidos o no. Wagner et al. (1992) modificó un vector adenovírico mediante conjugación a la polilisina y haciendo que ésta formara complejos con conjugados de transferrina-polilisina/ADN, lo que llevó a la producción de complejos ternarios transferrina-polilisina/adenovirus-polilisina/ADN. Un enfoque parecido para hacer diana en las células es la unión de transferrina (Tf) a partículas adenovíricas, con el fin de aprovechar el hecho de que el receptor transferrínico (TfR) está elevado en muchos tipos tumorales (Miyamoto et al., 1994; Baselga y Mendelsohn, 1994). Schwarzenberger et al. (1997) describe vectores de conjugación molecular (MCV). MCV se construyen condensando con polilisina (PL) un plásmido que contiene el gen de interés, y uniendo esta PL a un adenovirus que no es competente para la replicación (agente endosomolítico), y uniendo PL a la estreptoavidina para impactar en ligandos biotinilados. Sin embargo, se ha informado (Cotten et al., 1992; Wagner et al., 1992; Schwarzenberger et al., 1997) que los procedimientos habituales de enlace covalente de Tf al adenovirus, o la generación de conjugados Tf-polilisina-adenovirus, dan lugar a menudo a un descenso en la infectividad, debido posiblemente a las severas condiciones que se requieren para producir los virus Tf modificados.
Otro enfoque vincula el entrecruzamiento del fragmento Fab de un anticuerpo neutralizante antifibroso o de un anticuerpo monoclonal anti"joroba" a un ligando, tal como folato o FGF2 (Rogers et al., 1997; Douglas et al,. 1996). Los vectores adenovíricos que forman complejo con el ligando-Fab quimérico se han mostrado algo prometedores en la localización tumoral y muestran una reducida toxicidad hepática in vivo, comparada con los adenovirus originales.
Curiel et al., (patentes US nº 5.521.291 y nº 5.547.932) dan a conocer múltiples conjugados adenovírico-policatiónicos para internalizar ácidos nucleicos en las células eucarióticas. Alguno de estos conjugados utiliza la transferrina que se une a una substancia que posee una afinidad para el ácido nucleico como factor internalizante.
Cotten et al. (patente US nº 5.693.509) da a conocer adenovirus con la capacidad (de la que ya se ha informado) de penetrar eficientemente en las células en las que no pueden normalmente hacerlo, mientras conservan su capacidad para la expresión génica y/o sus propiedades endosomolíticas. La transferrina está covalentemente unida a partículas adenovíricas, de forma que éstas pueden experimentar endocitosis mediadas por los receptores. El procedimiento oxida la transferrina a una forma que contiene grupos aldehídos en la parte de hidratos de carbono y une la transferrina oxidada al adenovirus, bajo condiciones de reducción. Asimismo, se da a conocer que no puede predecirse si la infectividad se mantiene después de la modificación.
Low et al. (Patentes US nº 5.108.921; nº 5.416.016; y nº 5.635.382) dan a conocer procedimientos para potenciar el transporte a través de las membranas de moléculas exógenas, utilizando ligandos tales como folato, biotina, tiamina, y sus análogos. Los procedimientos...
Reivindicaciones:
1. Complejo virus-ligando que se dirige a una célula para el suministro de un virus a una célula diana en el interior de un animal huésped, en el que dicho complejo virus-ligando está constituido por un ligando y un virus, y en el que el ligando está unido de manera no covalente al virus, y es la transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF.
2. Complejo virus-ligando que se dirige a una célula según la reivindicación 1, en el que dicho virus y dicho ligando no están asociados entre sí de manera natural.
3. Complejo virus-ligando que se dirige a una célula según la reivindicación 1 ó 2, en el que dicho virus comprende un ácido nucleico terapéutico.
4. Complejo virus-ligando que se dirige a una célula según la reivindicación 3 ó 2, en el que dicho ácido nucleico terapéutico codifica un péptido o una proteína terapéuticos.
5. Complejo virus-ligando que se dirige a una célula según la reivindicación 4 en el que dicho ácido nucleico terapéutico codifica el p53 de tipo salvaje.
6. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones anteriores, en el que dicho virus es un retrovirus o un adenovirus.
7. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones 1 a 5, en el que dicho virus se selecciona de entre el grupo constituido por virus adeno-asociado, virus del herpes simplex, citomegalovirus, virus de la vacuna, virus de la viruela aviar, virus de la viruela de los canarios, y virus Sindbis.
8. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones anteriores, en el que dicho virus es un virus quimérico, un virus híbrido, o un virus recombinante.
9. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones anteriores, en el que dicho ligando que se dirige a una célula es una proteína original o una proteína recombinante.
10. Complejo virus-ligando que se dirige a una célula, según cualquiera de las reivindicaciones anteriores, en el que dicho ligando que se dirige a una célula y dicho virus, están presentes en una proporción comprendida en el intervalo de 100 a 1.000.000 de moléculas de ligando por virión.
11. Complejo virus-ligando que se dirige a una célula según la reivindicación 10, en el que dicho ligando que se dirige a una célula y dicho virus están presentes en una proporción comprendida en el intervalo de 6.700 a 400.000 moléculas de ligando por virión.
12. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones anteriores, en el que dicho ligando que se dirige a una célula y dicho virus, están presentes en una proporción comprendida en el intervalo de 1 μg a 10 mg de dicho ligando por 1010 viriones.
13. Complejo virus-ligando que se dirige a una célula según la reivindicación 12, en el que dicho ligando que se dirige a la célula y dicho virus están presentes en una proporción comprendida en el intervalo de 10 μg a 600 μg de dicho ligando por 1010 viriones.
14. Vector para el suministro sistémico de un virus a una célula diana, comprendiendo dicho vector un ligando que se dirige a una célula unido de manera no covalente a dicho virus, en el que dicho vector puede prepararse mezclando una composición constituida por un ligando que se dirige a una célula con un virus en un medio acuoso y en el que dicho ligando está constituida por transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF.
15. Vector según la reivindicación 14, en el que dicho virus y dicho ligando no están asociados naturalmente entre sí.
16. Vector según la reivindicación 14 ó 15, en el que dicho virus comprende un ácido nucleico terapéutico.
17. Vector según la reivindicación 16, en el que dicho ácido nucleico terapéutico codifica un péptido o una proteína terapéuticos.
18. Vector según la reivindicación 17, en el que dicho ácido nucleico terapéutico codifica el p53 de tipo salvaje.
19. Vector según cualquiera de las reivindicaciones 14 a 18, en el que dicho virus es un retrovirus o un adenovirus.
20. Vector según cualquiera de las reivindicaciones 14 a 18, en el que dicho virus se selecciona de entre el grupo constituido por virus adeno-asociado, virus del herpes simplex, citomegalovirus, virus de la vacuna, virus de la viruela aviar, virus de la viruela de los canarios y virus Sindbis.
21. Vector según cualquiera de las reivindicaciones 14 a 20, en el que dicho virus es un virus quimérico, un virus híbrido, o un virus recombinante.
22. Vector según cualquiera de las reivindicaciones 14 a 21, en el que dicho ligando que se dirige a una célula es una proteína original o una proteína recombinante.
23. Vector según cualquiera de las reivindicaciones 14 a 22, en el que dicho ligando que se dirige a una célula y dicho virus, están presentes en una proporción comprendida en el intervalo de 100 a 1.000.000 de moléculas de ligando por virión.
24. Vector según la reivindicación 23, en el que dicho ligando que se dirige a una célula y dicho virus están presentes en una proporción comprendida en el intervalo de 6.700 a 400.000 moléculas de ligando por virión.
25. Vector según cualquiera de las reivindicaciones 14 a 24, en el que dicho ligando que se dirige a una célula y dicho virus, están presentes en una proporción comprendida en el intervalo de 1 μg a 10 mg de dicho ligando por 1010 viriones.
26. Vector según la reivindicación 25, en el que dicho ligando que se dirige a una célula y dicho virus están presentes en una proporción comprendida en el intervalo de 10 μg a 600 μg de dicho ligando por 1010 viriones.
27. Procedimiento para preparar un vector para el suministro sistémico de un virus a una célula diana, comprendiendo dicho vector un ligando que se dirige a una célula, unido no covalentemente a dicho virus, que comprende mezclar una composición constituida por dicho ligando que se dirige a una célula con dicho virus en un medio acuoso, uniéndose dicho ligando de manera no covalente a dicho virus, en el que dicho ligando está constituido por transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF.
28. Procedimiento según la reivindicación 27, en el que dicha solución acuosa incluye uno o más agentes tampón, un agente que ajusta la osmolaridad o un antibiótico.
29. Complejo virus-ligando que se dirige a una célula según cualquiera de las reivindicaciones 1 a 13, para su utilización como un medicamento.
30. Vector según cualquiera de las reivindicaciones 14 a 28, para su utilización como un medicamento.
31. Utilización de un virus para la preparación de un agente terapéutico que comprende un vector que comprende un complejo virus-ligando que se dirige a una célula, para el suministro de dicho virus a una célula diana en el interior de un animal, en la que dicho complejo virus-ligando está constituido por un ligando y un virus, y en la que el ligando está unido de manera no covalente al virus, y es la transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF.
32. Utilización según la reivindicación 31, en la que dicho animal es un humano.
33. Utilización según la reivindicación 31 ó 32, en la que dicho agente terapéutico se administra sistémicamente.
34. Utilización según la reivindicación 31 ó 32, en la que dicho agente terapéutico se administra parenteralmente.
35. Utilización según la reivindicación 31 ó 32, en la que dicho agente terapéutico se administra intravenosa o intraarterialmente.
36. Utilización según la reivindicación 31 ó 32, en la que dicho agente terapéutico se administra intratumoralmente.
37. Utilización según cualquiera de las reivindicaciones 31 a 36, en la que dicho vector codifica el p53 de tipo salvaje.
38. Utilización según cualquiera de las reivindicaciones 31 a 37, en la que dicho agente terapéutico se administra a un animal que recibe quimioterapia además de dicho agente terapéutico.
39. Utilización según cualquiera de las reivindicaciones 31 a 37, en la que dicho agente terapéutico se administra a un animal que recibe tratamiento con radiación además de dicho agente terapéutico.
40. Utilización según cualquiera de las reivindicaciones 31 a 39, en la que dicho animal presenta cáncer de cabeza y cuello, vejiga, mama, tiroides, ovarios, cerebro, próstata, un melanoma o un linfoma.
41. Utilización según cualquiera de las reivindicaciones 31 a 33 y 37 a 40, en la que dicho virus comprende un ácido nucleico que codifica el p53 de tipo salvaje, en la que además dicho ligando que se dirige a una célula, es transferrina, y siendo además dicho agente terapéutico administrado sistémicamente.
42. Utilización según la reivindicación 33 ó 36,
en la que la célula diana es una célula cancerosa seleccionada de entre un cáncer de cabeza y cuello, cáncer de vejiga, cáncer de mama, cáncer de tiroides, cáncer de ovarios, cáncer de próstata, un melanoma y un linfoma;
estando el vector constituido esencialmente por el virus y uniéndose directamente a un receptor que está sobreexpresado en la célula cancerosa.
43. Utilización según la reivindicación 42, en la que el virus sensibiliza la célula cancerosa a la radiación o a la quimioterapia.
44. Utilización según la reivindicación 43, en la que el virus comprende un ácido nucleico de interés, cuya expresión en la célula cancerosa sensibiliza la célula cancerosa a la radiación o a la quimioterapia.
45. Utilización según la reivindicación 40, en la que el virus comprende un ácido nucleico que, cuando se expresa en las células cancerosas, sensibiliza la célula a la radiación o a la quimioterapia;
uniéndose el ligando directamente a un receptor en la célula cancerosa; y
estando el vector constituido esencialmente por el virus y el ligando.
46. Vector para su utilización en el suministro de un virus a una célula diana en el interior de un animal, en el que el vector comprende un complejo virus-ligando que se dirige a una célula, en el que dicho complejo virus-ligando está constituido por un ligando y un virus, y en el que el ligando está unido de manera no covalente al virus, y es la transferrina, un anticuerpo receptor de la transferrina, un fragmento de un anticuerpo receptor de la transferrina, EGF o VEGF.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]