PROCEDIMIENTOS ÚTILES PARA LA MODULACIÓN DE LA ANGIOGÉNESIS QUE UTILIZAN LA TIROSINA CINASA Src.
Composición farmacéutica para su utilización en un procedimiento destinado a potenciar la angiogénesis en un tejido diana de mamífero asociado a una enfermedad seleccionada de entre el grupo constituido por mala circulación,
extremidades isquémicas y heridas crónicas, comprendiendo dicha composición farmacéutica un vector de expresión vírico o no vírico que codifica una secuencia nucleotídica que puede expresar una proteína Src, que presenta cualquier resto de aminoácido en el codón 527 excepto tirosina, serina o treonina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/011780.
Solicitante: THE SCRIPPS RESEARCH INSTITUTE
THE GOVERNMENT OF THE UNITED STATES OF AMERICA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 10550 North Torrey Pines Road, Mail Drop TRC 8 La Jolla, CA 92037 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHERESH, DAVID, A., ELICEIRI,BRIAN, SCHWARTZBERG,Pamela L.
Fecha de Publicación: .
Fecha Solicitud PCT: 28 de Mayo de 1999.
Clasificación Internacional de Patentes:
- C12N9/12 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › transfieren grupos que contienen fósforo, p. ej. Quinasas (2.7).
Clasificación PCT:
- A61K38/45 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Transferasas (2).
- A61P19/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para problemas de las articulaciones, p.ej. artritis, artrosis.
- A61P35/00 A61P […] › Agentes antineoplásicos.
Clasificación antigua:
- C12N9/00 C12N […] › Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2361659_T3.pdf
Fragmento de la descripción:
Campo técnico
La presente invención se refiere generalmente al campo de la medicina, y se refiere específicamente a procedimientos y composiciones para modular la angiogénesis de tejidos que utilizan la proteína tirosina cinasa Src, variantes de Src y a los ácidos nucleicos que las codifican.
Antecedentes
La angiogénesis es un proceso de vascularización tisular que implica el desarrollo de nuevos vasos sanguíneos en un tejido, y se hace asimismo referencia al mismo como neovascularización. El procedimiento está mediado por la infiltración de células endoteliales y células de músculo liso. El procedimiento se cree que procede en alguna de las tres formas: los vasos pueden brotar de vasos preexistentes, el desarrollo de nuevos vasos puede surgir de células madre (vasculogénesis) o pequeños vasos existentes pueden aumentar de diámetro. Blood et al., Bioch. Biophys. Acta, 1032:89-118 (1990).
La angiogénesis es un proceso importante en el desarrollo de los recién nacidos, pero es también importante en la cicatrización de heridas y en la patogenia de una gran variedad de enfermedades clínicas incluyendo la inflamación de tejidos, artritis, crecimiento tumoral, retinopatía diabética, degeneración macular por neovascularización de la retina y enfermedades similares. Estas manifestaciones clínicas asociadas a la angiogénesis se denominan enfermedades angiogénicas. Folkman et al., Science, 235:442-447 (1987). La angiogénesis está generalmente ausente en tejidos de adultos o maduros, aunque se produce en la cicatrización de heridas y en el ciclo del crecimiento del cuerpo lúteo. Véase, por ejemplo, Moses et al., Science, 248:1408-1410 (1990).
Se ha propuesto que la inhibición de la angiogénesis sería una terapia útil para restringir el crecimiento tumoral. La inhibición de la angiogénesis ha sido propuesta por (1) inhibición de la liberación de “moléculas angiogénicas” tales como FGFb (factor de crecimiento de fibroblastos básico), (2) neutralización de moléculas angiogénicas, tales como mediante la utilización de anticuerpos anti-βbFGF, (3) utilización de inhibidores de receptor de vitronectina αvβ3 y (4) inhibición de la respuesta de células endoteliales a estímulos angiogénicos. Esta última estrategia ha recibido atención, y Folkman et al., Cancer Biology, 3:89-96 (1992), han descrito varios inhibidores de la respuesta a las células endoteliales, incluyendo el inhibidor de colagenasa, los inhibidores de recambio de la membrana basal, esteroides angioestáticos, inhibidores de la angiogénesis procedente de hongos, factor 4 de plaquetas, trombospondina, fármacos para la artritis tales como D-penicilamina y tiomalato de oro, análogos de la vitamina D3, interferón alfa y similares que pueden utilizarse para inhibir la angiogénesis. Para inhibidores adicionales propuestos de angiogénesis, véase Blood et al., Bioch. Biophys. Acta, 1032:89-118 (1990), Moses et al., Science, 248:14081410 (1990), Ingber et al., Lab. Invest., 59:44-51 (1988) y patentes US nº 5.092.885, nº 5.112.946, nº 5.192.744, nº 5.202.352, nº 5.753.230 y nº 5.766.591. Ninguno de los inhibidores de la angiogénesis descritos en las referencias anteriores implica las proteínas Src.
Para que se produzca angiogénesis, las células endoteliales deben degradarse en primer lugar y atravesar la membrana basal del vaso sanguíneo de manera similar a la utilizada por las células tumorales durante la invasión y la formación de la metástasis.
Se ha publicado anteriormente que la angiogénesis depende de la interacción entre las integrinas vasculares y las proteínas de la matriz extracelular. Brooks et al., Science, 264:569-571 (1994). Además, se publicó que la muerte celular programada (apoptosis) de las células vasculares angiógenas se inicia por la interacción, que estaría inhibida por determinados antagonistas de la integrina vascular α,β3. Brooks et al., Cell, 79:1157-1164 (1994). Más recientemente, se ha publicado que la unión de la metaloproteinasa-2 de la matriz (MMP-2) al receptor de vitronectina (α,β3) puede inhibirse utilizando antagonistas de α,β3., y de este modo inhibir la función enzimática de la proteinasa. Brooks et al., Cell, 85:683-693 (1996).
El documento WO 98/16638 se refiere a ligandos que incluyen secuencias de aminoácidos que se unen a por lo menos dos dominios de una proteína diana, en la que ligandos particularmente preferidos incluyen los que se dirigen a los dominios 2 y 3 de la homología Src de las proteínas eucarióticas tirosina cinasas.
Marx, M. y Dorsch, O. (Kidney Int., 1997, Vol. 51(1):110-8) dan a conocer que c-src ejerce efectos reguladores sobre la proliferación de células del mesangio, la organización citoesquelética, proteasas de la matriz y diferenciación.
Russel R. et al.(Proc. Natl. Acad. Sci., USA.,1991, Vol. 88:10696-10700) publican que la fosforilación del terminal carboxilo de pp-60c-src, producto del protooncogen c-src, en Tyr-527 suprime la actividad de tirosina cinasa y la transformación potencial.
Irby R. et al. (Surgical Forum,1998, Vol. 49:395-396) dan a conocer una implicación de Src en la iniciación y evolución del cáncer de colon.
Sumario de la invención
La presente invención se refiere a la modulación de la angiogénesis en tejidos por la tirosina cinasa Src, además en la presente memoria se denomina genéricamente Src, como se define en las reivindicaciones.
Se contemplan las composiciones y utilizaciones para modular la angiogénesis en un tejido asociada a una enfermedad. Una composición que comprende una cantidad moduladora de angiogénesis de una proteína Src debe administrarse al tejido para ser considerada una enfermedad que responde a la modulación de la angiogénesis. La composición que proporciona la proteína Src puede contener proteína purificada, fragmentos de proteína biológicamente activa, proteína Src, fragmentos de proteína o proteínas de fusión de los mismos producidos por recombinación o vectores de expresión de gen/ácido nucleico para expresar una proteína Src.
Cuando la proteína Src se inactiva o inhibe, la modulación es una inhibición de la angiogénesis. Cuando la proteína Src está activa o activada, la modulación es una potenciación de la angiogénesis.
El tejido que va a tratarse puede ser cualquier tejido en el que se desee la modulación de la angiogénesis. Para la inhibición de la angiogénesis, es útil tratar el tejido enfermo en el que se produce la neovascularización perjudicial. Los tejidos ejemplificativos incluyen tejido inflamado, tumores sólidos, metástasis, tejidos que experimentan restenosis y tejidos similares.
Para la potenciación, es útil tratar a los pacientes con extremidades isquémicas en las que existe una escasa circulación en las extremidades de diabéticos u con otras enfermedades. Pueden tratarse también los pacientes con heridas crónicas que no cicatrizan y por lo tanto podrían beneficiarse del aumento en la proliferación de células vasculares y neovascularización.
Resulta particularmente preferida la utilización de la proteína Src que contiene una secuencia de aminoácidos modificada como se describe en la presente memoria. Varias proteínas Src modificadas particularmente útiles y la expresión de las mismas se describen en la presente memoria.
La presente invención comprende además una composición farmacéutica para estimular la angiogénesis en un tejido diana de mamífero que comprende un vector de transferencia génica vírico o no vírico que contiene un ácido nucleico y un vehículo o excipiente farmacéuticamente aceptable; teniendo dicho ácido nucleico un segmento de ácido nucleico que codifica una proteína Src, teniendo dicha proteína Src algún resto de aminoácido en el codón 527 excepto tirosina, serina o treonina.
Está asimismo prevista una composición farmacéutica para inhibir la angiogénesis en un tejido diana de mamífero que comprende un vector de transferencia génica vírico o no vírico que contiene un ácido nucleico y un vehículo o excipiente farmacéuticamente aceptable; presentando dicho ácido nucleico un segmento de ácido nucleico que codifica una proteína Src que no presenta actividad de cinasa.
Breve descripción de los dibujos
En los dibujos que forman parte de la presente exposición:
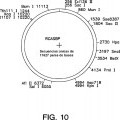
La figura 1 es una secuencia de ADNc de c-Src de pollo que es la secuencia de codificación completa con los intrones eliminados... [Seguir leyendo]
Reivindicaciones:
1. Composición farmacéutica para su utilización en un procedimiento destinado a potenciar la angiogénesis en un tejido diana de mamífero asociado a una enfermedad seleccionada de entre el grupo constituido por mala circulación, extremidades isquémicas y heridas crónicas, comprendiendo dicha composición farmacéutica un vector de expresión vírico o no vírico que codifica una secuencia nucleotídica que puede expresar una proteína Src, que presenta cualquier resto de aminoácido en el codón 527 excepto tirosina, serina o treonina.
2. Composición farmacéutica según la reivindicación 1, en la que dicho vector es un vector vírico de transferencia génica y en la que dicha composición contiene además un vehículo o excipiente farmacéuticamente aceptable.
3. Composición farmacéutica según la reivindicación 1, en la que dicha proteína Src es Src A.
4. Composición farmacéutica según la reivindicación 1, en la que dicho tejido presenta mala circulación.
5. Composición farmacéutica según la reivindicación 1, en la que dicha composición farmacéutica debe administrarse mediante administración intravenosa, transdérmica, intrasinovial, intramuscular u oral.
6. Composición farmacéutica según la reivindicación 1, en la que dicha composición farmacéutica debe administrarse como una sola dosis por vía intravenosa.
7. Composición farmacéutica según la reivindicación 1, en la que dicha composición farmacéutica comprende además un liposoma.
8. Utilización de una proteína Src que presenta cualquier resto de aminoácido en el codón 527 excepto tirosina, serina o treonina o una secuencia nucleotídica que puede expresar dicha proteína para la preparación de una composición farmacéutica destinada a potenciar la angiogénesis en un tejido asociado a una enfermedad seleccionada de entre el grupo constituido por mala circulación, extremidades isquémicas y heridas crónicas.
9. Utilización según la reivindicación 8, en la que dicha proteína Src es Src A.
10. Utilización según la reivindicación 8, en la que dicho tejido presenta una mala circulación.
11. Utilización de una proteína Src inactiva o de una secuencia nucleotídica que puede expresar dicha proteína para la preparación de una composición farmacéutica destinada a inhibir la angiogénesis en un tejido asociado a una enfermedad seleccionada de entre el grupo constituido por artritis, artritis reumatoide, tumor sólido, metástasis del tumor sólido, retinopatía, retinopatía diabética, degeneración macular, restenosis y enfermedades inflamatorias.
12. Utilización según la reivindicación 11, en la que dicha proteína Src inactiva es Src 251 o Src K295M.
13. Utilización según la reivindicación 11, en la que dicho tejido está inflamado y dicha enfermedad es la artritis o la artritis reumatoide.
14. Utilización según la reivindicación 11, en la que dicho tejido es un tumor sólido o una metástasis de tumor sólido.
15. Utilización según la reivindicación 14, en la que la administración de dicha composición farmacéutica se realiza juntamente con la quimioterapia.
16. Utilización según la reivindicación 11, en la que dicho tejido es el tejido retiniano y dicha enfermedad es retinopatía, retinopatía diabética o degeneración macular.
17. Utilización según la reivindicación 11, en la que dicho tejido está en la zona de la angioplastia coronaria y dicho tejido presenta riesgo de restenosis.
18. Utilización según la reivindicación 8 u 11, en la que la administración de dicha composición farmacéutica comprende la administración intravenosa, transdérmica, intrasinovial, intramuscular u oral.
19. Utilización según la reivindicación 8 u 11, en la que la administración de dicha composición farmacéutica comprende una sola dosis por vía intravenosa.
20. Utilización según la reivindicación 8 u 11, en la que dicha composición farmacéutica comprende además un liposoma.
21. Utilización según la reivindicación 8 u 11, en la que dicha composición farmacéutica comprende un vector de expresión retrovírica que puede expresar dicha secuencia nucleotídica.
22. Utilización según la reivindicación 8 u 11, en la que dicha composición farmacéutica comprende un vector de expresión no vírica que puede expresar dicha secuencia nucleotídica.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Regulador de la secreción hormonal, composición que lo contiene y procedimiento para controlar la secreción hormonal mediante su uso, del 17 de Junio de 2020, de Gemvax & Kael Co., Ltd: Un modulador de la secreción hormonal que comprende un péptido que incluye una secuencia de aminoácidos de SEQ ID NO: 1, una secuencia de aminoácidos que […]
Microorganismo con productividad de l-lisina aumentada y procedimiento para producir l-lisina utilizando el mismo, del 27 de Mayo de 2020, de CJ CHEILJEDANG CORPORATION: Una subunidad beta prima (subunidad-β') mutante de la ARN polimerasa, en la que la subunidad beta prima (subunidad-β') mutante de la ARN polimerasa tiene […]
Isoforma novedosa de cinasa de linfoma anaplásico y sus usos, del 20 de Mayo de 2020, de Memorial Sloan Kettering Cancer Center: Molécula de ácido nucleico aislado que comprende o que consiste esencialmente en los exones 20-29 y una parte, pero no todo, del intrón 19 de un gen de cinasa de […]
Compuesto de péptido farmacológicamente activo, procedimiento de preparación y uso del mismo, del 29 de Abril de 2020, de Messina, Angela Anna: Un péptido sintético que consiste en la secuencia de aminoácidos IAAQLLAYYFT (ID de SEC nº 1).
Método de amplificación de ADN circular, del 22 de Abril de 2020, de OriCiro Genomics, Inc: Un método para amplificar exponencialmente ADN circular mediante la repetición de ciclos de replicación, que comprende una etapa de: formar una […]
Fábrica de células bacterianas modificadas genéticamente para la producción de tiamina, del 22 de Abril de 2020, de Biosyntia ApS: Bacteria modificada genéticamente para la producción de tiamina no fosforilada; en la que dicha bacteria se caracteriza por tener transgenes […]
Polimerasas modificadas para la incorporación mejorada de análogos de nucleótidos, del 15 de Abril de 2020, de ILLUMINA, INC: Una ADN polimerasa de arqueas de la familia B alterada que comprende mutaciones de sustitución de aminoácidos en posiciones posicionalmente equivalentes a Leu408, Tyr409, Pro410 […]