MÉTODOS DE AUMENTO DE LA FUNCIÓN LINFÁTICA.
Uso de (a) un agente que disminuye la expresión, actividad o nivel de VEGF-A,
el agente seleccionado de (i) un anticuerpo que se une a VEGF-A o VEGFR-2 y disminuye la señalización de VEGF-A, (ii) VEGF-A inactivo, mutado que se une a VEGFR-2 e interrumpe la señalización de VEGF-A, (iii) VEGFR-2 o un fragmento del mismo que se une a VEGF-A e interrumpe la señalización de VEGF-A, (iv) un ácido nucleico de VEGF-A o VEGFR-2 que se puede unir a una secuencia celular de ácido nucleico de VEGF-A o VEGFR-2 y puede inhibir la expresión de VEGF-A o VEGFR-2, por ejemplo, un antisentido, ARNip o ribozimas, (v) inhibidores de la tirosina quinasa del receptor de VEGF, para la preparación de un medicamento para reducir el daño en la piel inducido por UVB crónica o aguda, en donde el medicamento comprende además (b) un agente que aumenta la expresión, actividad o nivel de un f a c t o r l i n f a n g i o g é n i c o , e n d o n d e e l f a c t o r linfangiogénico es VEGF-C, VEGF-D o VEGFR-3, el agente seleccionado de: (i) polipéptido VEGF-C o -D , o u n f r a g m e n t o biológicamente activo del mismo, (ii) un ácido nucleico que codifica un polipéptido VEGFC o -D, o un fragmento biológicamente activo del mismo, o (iii) un ácido nucleico de VEGFR-3
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/001309.
Solicitante: THE GENERAL HOSPITAL CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 55 FRUIT STREET BOSTON, MA 02114 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KAJIYA,KENTARO, DETMAR,MICHAEL.
Fecha de Publicación: .
Fecha Solicitud PCT: 18 de Enero de 2007.
Fecha Concesión Europea: 11 de Agosto de 2010.
Clasificación Internacional de Patentes:
- A61K38/17C
- A61K8/64 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 8/00 Cosméticos o preparaciones similares para el aseo. › Proteínas; Péptidos; Sus derivados o sus productos de degradación.
- A61Q19/00K
- C07K16/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra factores de crecimiento.
- G01N33/68R
Clasificación PCT:
- A61K31/7088 A61K […] › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K38/18 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento; Reguladores de crecimiento.
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P17/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 17/00 Medicamentos para el tratamiento de problemas dermatológicos. › para tratar heridas, úlceras, quemaduras, cicatrices, queloides o similares.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
ANTECEDENTES
El sistema linfático vascular está compuesto de una densa red de capilares de paredes finas que drenan la linfa rica en proteínas del espacio extracelular. Sus principales papeles incluyen el mantenimiento de la homeostasis tisular de líquidos y la mediación de la respuesta inmune aferente (Oliver et al. (2002) Genes Dev. 16:773-83; Witte et al. (2001) Microsc. Res. Tech. 55:122-45). Una función conocida de los vasos linfáticos es el drenaje de líquido tisular de tejidos normales e
15 inflamados (Kunstfeld et al. (2004) Blood 104:1048-57). La publicación internacional de patente número WO 2005/097187 describe que el daño en la piel, tal como el daño en la piel inducido por UVB aguda, se puede reducir en un sujeto, administrando a un sujeto que tiene, o está expuesto a, daño en
20 la piel inducido por UVB aguda, un agente que inhibe la señalización de VEGF. El artículo titulado “Upregulation of neuropilin-1 by basic fibroblast growth factor enhances vascular smooth muscle cell migration in response to VEGF” de Liu et al. (Cytokine, vol. 32:5, p. 206-212 (2005)) describe que la neuropilina-1 (NRP-1) es un co-receptor para el factor de crecimiento endotelial vascular (VEGF). Durante la neovascularización, las células vasculares del músculo liso (VSMC) y pericitos modulan la función de las células endoteliales. Los factores que median NRP-1 en las VSMC humanas (hVSMC) permanecen por elucidar. Se estudiaron varias citoquinas angiogénicas para identificar factores que aumentan la expresión de NRP-1 en hVSMC. El tratamiento de hVSMC con factor de crecimiento de fibroblastos básico (b-FGF) indujo expresiones del ARNm y proteína de NRP-1 mientras que el factor de crecimiento epidérmico, el factor de crecimiento de tipo insulínico-1 e interleuquina-1β no. b-FGF
indujo la fosforilación de Erk-1/2 y JNK. Los inhibidores de MEK1/2 y factor nuclear kappa B (NF-κB) (U0126 y TLCK, respectivamente) bloquearon la capacidad de b-FGF de inducir la expresión del ARNm de NRP-1, pero la inhibición de la actividad 5 JNK (SP600125) o PI3-quinasa (wortmanina) no. Además, el aumento en la expresión de NRP-1 por b-FGF aumentó la migración de hVSMC en respuesta a VEGF165. Este efecto era dependiente de la unión de VEGF165 a VEGFR-2, ya que anticuerpos bloqueantes contra VEGFR-2, pero no contra VEGFR-1, inhibieron la migración 10 inducida por VEGF165. En conclusión, b-FGF aumentó la expresión de NRP-1 en hVSMC que a su vez aumentó el efecto de VEGF165 en migración celular. La migración aumentada de las hVSMC estaba mediada a través de la unión de VEGF165 tanto a NRP-1 como a VEGFR-2, ya que la inhibición de VEGFR-2 en estas células
15 bloqueó los efectos de la migración celular mediados por VEGF. El artículo titulado “Overexpression of VEGF-C causes transient lymphatic hyperplasia but not increased lymphangiogenesis in regenerating skin” de Goldman et al. (Circ. Res., vol. 96:11 p. 1193-9 (2005)) describe que el factor de crecimiento endotelial vascular (VEGF)-C es necesario para la linfangiogénesis y tiene potencial para terapia linfangiogénica en enfermedades que carecen de drenaje linfático adecuado. Sin embargo, la capacidad de VEGF-C de aumentar el crecimiento linfático funcional sostenible en tejidos permanece poco claro. Para abordar esto, se evaluó la sobreexpresión de VEGF-C en linfangiogénesis adulta en piel en regeneración. Se usó un modelo de regeneración de piel de cola de ratón que incorpora una suspensión de células tumorales que sobreexpresan VEGF-C, lo que proporciona un suplemento continuo de exceso de VEGF-C al medio natural de regeneración durante más de 25 días, o células tumorales control transfectadas de otra manera idénticas. Se encontró que el exceso de VEGF-C no aumentó la velocidad de migración de células linfáticas endoteliales (LEC), la densidad de vasos linfáticos o la tasa de funcionalidad, incluso aunque anteriormente estaba presente hiperplasia linfática. Además, la hiperplasia desapareció cuando los niveles de VEGF-C
disminuyeron, lo que se produjo después de 25 días, lo que hace los linfáticos indistinguibles de aquellos en los grupos control. In vitro, se mostró que mientras el VEGF-C derivado de células pudo inducir quimioatracción de LEC a través de una 5 membrana (que implica transmigración de tipo ameboidea), no aumentó la quimioinvasión de LEC en una matriz de fibrina tridimensional (que requiere migración proteolítica). Estos resultados sugieren que mientras que el exceso de VEGF-C puede aumentar la proliferación temprana de LEC y producir hiperplasia 10 de vasos linfáticos, no aumenta la tasa fisiológica de migración
o funcionalidad, y por sí mismo no puede sostener ningún efecto duradero en tamaño, densidad u organización linfática en piel adulta en regeneración.
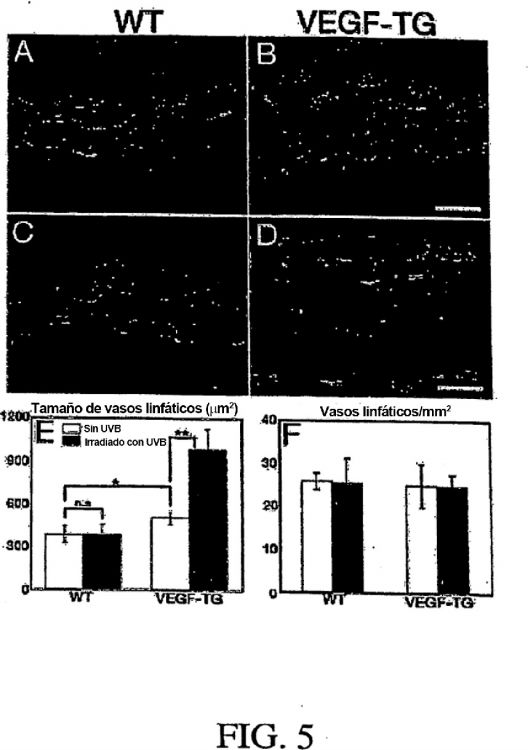
15 COMPENDIO Se describe que tanto la irradiación aguda como crónica con UVB de piel murina produce agrandamiento importante de vasos linfáticos. Sorprendentemente, estos vasos linfáticos agrandados están funcionalmente deteriorados y son hiperpermeables, detectado mediante linfangiografia intravital. Los niveles de expresión del factor de crecimiento endotelial vascular (VEGF)A, pero no de los factores linfangiogénicos conocidos VEGF-C o – D aumentaron en epidermis irradiada con UVB. La sobreexpresión dirigida de VEGF-A en epidermis de ratones transgénicos produjo agrandamiento y fuga incrementados de vasos linfáticos después de irradiación aguda con UVB, mientras que el bloqueo sistémico de la señalización de VEGF-A previno en gran parte anormalidades en los vasos linfáticos y fotodaño inducido por UVB. En conjunto, estos descubrimientos indican que los vasos linfáticos son diana de fotodaño cutáneo inducido por UVB y que VEGF-A media el deterioro de la función de vasos linfáticos y por tanto contribuye a los afectos adversos de la irradiación de UVB sobre la piel.
En un aspecto, la divulgación presenta métodos de reducir 35 el daño en la piel inducido por UVB disminuyendo la actividad o niveles de VEGF-A en la piel, por ejemplo, en la cara, pecho,
cuello, manos u otras regiones del cuerpo. Estos métodos pueden incluir además aumentar la actividad o niveles de un factor linfangiogénico, por ejemplo, VEGF-C o VEGF-D, en la piel.
En otro aspecto, la divulgación presenta métodos de reducir 5 edema disminuyendo la actividad o niveles de VEGF-A.
En aún otro aspecto, la divulgación presenta métodos de reducir el daño en la piel inducido por UVB, por ejemplo, en la cara, pecho, cuello, manos u otras regiones de cuerpo, fomentando la función linfática.
10 En todavía otro aspecto, la divulgación presenta métodos de cribado para un inhibidor de la actividad de VEGF-A proporcionando una célula con un receptor transmembrana que se puede unir y responder a VEGF-A; poniendo en contacto la célula con un polipéptido que incluye VEGF-A o un fragmento del mismo en presencia de un compuesto de prueba, por ejemplo, un producto
A. 20 En aún otro aspecto, la divulgación presenta métodos de cribado para un inhibidor de la actividad VEGF-A al proporcionar un primer polipéptido que incluye una parte de un receptor transmembrana que se puede unir a VEGF-A; poner en contacto el polipéptido con un segundo polipéptido que incluye VEGF-A o un fragmento del mismo en presencia de un compuesto de prueba, por ejemplo un producto o extracto natural; y evaluar la unión del primer polipéptido al segundo polipéptido, en donde un compuesto de prueba que inhibe la unión del primer polipéptido al segundo polipéptido es un inhibidor de la actividad VEGF-A. 30 En todavía otro aspecto, de cribado para un inhibidor de la expresión de VEGF-A, el método comprende: (a) proporcionar una célula que tiene una región promotora de VEGF-A; (b) exponer la célula a radiación UVB; (c) antes, durante o después de b), poner en contacto la célula con un compuesto de prueba, por ejemplo, un producto o extracto natural; y (d) medir la expresión dirigida por la región promotora, en donde un compuesto de prueba que disminuye la expresión es un inhibidor de la expresión de VEGF-A. En un aspecto, la divulgación presenta un método de tratar a un sujeto que tiene daño en la piel inducido por UVB, por ejemplo, en la cara, pecho, cuello, manos u otras regiones del...
Reivindicaciones:
3. El uso según la reivindicación 1 ó 2, en donde el agente que disminuye la expresión, actividad o nivel de VEGF-A es un antagonista del receptor de VEGF.
4. El uso según la reivindicación 1 ó 2, en donde el agente que disminuye la expresión, actividad o nivel de VEGF-A es un inhibidor de la actividad tirosina quinasa del receptor de VEGF.
5. El uso según la reivindicación 1 ó 2, en donde el agente que disminuye la expresión, actividad o nivel de VEGF-A es un anticuerpo anti-VEGF.
6. El uso según la reivindicación 1 ó 2, en donde el agente que aumenta la expresión, actividad o nivel de un factor linfangiogénico es un polipéptido VEGF-C o –D, o un fragmento biológicamente activo del mismo.
57
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Método para el tratamiento de la osteoporosis, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina que comprende una CDR-H1 de la SEQ ID NO: 245, una CDR-H2 de la SEQ ID NO: 246, una CDR-H3 de la SEQ ID NO: 247, […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
 Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
Método para tratar la pérdida de hueso alveolar mediante el uso de anticuerpos antiesclerostina, del 3 de Junio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina para su uso en un método para aumentar la altura del hueso alveolar en un sujeto que padece pérdida de hueso alveolar, donde […]
Proteínas de captura de la superficie celular recombinantes, del 13 de Mayo de 2020, de REGENERON PHARMACEUTICALS, INC.: Un método para detectar y aislar células que producen altos niveles de una proteína heterodimérica que tiene una primera subunidad y una segunda subunidad, […]