MÉTODO PARA OBTENER LÍNEAS DE CÉLULAS EMPAQUETADORAS RETROVIRALES, PRODUCTORAS DE UN SOBRENADANTE RETROVIRAL DE ELEVADA EFICACIA DE TRANSDUCCIÓN.
ESTA INVENCION DESCRIBE UN PROCEDIMIENTO PARA OBTENER UNA CELULA DE ENCAPSULACION RETROVIRICA RECOMBINANTE,
CAPAZ DE PRODUCIR VECTORES RETROVIRICOS, ASI COMO LA CELULA DE ENCAPSULACION RECOMBINANTE OBTENIDA MEDIANTE EL PROCEDIMIENTO. TAMBIEN SE DESCRIBE UN PROCEDIMIENTO PARA PRODUCIR PARTICULAS RETROVIRICAS RECOMBINANTES, OBTENIDAS INTRODUCIENDO EN LAS CELULAS DE ENCAPSULACION OBTENIDAS SEGUN LOS PROCEDIMIENTOS DESCRITOS EN LA PRESENTE, UN VECTOR RETROVIRICO RECOMBINANTE Y PROPAGANDO LAS CELULAS PRODUCTORAS RESULTANTES BAJO CONDICIONES FAVORABLES PARA LA PRODUCCION Y SECRECION DE SOBRENADANTE DE VECTOR RETROVIRICO. LOS SOBRENADANTES RETROVIRICOS PRODUCIDOS MEDIANTE ESTOS PROCEDIMIENTOS TAMBIEN SE REIVINDICAN EN LA PRESENTE. ESTA INVENCION ADEMAS DESCRIBE UN PROCEDIMIENTO PARA SELECCIONAR UN SOBRENADANTE DE VECTOR RETROVIRICO PARA OBTENER UNA ELEVADA EFICACIA DE TRANSDUCCION, Y PROCEDIMIENTOS PARA PRODUCIR UN SOBRENADANTE DE VECTOR RETROVIRICO PARA TRANSDUCIR CELULAS CON UNA ELEVADA EFICACIAEN APLICACIONES DE TERAPIA GENICA
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1996/020777.
Solicitante: SYSTEMIX, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3155 PORTER DRIVE PALO ALTO, CALIFORNIA 94304 ESTADOS UNIDOS DE AMERICA.
Inventor/es: PLAVEC, IVAN, RIGG,Richard,J, CHEN,Jingyi, DANDO,Jonathan,S, FORESTELL,Sean,P, BOHNLEIN,Ernst.
Fecha de Publicación: .
Fecha Solicitud PCT: 13 de Diciembre de 1996.
Clasificación Internacional de Patentes:
- C12N15/867P
Clasificación PCT:
- C12N15/85 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12N15/87 C12N 15/00 […] › Introducción de material genético extraño utilizando procedimientos no previstos en otro lugar, p. ej. cotransformación.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12N15/87 C12N 15/00 […] › Introducción de material genético extraño utilizando procedimientos no previstos en otro lugar, p. ej. cotransformación.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Mónaco, Irlanda, Finlandia.
Fragmento de la descripción:
Método para obtener líneas de células empaquetadoras retrovirales, productoras de un sobrenadante retroviral de elevada eficacia de transducción.
Campo técnico de la invención
Esta invención se refiere generalmente a la derivación y uso de líneas de células empaquetadoras para la producción de sobrenadante retroviral de transducción.
Antecedentes de la invención
La transferencia de genes humanos implica la transferencia de uno o más genes terapéuticos y las secuencias que controlan su expresión a células diana apropiadas. Se ha desarrollado un cierto número de sistemas de vectores para la transferencia de los genes terapéuticos para diversas indicaciones clínicas. La transferencia de genes in vivo implica la administración directa del vector a las células diana en un paciente. La transferencia de genes ex vivo implica separar células diana de un individuo, modificarlas ex vivo y devolver las células modificadas al paciente.
La mayoría de los protocolos de terapia génica aprobados para ensayos clínicos por el NIH Recombinant DNA Advisory Committee (RAC) han utilizado vectores retrovirales anfotrópicos (ORDA Reports Recombinant DNA Advisory Committee (RAC) Data Management Report, junio 1994, (1994) Human Gene Therapy 5:1295-1302). Los vectores retrovirales son el vehículo de elección, principalmente debido a la generalmente elevada tasa de transferencia de genes obtenida en experimentos con líneas de células y la capacidad de obtener una integración estable del material genético, asegurando que la progenie de la célula modificada vaya a contener el material genético transferido. Para una revisión de vectores retrovirales y su uso en la transferencia y expresión de genes extraños, véase Gilboa (1988) Adv. Exp. Med. Biol. 241:29; Luskey et al. (1990) Ann. N.Y. Acad. Sci. 612: 398; y Smith (1992) J. Hematother 1:155-166.
Muchos vectores retrovirales actualmente en uso se derivan del virus de la leucemia murina de Moloney (MMLV- siglas en inglés). En la mayoría de los casos, las secuencias virales gag, pol y env se separan del virus, permitiendo la inserción de secuencias de ADN extraño. Genes codificados por el ADN extraño son a menudo expresados bajo el control del fuerte promotor viral en la LTR. Una construcción de este tipo se puede empaquetar, eficazmente, en partículas de vector si las funciones gag, pol y env se proporcionan in trans mediante una línea de células empaquetadoras. Así, cuando la construcción del vector se introduce en la célula empaquetadora, las proteínas Gag-Pol y Env producidas por la célula se reúnen con el ARN del vector para producir viriones defectuosos en la replicación o transductores que son secretados en el medio de cultivo. Las partículas de vector, así producidas, pueden infectar e integrarse en el ADN de la célula diana, pero generalmente no producirán virus infecciosos, ya que carecen de secuencias virales esenciales.
La mayoría de las líneas de células empaquetadoras actualmente en uso han sido transfectadas con plásmidos separados que codifican Gag-Pol y Env, de modo que son necesarios múltiples eventos de recombinación antes de que se pueda producir un retrovirus competente para la replicación (RCR- siglas en inglés). Líneas de células empaquetadoras de vectores retrovirales, comúnmente utilizadas, se basan en la línea de células NIH/3T3 murina, e incluyen PA317 (Miller y Buttimore (1986) Mol. Cell. Biol. 6: 2895; Miller y Rosman (1989) BioTechniques 7: 980), CRIP (Danos y Mulligan (1988) Proc. Natl. Acad. Sci. USA 85: 6460) y gp + am12 (Markowitz et al. (1988) Virology 167: 400). A pesar de que la ruptura de los genes gag-pol y env dentro del genoma de la célula empaquetadora disminuye la incidencia de RCR, RCR se observa ocasionalmente en producciones a escala clínica de preparados de vectores retrovirales y es una preocupación de seguridad muy importante. Probablemente, esto se deba, al menos en parte, al hecho de que células NIH/3T3 contienen secuencias del MLV endógenas (Irving et al. (1993) Bio/Technol. 11: 1042-1046) que podrían participar en la recombinación para formar RCR (Cosset et al. (1993) Virology 193:385-395 y Vanin et al. (1994) J. Virology 68: 4241-4250), particularmente en cultivos en masa durante la producción de vectores a gran escala clínica.
La gama de células hospedantes que pueden ser infestadas por un retrovirus o transducidas por un vector retroviral se determina por la proteína viral Env. El virus recombinante se puede utilizar para infestar virtualmente a cualquier tipo de célula reconocida por la proteína Env proporcionada por la célula empaquetadora, dando como resultado la integración del genoma viral en la célula transducida y la producción estable del producto génico extraño. La eficacia de la infección está también relacionada con el nivel de expresión del receptor en la célula diana. En general, Env ecotrópica murina de MMLV permite la infección de células de roedores, mientras que Env anfotrópica permite la infección de células de roedores, aves y de algunos primates, incluidas células humanas. Sistemas de vectores xenotrópicos que utilizan Env xenotrópica murina también permitirían la transducción de células humanas.
La gama de hospedadores de vectores retrovirales ha sido alterada sustituyendo la proteína Env del virus base con la de un segundo virus. La partícula de vector "pseudotipada" resultante tiene la gama hospedadora del virus que dona la proteína de la envoltura y que es expresada por la línea de células empaquetadoras. Por ejemplo, la glicoproteína G procedente del virus de la estomatitis vesicular (VSV-G) ha sido sustituida por la proteína Env de MMLV, ampliando con ello el intervalo de hospedadores. Véase, p. ej., Burns et al. (1993) Proc. Natl. Acad. Sci. USA 90: 8033-8037 y la solicitud de patente PCT internacional, nº de publicación WO 92/14829.
Los resultados inconsistentes y la transferencia ineficaz de genes a algunos tipos de células diana son dos problemas adicionales asociados con los actuales sistemas de vectores retrovirales. Por ejemplo, células madre hematopoyéticas son un tipo de célula diana atractivo para la terapia génica, debido a su capacidad de auto-renovación y a su capacidad para diferenciarse en todos los linajes hematopoyéticos, repoblando con ello a un paciente con las células modificadas. Sin embargo, la transferencia de genes retrovirales en células madre hematopoyéticas ha sido inconsistente e ineficaz de manera decepcionante. Kantoff et al. (1987) J. Exp. Med. 166: 219-234; Miller, A. D. (1990) Blood 76: 271-278; y Xu et al. (1994) J. Virol. 68: 7634. Esfuerzos para incrementar la eficacia de transferencia de genes incluyen producir sobrenadantes de vectores retrovirales de mayor título de punto final. El título de punto final es una medida del número de partículas de vector funcionales en un preparado que, cuando aumenta, debería aumentar en teoría la eficacia de la transducción al aumentar la relación de vector funcional a células diana, es decir, aumentar la multiplicidad de infección (m. o. i. - siglas en inglés). Sin embargo, a pesar de títulos de punto final incrementados, la eficacia de la transferencia de genes retrovirales (eficacia de la transducción) no ha aumentado de manera correspondiente (Xu et al. (1994), supra; Paul (1993) Hum. Gene Therapy 4: 609-615; Fraes-Lutz et al. (1994) 22: 857-865).
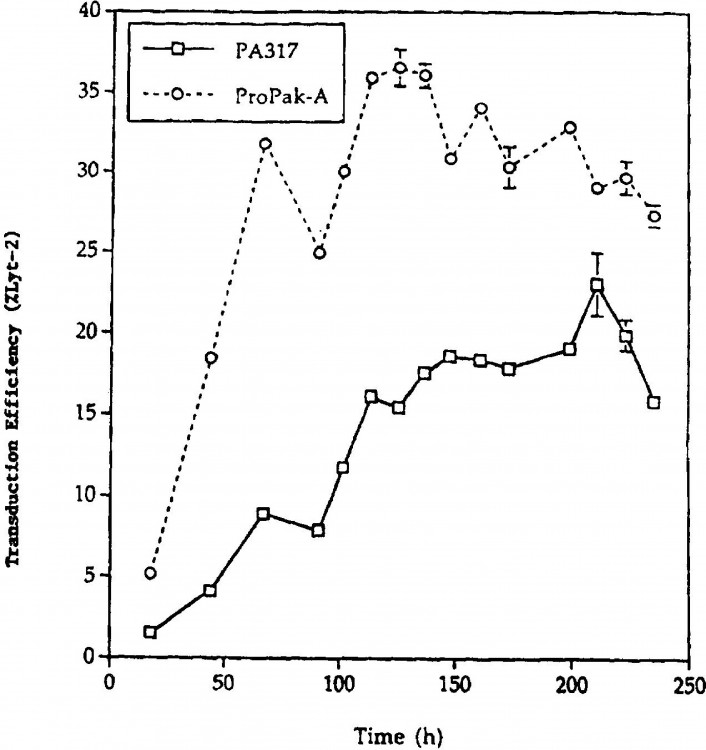
Esfuerzos para aumentar el título de punto final han incluido mejorar la producción de sobrenadantes de vectores retrovirales (véase Kotani et al. (1994) Human Gene Therapy, 5: 19-28) y la concentración física de partículas de vector mediante ultrafiltración (Paul, et al. (1993), supra. y Kotani, et al. (1994) supra). Se ha demostrado que la incubación de células productoras a 32ºC más que a 37ºC proporcionaba sobrenadantes con mayores títulos de punto final, pero no se compararon las eficacias de la transducción (véase Kotani et al. (1994) supra). Los autores de Kotani et al. (1994) supra, postularon que los elevados títulos se debían a una menor tasa de inactivación, combinada con una tasa más rápida de la producción de viriones a 32ºC. En otro estudio, la eficacia de la transducción...
Reivindicaciones:
1. Una célula empaquetadora viral recombinante, seleccionada del grupo consistente en ProPak-A.6 con el nº de acceso ATCC CRL 12006 y ProPak-X.36 con el nº de acceso ATCC CRL 12007.
Patentes similares o relacionadas:
SECRECIÓN MEJORADA DE NEUBLASTINA, del 2 de Marzo de 2011, de NSGENE A/S BIOGEN IDEC MA INC.: Ácido nucleico que comprende una secuencia polinucleotídica que codifica para un polipéptido que comprende un polipéptido de neublastina […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
 Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Procedimiento para la producción de polipéptidos, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Promotor que tiene la secuencia de ácido nucleico de SEQ ID NO: 02.
Ratones con un sistema inmunitario humanizado con células dendríticas reforzadas, del 22 de Julio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un ratón Rag-/-, γc-/-, Flk2-/- deficiente para el gen activador de recombinación 2 (Rag2) y/o el gen activador de recombinación 1 (Rag1), cadena gamma […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Expresión de proteína biotecnológica mejorada que usa un activador CHEF1 híbrido, del 17 de Junio de 2020, de AGC Biologics, Inc: Un vector de expresión que comprende ADN regulador de la transcripción del factor 1α de elongación de hámster chino (CHEF1) 5' y un activador de citomegalovirus (CMV) que […]
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]