ENSAYO IN VITRO PARA MEDIR LA INMUNOGENIA DE UNA VACUNA.
Un ensayo para medir la inmunogenia de una vacuna, en el que la vacuna comprende un epítopo que tiene una conformación asociada a una forma inmunogénicamente activa de la vacuna y un fragmento que tiene una conformación asociada a una forma inmunogénicamente inactiva de la vacuna,
en el que el método comprende exponer a una muestra de la vacuna a un primer anticuerpo monoclonal capaz de unirse al epítopo en la conformación asociada a la forma inmunogénicamente activa de la vacuna y a un segundo anticuerpo monoclonal capaz de unirse al fragmento en la conformación asociada a la forma inmunogénicamente inactiva de la vacuna y medir la cantidad de primer anticuerpo monoclonal unido a la muestra de vacuna y la cantidad del segundo anticuerpo monoclonal unido a la muestra de vacuna
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2001/028877.
Solicitante: MEDIMMUNE, LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE MEDIMMUNE WAY GAITHERSBURG, MD 20878 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SUZICH, JOANN, SCHENERMAN,Mark,A, WANG,Sheau-Chiann, STROUSE,Robert,J, WHITE,Wendy,I.
Fecha de Publicación: .
Fecha Solicitud PCT: 17 de Septiembre de 2001.
Clasificación Internacional de Patentes:
- C07K16/08A14
Clasificación PCT:
- A61K39/23 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Parvoviridae, p. ej. virus de la leucemia felina.
- A61K39/42 A61K 39/00 […] › virales.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- C12Q1/04 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › Determinación de la presencia o del tipo de microorganismo; Empleo de medios selectivos para la investigación o análisis de antibióticos o bactericidas; Composiciones para este fin que contienen un indicador químico.
- C12Q1/18 C12Q 1/00 […] › Investigación o análisis de la actividad antimicrobiana de un material.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
- C12Q1/70 C12Q 1/00 […] › en los que intervienen virus o bacteriófagos.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- A61K39/23 A61K 39/00 […] › Parvoviridae, p. ej. virus de la leucemia felina.
- A61K39/42 A61K 39/00 […] › virales.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- C12Q1/04 C12Q 1/00 […] › Determinación de la presencia o del tipo de microorganismo; Empleo de medios selectivos para la investigación o análisis de antibióticos o bactericidas; Composiciones para este fin que contienen un indicador químico.
- C12Q1/18 C12Q 1/00 […] › Investigación o análisis de la actividad antimicrobiana de un material.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
- C12Q1/70 C12Q 1/00 […] › en los que intervienen virus o bacteriófagos.
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2357381_T3.pdf





Fragmento de la descripción:
Referencia cruzada a la solicitud relacionada
Esta solicitud reivindica prioridad de la Solicitud Provisional de Estados Unidos Nº de Serie 60/233.439, presentada el 18 de septiembre de 2000, cuya totalidad se incorpora en este documento como referencia. 5
Antecedentes de la invención
Campo de la invención
La presente invención se refiere al campo de la medición in vitro de la inmunogenia de vacunas. En particular, la invención se refiere a la medición de la inmunogenia de vacunas en base a las propiedades de unión de formas inmunógenas y no inmunógenas de vacunas en base a partículas similares a virus. 10
Sumario de la técnica relacionada
Uno de los factores críticos en la determinación de la estabilidad de los productos de vacuna a granel y en viales es la medición de la inmunogenia. Por ejemplo, el ensayo de la potencia de partículas similares a un virus (VLP) de HPV-16 mediante la inmunización de ratones es una tarea que requiere mucho esfuerzo y tiempo. Típicamente, después de la inmunización del material de VLP formulado en ratones a diversos niveles de dosis, se requieren 15 aproximadamente seis semanas antes de que pueda determinarse si los animales son capaces de montar una respuesta inmune suficiente. Este problema se vuelve aún más difícil cuando se ensayan diversos adyuvantes y excipientes, debido al número de animales que deben utilizarse. En un esfuerzo por hacer más eficaces los esfuerzos de desarrollo es deseable encontrar un ensayo rápido y fiable que permita la evaluación de la inmunogenia de vacunas basadas en partículas similares a virus (VLP). 20
El documento de Ghim, SJ. et al., “Antigenicity of bovine papillomavirus type 1 (BPV-1) L1 virus-like particles compared that of intact BPV-1 virions” J. Gen. Virol., 77: 183 - 188, 1996 compara la antigenicidad de viriones de PV bovino de tipo 1 intacto (BPV-1) con el de VLP L1 de BPV recombinante mediante ELISA usando un panel bien caracterizado de anticuerpos policlonales y monoclonales generados contra partículas de BPV-1 intacto y desnaturalizado. 25
El documento White, W.I. et al., “Characterization of a major neutralizing epitope on human papillomavirus type 16 L1” J. Virol., 73 (6): 4882 - 4889, 1999 describe la unión de tres anticuerpos monoclonales a partículas similares a virus con L1 del virus del papiloma humano de tipo 16 compuestas por la secuencia de referencia L1 y tres secuencias variantes de L1.
Sumario y objetos de la invención 30
Es un objeto de la invención proporcionar un ensayo para medir la inmunogenia de una vacuna, en el que la vacuna comprende un epítopo que tiene una conformación asociada a una forma inmunogénicamente activa de la vacuna y un fragmento que tiene una conformación asociada a una forma inmunogénicamente inactiva de la vacuna. El método comprende exponer a una muestra de la vacuna a un primer anticuerpo monoclonal capaz de unirse al epítopo en la conformación asociada a la forma inmunogénicamente activa de la vacuna y un segundo anticuerpo monoclonal 35 capaz de unirse al fragmento en la conformación asociada a la forma inmunogénicamente inactiva de la vacuna y medir la cantidad de primer anticuerpo monoclonal unido a la muestra de vacuna y la cantidad del segundo anticuerpo monoclonal unido a la muestra de vacuna. Preferentemente, el primer y segundo anticuerpos monoclonales están marcados cada uno con una primera y segunda sustancias detectables, respectivamente, antes de la exposición de la vacuna a ellos, y en los que la cantidad de primer anticuerpo monoclonal unido a la forma inmunogénicamente activa de 40 la vacuna y de segundo anticuerpo monoclonal unido a la forma inmunogénicamente inactiva de la vacuna se determinan midiendo la cantidad de primera y segunda sustancias detectables asociadas a la muestra de vacuna después de la exposición al primer y segundo anticuerpos monoclonales. De la forma más preferente, la primera y segunda sustancias detectables emiten luz fluorescente de diferentes longitudes de onda cuando están unidas a la forma inmunogénicamente activa de la vacuna y a la forma inmunogénicamente inactiva de la vacuna, respectivamente, 45 y en el que la medición de la cantidad de primer y segundo anticuerpos monoclonales unidos a la vacuna se realiza midiendo la luz fluorescente emitida por la primera y segunda sustancias detectables. Típicamente, la muestra de vacuna comprende material de vacuna y un adyuvante.
En una realización preferida, la muestra de vacuna se coloca en una placa filtrante antes de la exposición al primer y segundo anticuerpos monoclonales. La placa filtrante comprende dos o más pocillos, en los que la muestra de 50 vacuna se coloca en al menos un pocillo y adyuvante de control desprovisto de material de vacuna se coloca en al menos otro pocillo que no contiene el material de vacuna, y en los que los primer y segundo anticuerpos monoclonales marcados se añaden a los pocillos en la placa. Los pocillos que contienen la muestra de vacuna se lavan después de la adición del primer y segundo anticuerpos monoclonales para retirar de los pocillos que contienen la muestra de vacuna el anticuerpo monoclonal en exceso que no está unido al material de vacuna antes de medir la luz emitida por las 55 sustancias fluorescentes.
La presente invención es particularmente adecuada para su implementación en ensayos de inmunogenia dirigidos a vacuna del virus del papiloma, particularmente vacuna del virus del papiloma basadas en partículas similares a virus que comprenden la proteína L1, más particularmente HPV-16 y HPV-18.
60
Breve descripción de los dibujos
La figura 1 muestra datos del ensayo en placa filtrante de J4 que muestra el efecto del tratamiento con timerosal sobre los patrones de unión a anticuerpo monoclonal J4, R5 y 18A1. Las barras de error representan el error estándar de triplicados ensayados en el ensayo.
La figura 2 muestra datos del ensayo de J4 después de 10 días de tratamiento con timerosal a 37ºC que muestran 5 la dramática pérdida de unión al anticuerpo J4 en muestras tratadas con timerosal. Las barras de error representan el error estándar de triplicados realizados en el ensayo.
La figura 3 muestra resultados del ensayo en placa filtrante de J4 que ensaya MEDI-517 (lote L98H074) que no superó el ensayo de inmunogenia en el punto temporal de estabilidad acelerada de 8 meses. Dado que no se conservó material de control del mismo lote, se preparó un lote adicional de material a la misma concentración de 10 HPV-18 y se usó como control. Las barras de error representan el error estándar de triplicados realizados en el ensayo de J4.
La figura 4 muestra el efecto del organomercurial específico de tiol ácido p-cloromercurifenilsulfónico (PCMPS) sobre el epítopo de J4 del material de HPV-18 según se ensayó en el ensayo en placa filtrante de J4. Las barras de error representan el error estándar de triplicados realizados en el ensayo de J4. 15
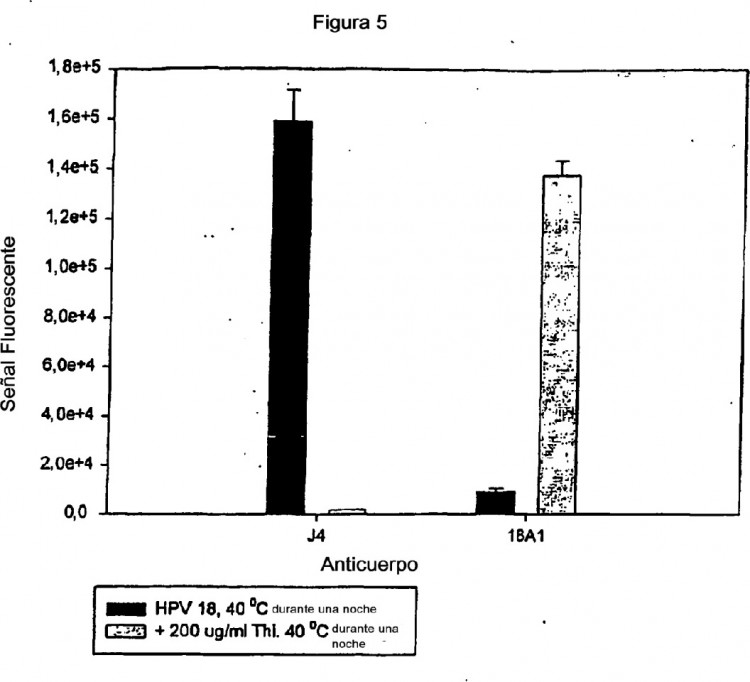
La figura 5 muestra el efecto del tratamiento con timerosal durante una noche sobre el epítopo de J4 a la elevada temperatura de 40ºC. La pérdida del epítopo de J4 se aceleraba en gran medida por encima del estado de almacenamiento a 37ºC, que requería casi 10 días para alcanzar el mismo nivel de pérdida. Las barras de error representan el error estándar de triplicados realizados en el ensayo de J4.
Descripción detallada de las realizaciones preferidas 20
La presente invención se basa en el descubrimiento de que la combinación de unión a Mab de epítopo conformacional y lineal puede ayudar a determinar el estado relativo de desnaturalización de una muestra de vacuna. La invención se basa además en el descubrimiento de la correlación de la unión al epítopo conformacional con inmunogenia y neutralización. En base a estos descubrimientos, se cree que los datos correlativos obtenidos junto con el desarrollo de la presente invención permitirán una ruta alternativa para inmunogenia de vacunas que eliminen o 25 reduzcan drásticamente la necesidad de ensayos en animales de inmunogenia asociados con métodos convencionales de desarrollo de vacunas y control de calidad.
El concepto inventivo de la presente solicitud es particularmente adecuado para su implementación usando anticuerpos monoclonales que se unen específicamente a un epítopo u otro fragmento de material de vacuna en diversos estados conformacionales que están directamente correlacionados con la actividad... [Seguir leyendo]
Reivindicaciones:
1. Un ensayo para medir la inmunogenia de una vacuna, en el que la vacuna comprende un epítopo que tiene una conformación asociada a una forma inmunogénicamente activa de la vacuna y un fragmento que tiene una conformación asociada a una forma inmunogénicamente inactiva de la vacuna, en el que el método comprende exponer a una muestra de la vacuna a un primer anticuerpo monoclonal capaz de unirse al epítopo en la conformación asociada 5 a la forma inmunogénicamente activa de la vacuna y a un segundo anticuerpo monoclonal capaz de unirse al fragmento en la conformación asociada a la forma inmunogénicamente inactiva de la vacuna y medir la cantidad de primer anticuerpo monoclonal unido a la muestra de vacuna y la cantidad del segundo anticuerpo monoclonal unido a la muestra de vacuna.
2. El ensayo de la reivindicación 1, en el que los primer y segundo anticuerpos monoclonales están, cada uno, 10 marcados con una primera y segunda sustancias detectables, respectivamente, antes de la exposición de la vacuna a ellos, y en el que la cantidad de primer anticuerpo monoclonal unido a la forma inmunogénicamente activa de la vacuna y de segundo anticuerpo monoclonal unido a la forma inmunogénicamente inactiva de la vacuna se determinan midiendo la cantidad de primera y segunda sustancias detectables asociadas a la muestra de vacuna después de la exposición al primer y segundo ligandos. 15
3. El ensayo de la reivindicación 2, en el que la primera y segunda sustancias detectables emiten luz fluorescente de diferentes longitudes de onda cuando están unidas a la forma inmunogénicamente activa de la vacuna y a la forma inmunogénicamente inactiva de la vacuna, respectivamente, y en el que la medición de la cantidad de primer y segundo anticuerpo monoclonal unido a la vacuna se realiza midiendo la luz fluorescente emitida por la primera y segunda sustancias detectables. 20
4. El ensayo de la reivindicación 3, en el que la muestra de vacuna comprende material de vacuna y un adyuvante.
5. El ensayo de la reivindicación 4, en el que la muestra de vacuna se coloca en una placa filtrante antes de la exposición al primer y segundo anticuerpos monoclonales.
6. El ensayo de la reivindicación 5, en el que la placa filtrante comprende dos o más pocillos, en el que la muestra 25 de vacuna se coloca en al menos un pocillo y el adyuvante de control desprovisto de material de vacuna se coloca en al menos otro pocillo que no contiene el material de vacuna, y en el que los primer y segundo anticuerpos monoclonales marcados se añaden a los pocillos en la placa.
7. El ensayo de la reivindicación 6, en el que los pocillos que contienen la muestra de vacuna se lavan después de la adición de los primer y segundo anticuerpos monoclonales para retirar de los pocillos que contienen la muestra de 30 vacuna el exceso de anticuerpo monoclonal que no está unido al material de vacuna antes de medir la luz emitida por las sustancias fluorescentes.
8. El ensayo de la reivindicación 1, en el que la vacuna es una vacuna del virus del papiloma.
9. El ensayo de la reivindicación 8, en el que la vacuna comprende una partícula similar a un virus.
10. El ensayo de la reivindicación 9, en el que la partícula similar a un virus comprende una proteína L1. 35
11. El ensayo de la reivindicación 9, en el que la partícula similar a un virus comprende HPV-16.
12. El ensayo de la reivindicación 11, en el que el epítopo que tiene una conformación asociada a una forma activa de la vacuna es epítopo de V5.
13. El ensayo de la reivindicación 12, en el que el anticuerpo monoclonal capaz de unirse al epítopo en una conformación asociada a la forma inmunogénicamente activa de la vacuna es el anticuerpo monoclonal HPV16.V5. 40
14. El ensayo de la reivindicación 13, en el que el HPV16.V5 está marcado con una sustancia fluorescente.
15. El ensayo de la reivindicación 11, en el que la forma inactiva de la vacuna comprende proteína L1 desnaturalizada.
16. El ensayo de la reivindicación 15, en el que la proteína L1 comprende proteína L1 lineal.
17. El ensayo de la reivindicación 9, en el que la partícula similar a un virus comprende HPV-18. 45
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]