ANTIBIÓTICO DE ANTRACICLINA CRISTALINO Y PROCEDIMIENTO PARA SU PRODUCCIÓN.
Una forma cristalina de un antibiótico de antraciclina representado por la siguiente fórmula (I) y que tiene al menos valores 2θ
característicos (en grados) de 6,18, 7,88, 9,82, 11,60, 13,30, 15,80, 20,88 y 23,12 medidos por el método de difracción de rayos X en polvo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP1998/005391.
Solicitante: MERCIAN CORPORATION.
Nacionalidad solicitante: Japón.
Dirección: 5-8, KYOBASHI 1-CHOME CHUO-KU, TOKYO 104-8305 JAPON.
Inventor/es: JOHDO, OSAMU, YOSHIOKA, TAKEO, NAKAMURA,Kiyotomo.
Fecha de Publicación: .
Fecha Solicitud PCT: 1 de Diciembre de 1998.
Clasificación Internacional de Patentes:
- C07H15/252D
Clasificación PCT:
- C07H15/252 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 15/00 Compuestos que contienen radicales hidrocarbonados o hidrocarbonados sustituidos, unidos directamente a los heteroátomos de los radicales sacárido. › Radicales naftaceno, p. ej. daunomicinas, adriamicinas.
Clasificación antigua:
- C07H15/252 C07H 15/00 […] › Radicales naftaceno, p. ej. daunomicinas, adriamicinas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2356284_T3.pdf
Fragmento de la descripción:
Campo técnico
Esta invención se refiere a nuevas formas cristalinas de un antibiótico de
antraciclina, particularmente daunomicina (también conocida como daunorubicina), y a
un procedimiento para producir las mismas.
Antecedentes de la técnica
Se sabe que la daunomicina (también conocida como daunorubicina; en lo
sucesivo abreviada como DM), que es un antibiótico de antraciclina representado por
la siguiente fórmula (I)
**(Ver fórmula)**
se obtiene a partir de un medio de cultivo de un actinomiceto, y tiene un amplio espectro anticanceroso contra tumores animales experimentales. De hecho, la DM está siendo ampliamente usada como agente quimioterapéutico para el cáncer en aplicaciones clínicas.
15 Sin embargo, la forma mayoritaria de DM (hidrocloruro de DM) disponible en la actualidad es un polvo amorfo o un sólido que está clasificado provisionalmente como cristalino pero tiene una alta higroscopicidad y una escasa estabilidad. Desde el punto de vista de la preparación de DM en medicinas, las propiedades físicas y químicas, no sólo de su polvo mayoritario final sino también de sus productos intermedios, tienen
20 una gran significación. Por ejemplo, la escasa estabilidad química requiere una gran precaución en el almacenamiento, y la alta higroscopicidad hace que su manejo sea difícil. Además, en consideración a su uso como fármaco, cualquier disolvente residual puede constituir un inconveniente fatal. Entre la técnica anterior, la patente europea EP 0 306 541 describe un procedimiento mejorado para la purificación de hidrocloruro de daunorubicina a partir de caldo de fermentación, caracterizado por el uso de una columna de sílice y una mezcla de cloroformo y metanol que contiene ácido fórmico.
Además, la patente británica GB 1 003 383 describe un laborioso procedimiento para la purificación de daunorubicina a partir de caldo de cultivo que incluye mezclar con un material absorbente, suspender en acetona, filtrar, seguido de varias etapas de extracción-concentración y recristalización.
La patente de EE.UU. 4.861.870 describe un procedimiento para purificar un glicósido de antraciclinona mediante la adsorción selectiva de una disolución acuosa ligeramente ácida de un glicósido impuro sobre al menos una resina y la posterior desabsorción del glicósido purificado por elución con agua ácida o una mezcla de agua y un disolvente polar.
Por consiguiente, un objeto de la presente invención es proporcionar un producto sólido de hidrocloruro de DM que tenga una excelente estabilidad química y, preferiblemente, que tenga además una baja higroscopicidad y un contenido de disolvente residual permisible. Descripción de la invención
Los presentes inventores hicieron repetidas investigaciones con la idea de solucionar los problemas descritos anteriormente, y han encontrado ahora que la cristalización de hidrocloruro de DM usando un cierto sistema disolvente produce una forma cristalina específica de hidrocloruro de DM que tiene una excelente estabilidad química y, en algunos casos, esta forma cristalina también tiene una baja higroscopi- cidad y puede solucionar el problema con el disolvente residual.
Por tanto, según la presente invención, se proporciona una forma cristalina de hidrocloruro de DM que tiene al menos valores 2θ característicos (en grados) de 6,18, 7,88, 9,82, 11,60, 13,30, 15,80, 20,88 y 23,12 medidos por el método de difracción de rayos X en polvo.
Según la presente invención, también se proporciona un procedimiento para producir la forma cristalina mencionada anteriormente de hidrocloruro de DM a partir de una disolución que contiene hidrocloruro de DM, comprendiendo el procedimiento las etapas de preparar la disolución mencionada anteriormente a partir de un polvo de hidrocloruro de daunomicina que tiene una pureza relativa mayor que 90% usando un sistema disolvente compuesto de un mal disolvente para el antibiótico y un buen disolvente que es miscible con el mal disolvente y capaz de disolver el antibiótico; y someter la disolución así preparada a un tratamiento de cristalización, en donde el mal disolvente contiene al menos 1-butanol y en donde el buen disolvente se selecciona entre agua, metanol, etanol y mezclas de dos o más de ellos.
Breve descripción del dibujo
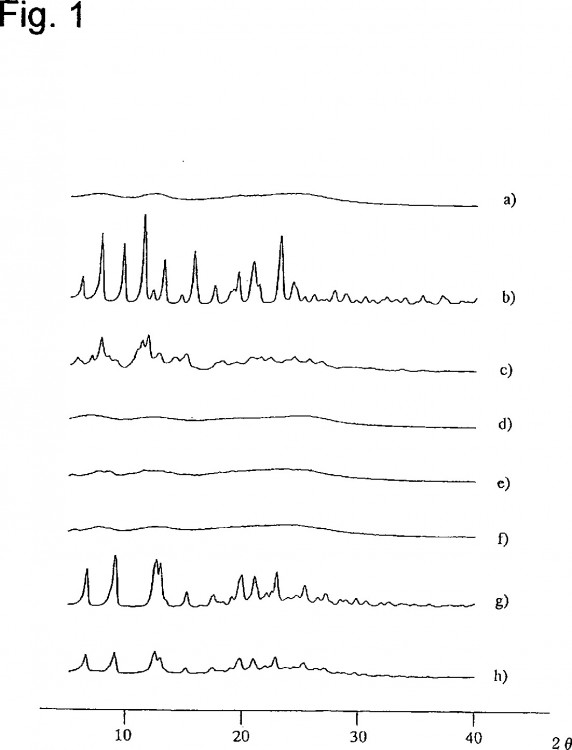
La FIG. 1 es un gráfico que muestra los resultados del análisis por difracción de rayos X en polvo de polvos de hidrocloruro de DM y diversas formas cristalinas de hidrocloruro de DM. En este gráfico, b) muestra el resultado del análisis por difracción de rayos X en polvo de una forma cristalina de hidrocloruro de DM de acuerdo con la presente invención; a), d), e) y f) muestran los resultados del análisis por difracción de rayos X en polvo de polvos de hidrocloruro de DM amorfos (polvos comparativos); y c), g) y h) muestran los resultados del análisis por difracción de rayos X en polvo de formas sólidas de hidrocloruro de DM que se consideran cristalinas pero no muestran las propiedades de la forma cristalina de acuerdo con la presente invención (formas cristalinas comparativas). Descripción específica de la invención
Específicamente, la forma cristalina de hidrocloruro de DM de acuerdo con la presente invención se caracteriza por tener al menos valores 2θ característicos (en grados) de 6,18, 7,88, 9,82, 11,60, 13,30, 15,80, 20,88 y 23,12 medidos por el método de difracción de rayos X en polvo (el método de Debye-Scherrer) [véase b) en la FIG. 1]. El término “forma cristalina”, tal como se emplea en la presente memoria, significa un único cristal o una masa de tales cristales, y los resultados mencionados anterior- mente de análisis por difracción de rayos X en polvo son los obtenidos de tales masas.
La forma cristalina de acuerdo con la presente invención se distingue claramente de los polvos amorfos [que corresponden a los mostrados como a), d), e) y f) en la FIG.1] y de las formas sólidas consideradas provisionalmente como cristalinas [que corresponden a las mostradas como c), g) y h) en la FIG. 1]. Además, como se describirá más tarde, la forma cristalina b) tiene unas propiedades excelentes desde los puntos de vista de la higroscopicidad, el disolvente residual y la estabilidad química.
De manera general, y no a modo de limitación, el procedimiento para producir la forma cristalina de acuerdo con la presente invención mencionada anteriormente comprende las etapas de preparar una disolución disolviendo un polvo de hidrocloruro de daunomicina que tiene una pureza relativa mayor que 90% en un disolvente capaz de disolver la DM; y cristalizar la DM añadiendo a la disolución un disolvente que es miscible con el disolvente mencionado anteriormente pero es un mal disolvente para la DM.
Es importante usar un disolvente que contenga al menos 1-butanol como el mal disolvente mencionado anteriormente. Los ejemplos típicos de tales disolventes incluyen 1-butanol solo y mezclas de disolventes compuestas de 1-butanol y otros disolventes orgánicos (p.ej., acetona, hexano y éter diisopropílico). Por otra parte, como el disolvente capaz de disolver la DM, se puede usar cualquier disolvente que pueda disolver la DM, sea miscible con el mal disolvente mencionado anteriormente, y sea adecuado por ello para el fin de la presente invención. Los ejemplos típicos de tales disolventes incluyen, pero no se limitan a, agua, metanol, etanol y mezclas de dos o más de ellos.
De acuerdo con una realización preferida, el procedimiento de producción de la presente invención comprende las etapas de preparar una disolución disolviendo un polvo de hidrocloruro de DM que tiene una pureza relativa mayor que 90% en metanol (por ejemplo, usando el polvo de hidrocloruro de DM y metanol en una relación de pesos de 1:5 a 1:20); y cristalizar la DM añadiendo 1-butanol o una mezcla de 1butanol y acetona, hexano o éter diisopropílico (por ejemplo, que contiene hasta 60% de acetona, hexano o éter diisopropílico) a la disolución mencionada anteriormente en una cantidad de aproximadamente 1 a 20 partes en volumen en base al metanol.
Cuando la expresión “1-butanol/acetona”, por ejemplo, se usa en relación con la presente invención, significa el uso combinado de 1-butanol y acetona. Por tanto, según la presente invención, el disolvente usado para disolver un polvo de hidrocloruro de DM puede comprender no solamente metanol solo, sino también una mezcla de metanol y 1-butanol o una... [Seguir leyendo]
Reivindicaciones:
1. Una forma cristalina de un antibiótico de antraciclina representado por la siguiente fórmula (I) y que tiene al menos valores 2θ característicos (en grados) de 6,18, 7,88, 9,82, 11,60, 13,30, 15,80, 20,88 y 23,12 medidos por el método de difracción de rayos X en polvo.
2. Un procedimiento para producir una forma cristalina de un antibiótico de antraciclina representado por la siguiente fórmula (I) y que tiene al menos valores 2θ característicos (en grados) de 6,18, 7,88, 9,82, 11,60, 13,30, 15,80, 20,88 y 23,12 medidos por el método de difracción de rayos X en polvo,
**(Ver fórmula)**
**(Ver fórmula)**
a partir de una disolución que contiene el antibiótico, comprendiendo el procedimiento las etapas de preparar dicha disolución a partir de un polvo de hidrocloruro de daunomicina que tiene una pureza relativa mayor que 90% usando un sistema disolvente compuesto de un mal disolvente para el antibiótico y un buen disolvente que es miscible con el mal disolvente y capaz de disolver el antibiótico; y someter la disolución así preparada a un tratamiento de cristalización, en donde el mal disolvente contiene al menos 1-butanol y en donde el buen disolvente se selecciona entre agua, metanol, etanol y mezclas de dos o más de ellos.
3. Un procedimiento de acuerdo con la reivindicación 2, en el que el mal disolvente se selecciona del grupo que consiste en 1-butanol, 1-butanol/acetona, 1-butanol/ hexano y 1-butanol/éter diisopropílico.
4. Un procedimiento de acuerdo con la reivindicación 2, que comprende las etapas de
5 disolver 1 parte en peso del antibiótico de fórmula (I) en 5 a 20 partes en peso de metanol, añadir 1-butanol o una mezcla de disolventes que comprende 1butanol/acetona, 1-butanol/hexano o 1-butanol/éter diisopropílico (en donde la acetona, el hexano o el éter diisopropílico pueden comprender hasta 60% en volumen de la mezcla de disolventes) a la disolución resultante en una cantidad de 1 a 20 partes en volumen en base al volumen de metanol, y cristalizar el antibiótico a una temperatura en el intervalo de 5 a 35ºC.
Patentes similares o relacionadas:
Método para producir epirrubicina e intermedio de producción novedoso para la misma, del 22 de Abril de 2020, de MEIJI SEIKA PHARMA Co., LTD: Un método de producir una sal de ácido orgánico de 4'-epidaunorrubicina o un hidrato o solvato de la misma, que comprende una etapa de mezclar 4'-epidaunorrubicina de […]
Brazos autorreactivos y profármacos que los comprenden, del 31 de Enero de 2018, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Compuesto de fórmula general (I): en la que: - X representa OH, NH2, NHOH o R'NH con R' pudiendo representar un radical alquilo en C1 a C10, lineal o […]
Derivados antibióticos de antraciclina con alta actividad, métodos de preparación y usos de los mismos, del 23 de Agosto de 2017, de TIANJIN HEMAY ONCOLOGY PHARMACEUTICAL CO., LTD: Compuesto representado por la fórmula (I), una sal o un solvato del mismo: **(Ver fórmula)** donde R1 representa H, hidrocarbilo C1-4 u Ohidrocarbilo […]
Derivados de antraquinona tetracíclica, del 19 de Abril de 2017, de TIANJIN HEMAY ONCOLOGY PHARMACEUTICAL CO., LTD: Un compuesto representado por la fórmula (I) y una sal farmacéuticamente aceptable del mismo,**Fórmula** en la que: R1 se selecciona entre el grupo que consiste […]
Monohidrato cristalino estable de clorhidrato de epirrubicina y método de producción, del 1 de Febrero de 2017, de Synbias Pharma AG: Método para producir un monohidrato cristalino de clorhidrato de epirrubicina, que comprende: (a) adicionar al menos un primer solvente y […]
Método para producir 4-desmetoxidaunorrubicina, del 6 de Enero de 2016, de Synbias Pharma AG: Un método para la producción de 4-desmetoxidaunorrubicina, o una sal de la misma, que tiene la estructura química de fórmula (I),**Fórmula** en la que An- representa […]
AGENTES COTOTOXICOS QUE COMPRENDEN DOXORRUBICINAS Y DAUNORRUBICINAS Y SU UTILIZACION TERAPEUTICA., del 1 de Junio de 2007, de IMMUNOGEN, INC.: Compuesto que comprende un grupo de enlace R o R' representado por la fórmula (I): en la que, X es H u OH; Y es O o NR2, en el que R2 es alquilo lineal o ramificado que tiene […]
PROCEDIMIENTO PARA LA SINTESIS DE TETRACICLINAS OPTICAMENTE ACTIVAS., del 16 de Marzo de 2007, de MENARINI RICERCHE S.P.A.: Procedimiento para la preparación de antraciclina de fórmula VIII: (Ver fórmula) en la que R1 = H, OH, OCH3, R2 = H, OH, R3 = X, Y o Z, en las que que comprende […]