ADMINISTRACIÓN Y PRODUCCIÓN CONTROLADAS DE AGENTES BIOLÓGICAMENTE ACTIVOS MEDIANTE BACTERIAS INTESTINALES.
Bacteria comensal intestinal de Bacteroides ovatus recombinante que comprende y expresa una proteína o un polipéptido biológicamente activo,
comprendiendo la bacteria un operón xilanasa que comprende un promotor de xilanasa de Bacteroides ovatus que dirige la expresión de una secuencia de ácido nucleico que codifica para la proteína o el polipéptido terapéutico heterólogo biológicamente activo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2006/000222.
Solicitante: PLANT BIOSCIENCE LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: John Innes Centre Norwich Research Park Colney LaneNorwichNorfolk NR 4 7UH.
Inventor/es: FARRAR, MARK, CARDING,SIMON.
Fecha de Publicación: .
Fecha Solicitud PCT: 24 de Enero de 2006.
Fecha Concesión Europea: 6 de Octubre de 2010.
Clasificación Internacional de Patentes:
- A61K35/74 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Bacterias (uso terapéutico de una proteína de la bacteria A61K 38/00).
Clasificación PCT:
- A61K35/74 A61K 35/00 […] › Bacterias (uso terapéutico de una proteína de la bacteria A61K 38/00).
- A61K38/17 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- C12N1/21 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › modificados por la introducción de material genético extraño.
- C12N15/74 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores o sistemas de expresión especialmente adaptados a huéspedes procariotas distintos a E. coli, p. ej. Lactobacillus, Micromonospora.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
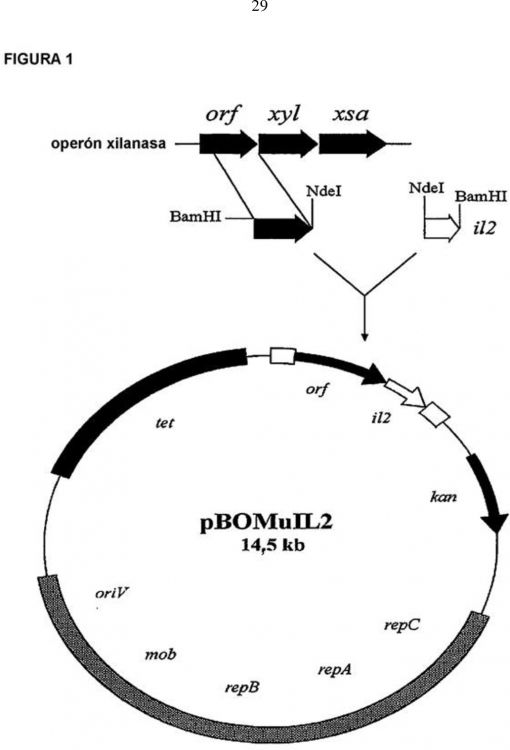
Fragmento de la descripción:
La presente invención se refiere a la producción y secreción de proteína(s) o polipéptido(s) biológicamente activo(s) por la microflora intestinal, a métodos de administración de los mismos y a métodos de control de la 5 producción y secreción de dicha(s) proteína(s) o polipéptido(s) biológicamente activo(s). La presente invención es particularmente útil en el desarrollo de nuevas inmunoterapias y especialmente para el tratamiento de enfermedades intestinales inflamatorias. 10
ANTECEDENTES
La comunidad microbiana en el intestino grueso humano consiste en una gama diversa de bacterias que son predominantemente anaerobios obligados. Estas bacterias actúan 15 juntas degradando sustratos de la dieta que alcanzan el colon (incluyendo insulina, fructo-oligosacáridos y almidón resistente), produciendo una gama de productos que son importantes para la enfermedad y la salud humana.
La respuesta inmunitaria de la mucosa puede verse 20 influida por la manipulación de la flora bacteriana residente normal. Esta flora posee una gran variedad de propiedades biológicas e inmunomoduladoras que pueden influir, directa o indirectamente, en el desarrollo y la función del sistema inmunitario de la mucosa. Trastornos crónicos del intestino, 25 por ejemplo la enfermedad inflamatoria del intestino (EII) que incluye los trastornos de la enfermedad de Crohn y la colitis ulcerosa, afectan a una proporción significativa de la población en países desarrollados. Se han usado modelos animales de inflamación de la mucosa para probar y determinar 30 los mecanismos inmunitarios implicados en la patogenia de estas enfermedades. La colitis ulcerosa se desarrolla de manera espontánea en ratones interleucina (IL) 2-/- e IL10-/- ambos de los cuales se usan como modelos de EII. Se han descrito también muchos otros modelos de ratón de EII, la 35
mayoría de los cuales tienen deleciones seleccionadas como diana de genes de respuesta inmunitaria. El tratamiento actual de EII se limita a terapias con fármacos antiinflamatorios e inmunosupresores incluyendo IL10 recombinante y anticuerpos frente al factor de necrosis tumoral- (TNF-). Sin embargo, 5 estas terapias no son curativas y pueden provocar efectos secundarios adversos tales como toxicidad e inmunosupresión. Por tanto, existe una necesidad de una forma de inmunoterapia más controlada y dirigida.
Se sabe de la técnica anterior usar bacterias 10 comensales, o bacterias que se producen de manera natural en el canal alimentario, tales como Lactobacillus spp. y Streptococcus spp. para tratar la inflamación intestinal y ciertas formas de EII en seres humanos (Shanahan 2001), sin embargo estos resultados tienen pruebas de éxito limitadas y 15 eficacia inconstante. Se sabe de la técnica anterior usar Lactococcus lactis de grado alimentario modificada por ingeniería genética para secretar interleucina-10 (IL10), que cuando se administra por vía intragástrica a dos modelos murinos de EII se demostró que era tan eficaz tanto en la 20 prevención como en el tratamiento de la enfermedad que la terapia con esteroides más convencional (Steidler et al. 2000). Este sistema de Lactococcus se ha usado también para producir IL2 e IL6 biológicamente activa (Steidler et al. 1995; Steidler et al. 1998). Sin embargo, una desventaja 25 importante asociada con estos sistemas de la técnica anterior es que L. lactis no puede colonizar el intestino debido a la incapacidad del organismo para unirse al epitelio del intestino y/o su dependencia nutricional de la provisión de aminoácidos y péptidos que no están disponibles in vivo. Por 30 consiguiente, cualquier terapia o tratamiento in vivo requeriría la dosificación repetida al sitio apropiado con el organismo modificado.
Otra desventaja y preocupación de bioseguridad del uso de esta bacteria aerobia particular es que podría sobrevivir 35
fuera del huésped/paciente durante un tiempo suficiente para transmitirse a otros.
Una desventaja aún adicional de los sistemas de la técnica anterior es que no hay ningún medio de controlar la expresión constitutiva de las moléculas de interleucina 5 inmunológicamente activas y estas moléculas activas por sí mismas, cuando se producen en exceso, pueden tener efectos adversos. Por consiguiente, los sistemas probióticos genéticamente modificados de la técnica anterior carecen de control y regulación de la actividad de las bacterias 10 probióticas tras su administración. Esto representa un problema de seguridad grave para la terapia en seres humanos.
Para abordar las deficiencias en la técnica anterior y para desarrollar adicionalmente bacterias comensales como sistemas de administración novedosos para moléculas 15 biológicamente activas, se han desarrollado organismos probióticos modificados por ingeniería genética en los que la producción de agentes inmunoterapéuticos por bacterias comensales in situ puede regularse y controlarse mediante factores de la dieta. 20
Es un objeto de la presente invención modificar por ingeniería genética una bacteria comensal intestinal de modo que produzca y secrete proteína(s) o polipéptido(s) biológicamente activo(s) de una manera regulada como base para inmunoterapias novedosas para trastornos intestinales 25 crónicos.
BREVE SUMARIO DE LA DESCRIPCIÓN
Según un primer aspecto de la invención, se proporciona una bacteria comensal intestinal de Bacteroides ovatus 30 recombinante que comprende y expresa una proteína o un polipéptido biológicamente activo, comprendiendo la bacteria un operón xilanasa que comprende un promotor de xilanasa de Bacteroides ovatus y una secuencia de ácido nucleico que
codifica para la proteína o el polipéptido terapéutico heterólogo biológicamente activo.
A lo largo de toda la descripción y las reivindicaciones de esta memoria descriptiva, las palabras “comprenden” y “contienen” y variaciones de las palabras, por ejemplo “que 5 comprende” y “comprende”, significan “incluyendo pero sin limitarse a”, y no pretenden excluir (ni excluyen) otros restos, aditivos, componentes, números enteros o etapas.
A lo largo de toda la descripción y las reivindicaciones de esta memoria descriptiva, el singular abarca el plural a 10 menos que el contexto requiera otra cosa. En particular, cuando se usa el artículo indefinido, debe entenderse que la memoria descriptiva contempla la pluralidad así como la singularidad, a menos que el contexto requiera otra cosa.
Debe entenderse que los rasgos distintivos, los números 15 enteros, las características, los compuestos, los restos o los grupos químicos descritos conjuntamente con un aspecto, realización o ejemplo particular de la invención pueden aplicarse a cualquier otro aspecto, realización o ejemplo descrito en el presente documento a menos que sea incompatible 20 con el mismo.
Un operón puede definirse como una unidad funcional que consiste en un promotor, un operador y varios genes estructurales. Un ejemplo es el operón xilanasa. Los genes estructurales codifican comúnmente para varias enzimas 25 funcionalmente relacionadas, y aunque se transcriben como un ARNm (policistrónico), cada uno tiene su sitio de iniciación de la traducción separado. En el operón típico, la región operadora actúa como elemento de control de la activación o desactivación de la síntesis de ARNm. El operón xilanasa se 30 activa en presencia de xilano.
Preferiblemente, el promotor es constitutivo y más preferiblemente es el promotor de xilanasa. Por tanto, se apreciará que la expresión de una o más proteínas o polipéptidos biológicamente activos se controla mediante la 35
presencia de xilano en la dieta. Por tanto, puede decirse que las bacterias comprenden un elemento regulador inducible por xilano.
Preferiblemente, el operón xilanasa de la bacteria comensal intestinal de Bacteroides ovatus incluye además una 5 secuencia señal de secreción de enterotoxina de Bacteroides fragilis.
El xilano es un polisacárido soluble en agua, gomoso, que se encuentra en paredes de células vegetales y que produce xilosa tras su hidrólisis. Por tanto, es un componente o 10 factor común de la dieta, por consiguiente la inclusión o exclusión del xilano en la dieta controla la expresión de la proteína o el polipéptido biológicamente activo. Por tanto, las bacterias modificadas de la presente invención proporcionan ventajosamente...
Reivindicaciones:
1. Bacteria comensal intestinal de Bacteroides ovatus recombinante que comprende y expresa una proteína o un polipéptido biológicamente activo, comprendiendo la bacteria un operón xilanasa que comprende un promotor de 5 xilanasa de Bacteroides ovatus que dirige la expresión de una secuencia de ácido nucleico que codifica para la proteína o el polipéptido terapéutico heterólogo biológicamente activo.
2. Bacteria según la reivindicación 1, en la que el operón 10 xilanasa incluye además una secuencia señal de secreción de enterotoxina de Bacteroides fragilis.
3. Bacteria según cualquier reivindicación anterior, en la que la proteína o el polipéptido biológicamente activo usado se deriva de fuentes o bien virales, o bien 15 procariotas o bien eucariotas.
4. Bacteria según cualquier reivindicación anterior, en la que la proteína o el polipéptido biológicamente activo se selecciona del grupo que comprende insulina, hormona del crecimiento, prolactina, calcitonina, hormona 20 luteinizante, hormona paratiroidea, somatostatina, hormona estimulante del tiroides, vacunas, antígenos, polipéptido intestinal vasoactivo, factores trébol, factores de reparación celulares y tisulares, factor de crecimiento transformante , factor de crecimiento de 25 queratinocitos, una citocina de grupo estructural 1 que adopta un haz de 4 hélices antiparalelas seleccionada del grupo que comprende IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-9, IL-10, IL-11, IL-12, IL-13, GM-CSF, M-CSF, SCF, IFN-, EPO, G-CSF, LIF, OSM, CNTF, GH, PRL o 30 IFN/, una citocina de grupo estructural 2 seleccionada del grupo que comprende TNF, TNF, ligandos de CD40, CD27 o FAS, familia IL-1 de citocinas, familia del factor de crecimiento de fibroblastos, factores de
crecimiento derivados de las plaquetas, factor de crecimiento transformante y factores de crecimiento nerviosos, una citocina de grupo estructural 3, familia de citocinas del factor de crecimiento epidérmico, quimiocinas, citocinas relacionadas con la insulina, y 5 una citocina de grupo estructural 4 seleccionada del grupo que comprende EGF, dominios kringle y de tipo inmunoglobulina.
5. Bacteria según la reivindicación 4, en la que la proteína o el polipéptido biológicamente activo es un 10 receptor o antagonista para proteínas o polipéptidos biológicamente activos enumerados en la reivindicación 4.
6. Bacteria según cualquier reivindicación anterior modificada para expresar una pluralidad de proteínas o 15 polipéptidos biológicamente activos.
7. Composición farmacéutica que comprende una bacteria comensal intestinal de Bacteroides ovatus recombinante según cualquier reivindicación anterior.
8. Composición farmacéutica según la reivindicación 7, que 20 comprende un vehículo, diluyente o excipiente fisiológicamente aceptable.
9. Bacteria comensal intestinal de Bacteroides ovatus recombinante según una cualquiera de las reivindicaciones 1 a 3 ó 6, para su uso en el 25 tratamiento de una enfermedad intestinal inflamatoria, en la que el polipéptido o la proteína se selecciona del grupo que comprende una hormona del crecimiento, un factor trébol, factor de crecimiento transformante , factor de crecimiento de queratinocitos, IL-2, IL-4, 30 IL-5, IL-6, IL-7, IL-10, IL-11, IL-12, IL-13, GM-CSF, G-CSF, GM-CSF, IFN-, TNF, TNF, un miembro de la familia IL-1 de citocinas, un miembro de la familia de
citocinas del factor de crecimiento epidérmico, o una quimiocina.
Patentes similares o relacionadas:
Cepa de Faecaslibacterium Prausnitzii CNCM I-4573 para el tratamiento y la prevención de una inflamación gastrointestinal, del 15 de Julio de 2020, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Cepa bacteriana de la especie Faecalibacterium prausnitzii depositada en la CNCM bajo el número de acceso CNCM I-4573, para su utilización en el tratamiento y/o la prevención […]
Composiciones que comprenden cepas bacterianas, del 15 de Julio de 2020, de 4D Pharma Research Limited: Una composición que comprende una cepa bacteriana de la especie Eubacterium contortum, en donde la composición no contiene ninguna otra cepa o especie […]
BACTERIA DE HOLDEMANELLA SP. Y USO DE LA MISMA, del 2 de Julio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a la cepa de Holdemanella biformis la cepa H. biformis CECT 9752 a sus componentes celulares, metabolitos, […]
Bacteria de Holdemanella sp. y uso de la misma, del 26 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Bacteria de Holdemanella sp. y uso de la misma. La presente invención se refiere a la cepa de Holdemanella biformis la cepa H. biformis CECT 9752 a […]
COMPOSICIONES HOMEOPÁTICAS A BASE DE VIBRIO PARAHAEMOLYTICUS Y VIBRIO ALGINOLYTICUS Y SU USO COMO INMUNOESTIMULANTES EN EL CULTIVO DE ESPECIES ACUÁTICAS, del 25 de Junio de 2020, de CENTRO DE INVESTIGACIONES BIOLOGICAS DEL NOROESTE, S.C: La presente invención se refiere a composiciones homeopáticas a base de Vibrio parahaemolyticus y Vibrio Alginolyticus para uso inmunoestimulante en acuicultura, […]
Preparación de aceite microbiano que contiene ácidos grasos poliinsaturados, del 10 de Junio de 2020, de DSM IP ASSETS B.V.: Un aceite microbiano que comprende al menos el 50% de ácido araquidónico (ARA) basado en el aceite y que tiene un contenido en triglicéridos de al menos el 90%.
Procedimientos para el tratamiento dietético del síndrome del intestino irritable y la malabsorción de carbohidratos, del 3 de Junio de 2020, de GANEDEN BIOTECH, INC.: Uso de esporas de Bacillus coagulans Hammer en la fabricación de un medicamento para reducir los síntomas del síndrome del intestino irritable (SII) […]
Composiciones farmacéuticas y alimenticias basadas en Hafnia alvei para inducir saciedad y prolongar la saciedad, del 27 de Mayo de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un método cosmético no terapéutico para inducir saciedad en un sujeto que lo necesita que comprende administrar oralmente al sujeto una cantidad […]