PROCESO PARA LA FABRICACION DE ACETATO DE ALFA-TOCOFERILO.
Un proceso para la fabricación de acetato de α-tocoferilo o que comprende hacer reaccionar 2,
3,6-trimetilhidroquinona-1-acetato con un compuesto seleccionado del grupo conformado por fitol (fórmula IV con R = OH), isofitol (fórmula III con R = OH) y derivados de isofitol representados por las siguientes fórmulas III y IV con R = C2-5-alcanoiloxi, benzoiloxi, mesiloxi bencenosulfoniloxi o tosiloxi, en presencia de un catalizador de fórmula Mn+(R1SO3-)n, donde Mn+ es un catión metálico de plata, cobre, galio, hafnio o de tierras raras, n es la valencia del catión Mn+ y R1 es flúor, C1-8alquilo perfluorado o arilo perfluorado, y, si se requiere, ciclar 3-fitil-2,5,6-trimetilhidroquinona-1-acetato o un isómero de doble enlace obtenido a partir de este como producto intermedio de la reacción para obtener acetato de α-tocoferilo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2003/014723.
Solicitante: DSM IP ASSETS B.V..
Nacionalidad solicitante: Países Bajos.
Dirección: HET OVERLOON 1, 6411 TE HEERLEN.
Inventor/es: BONRATH, WERNER, NETSCHER, THOMAS, GIRAUDI,LISA, DITTEL,CLAUS, PABST,THOMAS.
Fecha de Publicación: .
Fecha Concesión Europea: 21 de Julio de 2010.
Clasificación Internacional de Patentes:
- C07D311/72 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 311/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que contienen un átomo de oxígeno como único heteroátomo, condensados con otros ciclos. › Derivados del 3,4-dihidro que tienen en la posición 2 al menos un radical metilo y en la posición 6 un átomo de oxígeno, p. ej. tocoferoles.
Clasificación PCT:
- C07D311/72 C07D 311/00 […] › Derivados del 3,4-dihidro que tienen en la posición 2 al menos un radical metilo y en la posición 6 un átomo de oxígeno, p. ej. tocoferoles.
Clasificación antigua:
- C07D311/72 C07D 311/00 […] › Derivados del 3,4-dihidro que tienen en la posición 2 al menos un radical metilo y en la posición 6 un átomo de oxígeno, p. ej. tocoferoles.
Fragmento de la descripción:
Proceso para la fabricación de acetato de α-tocoferilo.
La presente invención se refiere a un proceso nuevo para la fabricación de acetato de α-tocoferilo.
Las síntesis industriales de la vitamina E, α-tocoferol, están basadas en la reacción de 2,3,5-trimetildroquinona (TMHQ) con (iso)fitol o haluros de fitilo, véase, p. ej., Ullmann's Encyclopedia of Industrial Chemistry Vol. A27, VCH (1996), págs. 478-488. La TMHQ se puede obtener a partir de cetoisoforona vía el diacetato de 2,3,5-trimetilhidroquinona, p. ej., como se describe en EP-A 0 850 910, EP-A 0 916 642, EP-A 0 952 137 o EP-A 1 028 103, y la saponificación de este último.
EP-A 0 658 552 también presenta un proceso para la fabricación de α-tocoferol y derivados de este, donde se emplean fluorosulfonatos [M(RSO3)3], nitratos [M(NO3)3] y sulfatos [M2(SO4)3] como catalizadores, donde M representa un átomo de Sc, Y o lantánido, y R representa flúor, un grupo alquilo inferior fluorado o un grupo arilo que puede estar sustituido por uno o más átomos de flúor. La reacción se lleva a cabo en un disolvente que es inerte al catalizador y a los materiales de partida, a derivados de TMHQ y de alcohol alílico o alcoholes cenílicos, como fitol o isofitol, siendo ejemplos del disolvente los hidrocarburos alifáticos, hidrocarburos aromáticos y ésteres alifáticos. Preferentemente, se emplean derivados de alcohol alílico o alcoholes alquenílicos en un exceso molar de un 4% o un 10% en comparación con TMHQ.
Debido a que el α-tocoferol es lábil en condiciones oxidantes, se suele convertir en su acetato que es más estable y más fácil de manipular. Así pues, la fabricación de la forma comercial habitual de la vitamina E, es decir, acetato de α-tocoferilo, implica el paso adicional de esterificación del α-tocoferol (como se obtiene de la reacción de TMHQ con (iso)fitol o haluros de fitilo).
Un ejemplo de esto último es el proceso descrito en DE-OS 2 160 103, en el que se hace reaccionar (iso)fitol o un haluro de fitilo con TMHQ o 2,3,6-trimetilhidroquinona-1-acetato en presencia de hierro o cloruro ferroso y cloruro de hidrógeno. En todos los casos se obtiene α-tocoferol el cual se debe convertir en su acetato en otro paso. Lo mismo se aplica cuando se emplean catalizadores ácidos sólidos como los que se presentan en DE-OS 24 04 621. Incluso si se emplea 2,3,6-trimetilhidroquinon-1,4-diacetato como material de partida, como en el proceso conforme a DE-A 100 11 402, se obtiene α-tocoferol en una cantidad significativa, de forma que se requiere una acetilación parcial adicional, ya que el α-tocoferol y el acetato de α-tocoferol no se pueden separar fácilmente por destilación.
Schneider et al., Applied Catalysis A: General, vol. 220, p.51-58 (2001) presenta un método para sintetizar α-tocoferol a partir de trimetilhidroquinon-diacetato, -1-monoacetato o trimetilhidroquinona con la adición de isofitol por catálisis con Nafion.
WO 96/19288 presenta un catalizador de Nafion alternativo retenido en un óxido metálico poroso y estos óxidos metálicos pueden comprender compuestos de óxidos metálicos o semimetálicos, tales como p. ej., óxidos de itrio o cobre. Sin embargo, no incluye la fabricación de acetato de α-tocoferol de la presente invención.
Inoue et al., J. Organ. Chem., vol. 52, p. 5495-5497 (1987) presenta la producción de ésteres de α-tocoferol en la que el mono- o diéster de una hidroquinona se hace reaccionar con un derivado de alcohol alílico o un alcohol alílico, es decir, fitoles, en presencia de haluros de cinc y ácidos que liberan protones.
Por lo tanto, el objeto de la presente invención es proporcionar un proceso para la fabricación de acetato de α-tocoferol partiendo de 2,3,6-trimetilhidroquinon-1-acetato en presencia de un catalizador, en el que se evita un paso adicional de acetilación.
El objeto es conseguir un nuevo enfoque para la fabricación de acetato de α-tocoferol (TCPA). De acuerdo con este enfoque, se hace reaccionar 2,3,6-trimetilhidroquinon-1-acetato (TMHQA) con fitol (PH), isofitol (IP) o un derivado de (iso)fitol para obtener TCPA o 3-fitil-2,5,6-trimetilhidroquinon-1-acetato (PTMHQA), momento en el que este último se somete al cierre del anillo para obtener TCPA.
Así pues, en un primer aspecto, la presente invención se refiere a un proceso que comprende hacer reaccionar TMHQA representado por la fórmula II
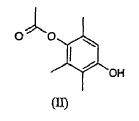
con un compuesto seleccionado del grupo conformado por fitol (fórmula IV, con R = OH), isofitol (fórmula III, con R = OH) y derivados de (iso)fitol representados por las siguientes fórmulas III y IV con R = C2-5alcanoiloxi, benzoiloxi, metanosulfoniloxi (= mesiloxi), bencenosulfoniloxi o toluenosulfoniloxi (=tosiloxi), preferentemente seleccionados del grupo conformado por fitol, isofitol y derivados de (iso)fitol representados por las siguientes fórmulas III y IV con R = acetiloxi o benzoiloxi, más preferentemente seleccionados del grupo conformado por fitol e isofitol, más preferentemente con isofitol,
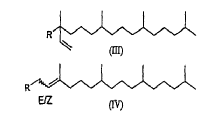
en presencia de un catalizador de fórmula Mn+(R1SO3-)n, donde Mn+ es un catión metálico de plata, cobre, galio, hafnio o de tierras raras, n es la valencia del catión Mn+ y R1 es flúor, C1-8alquilo perfluorado o arilo perfluorado, para obtener acetato de α-tocoferol representado mediante la siguiente fórmula I.
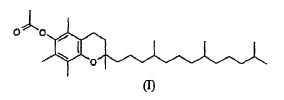
En otro aspecto, la invención se refiere a un proceso que comprende hacer reaccionar TMHQA con un compuesto seleccionado del grupo conformado por fitol, isofitol y derivados de (iso)fitol representados por las fórmulas III y IV, como se definieron anteriormente con las mismas preferencias, en presencia de un catalizador de fórmula Mn+(R1SO3-)n, donde Mn+, n y R1 son como los definidos anteriormente, para obtener 3-fitil-2,5,6-trimetilhidroquinon-1-acetato representado por la fórmula V
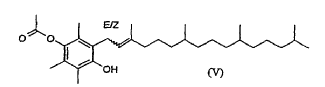
y/o un isómero de doble enlace de este y ciclar el 3-fitil-2,5,6-trimetilhidroquinon-1-acetato y/o un isómero de doble enlace de este (como se explica a continuación) obtenido para producir acetato de α-tocoferol.
En lo referente al sustituyente R: el término "C2-5alcanoiloxi" contempla C2-5alcanoiloxi lineal y C4-5alcanoiloxi ramificado. Los ejemplos preferidos de "C2-5alcanoiloxi" son acetiloxi, propioniloxi y pivaloiloxi.
En lo referente al catión metálico Mn+: los ejemplos de tierras raras que pueden estar presentes en el catalizador para emplear en la presente invención son Sc3+, Y3+, Lu3+, La3+, Ho3+, Tm3+, Gd3+ y Yb3+. Los cationes preferidos son Ag+, Cu+, Ga3+, Sc3+, Lu3+, Ho3+, Tm3+, Yb3+ y Hf4+, son especialmente preferidos Ag+, Ga3+, Sc3+ y Hf4+.
En lo referente al sustituyente R1: el término "C1-8perfluoroalquilo" incluye C1-8perfluoroalquilo lineal y C3-8per- fluoroalquilo ramificado. Preferentemente, C1-8perfluoroalquilo es trifluorometilo, pentafluoroetilo o nonafluoro-n-butilo, más preferentemente trifluorometilo o nonafluoro-n-butilo y más preferentemente trifluorometilo.
Un ejemplo preferido para "perfluoroarilo" es perfluorofenilo, que puede estar mono o multisustituido con trifluorometilo. Un perfluoroarilo más preferido es perfluorofenilo.
El catalizador de la fórmula Mn+(R1SO3-)n se puede obtener p. ej. conforme a los procedimientos descritos en US 3.615.169 o en el Journal...
Reivindicaciones:
1. Un proceso para la fabricación de acetato de α-tocoferilo o que comprende hacer reaccionar 2,3,6-trimetilhidroquinona-1-acetato con un compuesto seleccionado del grupo conformado por fitol (fórmula IV con R = OH), isofitol (fórmula III con R = OH) y derivados de isofitol representados por las siguientes fórmulas III y IV con R = C2-5-alcanoiloxi, benzoiloxi, mesiloxi bencenosulfoniloxi o tosiloxi,
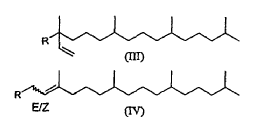
en presencia de un catalizador de fórmula Mn+(R1SO3-)n, donde Mn+ es un catión metálico de plata, cobre, galio, hafnio o de tierras raras, n es la valencia del catión Mn+ y R1 es flúor, C1-8alquilo perfluorado o arilo perfluorado, y, si se requiere, ciclar 3-fitil-2,5,6-trimetilhidroquinona-1-acetato o un isómero de doble enlace obtenido a partir de este como producto intermedio de la reacción para obtener acetato de α-tocoferilo.
2. El proceso según la reivindicación 1, en el que el Mn+ del catalizador es Ag+, Cu+, Ga3+, Sc3+, Lu3+, Ho3+, Tm3+, Yb3+ o Hf4+.
3. El proceso según la reivindicación 1, en el que el Mn+ del catalizador es Ag+, Ga3+, Sc3+ o Hf4+.
4. El proceso según cualquiera de las reivindicaciones 1 a 3, en el que el R1 del catalizador es trifluorometilo.
5. El proceso según cualquiera de las reivindicaciones 1 a 4, en el que el catalizador se emplea en una cantidad relativa de aproximadamente 0.001% mol a aproximadamente 1% mol, en función de 2,3,6-trimetilhidroquinona-1-acetato o un compuesto representado por la fórmula III o IV, dependiendo de cuál se emplee en menor cantidad molar.
6. El proceso según cualquiera de las reivindicaciones 1 a 5, en el que se hace reaccionar 2,3,6-trimetilhidroquinona-1-acetato con fitol y/o isofitol, preferentemente con fitol, y, si se requiere, se cicla 3-fitil-2,5,6-trimetilhidroquinona-1-acetato o un isómero de doble enlace de este obtenido como producto intermedio de la reacción para obtener acetato de α-tocoferilo.
7. El proceso según cualquiera de las reivindicaciones 1 a 6, en el que el proceso se lleva a cabo en un disolvente orgánico aprótico apolar o polar.
8. El proceso según cualquiera de las reivindicaciones 1 a 6, en el que el proceso se lleva a cabo en un sistema de disolventes bifásico que consta de un disolvente polar y un disolvente apolar.
9. El proceso según la reivindicación 8, en el que el disolvente polar se selecciona del grupo conformado por carbonatos alifáticos y cíclicos, ésteres alifáticos y ésteres cíclicos, cetonas cíclicas y alifáticas, y mezclas de estos, y el disolvente apolar se selecciona del grupo conformado por hidrocarburos alifáticos e hidrocarburos aromáticos.
10. El proceso según la reivindicación 9, en el que el disolvente polar es al menos un carbonato cíclico y el disolvente apolar es al menos un alcano de C5 a C15 lineal, ramificado o cíclico.
11. El proceso según la reivindicación 10, en el que el disolvente polar es carbonato de etileno o carbonato de propileno o una mezcla de estos, preferentemente carbonato de etileno, y el disolvente apolar es hexano, heptano, octano, ciclohexano o metilciclohexano o una mezcla de estos, preferentemente heptano.
12. El proceso según las reivindicaciones 7 a 11, en el que se emplean de aproximadamente 0.25 ml a aproximadamente 6 ml, preferentemente de aproximadamente 0.5 ml a aproximadamente 3 ml, de un disolvente orgánico por mmol del compuesto representado por la fórmula III o IV, dependiendo de cuál se emplee, representado estas cantidades la cantidad total de disolvente, es decir, independientemente de que la reacción se lleve a cabo en una única fase (un disolvente orgánico apolar o un disolvente orgánico polar) o en un sistema de disolventes bifásico (un disolvente orgánico apolar o un disolvente orgánico polar).
13. El proceso según cualquiera de las reivindicaciones 8 a 11, en el que el cociente de volumen del disolvente apolar respecto al disolvente polar en el sistema de disolventes bifásico entra en el rango de aproximadamente 1 : 5 a aproximadamente 30 : 1, preferentemente de aproximadamente 1 : 3 a aproximadamente 20 : 1, especialmente de aproximadamente 10 : 1 a aproximadamente 15 : 1.
14. El proceso de cualquiera de las reivindicaciones 1 a 13, en el que el cociente molar de 2,3,6-trimetilhidroquinona-1-acetato respecto al compuesto representado por la fórmula III o IV presente en la mezcla de reacción es de aproximadamente 3 : 1 a aproximadamente 0.8 : 1, preferentemente de aproximadamente 2 : 1 a aproximadamente 1 : 1, más preferentemente de aproximadamente 1.75 : 1 a aproximadamente 1 : 1.
15. El proceso según cualquiera de las reivindicaciones 1 a 14, en el que la reacción se lleva a cabo a temperaturas de aproximadamente 20ºC a aproximadamente 160ºC, preferentemente de aproximadamente 80ºC a aproximadamente 150ºC, especialmente de aproximadamente 105ºC a aproximadamente 150ºC, más preferentemente de aproximadamente 125ºC a aproximadamente 145ºC.
16. El proceso según la reivindicación 1, en el que se hace reaccionar 2,3,6-trimetilhidroquinona-1-acetato con isofitol o fitol en presencia de un catalizador de fórmula Mn+(R1SO3-)n, donde Mn+ es un catión metálico de plata, cobre, galio, hafnio o de tierras raras, n es la valencia del catión Mn+ y R1 es flúor, C1-8alquilo perfluorado o arilo perfluorado, en un disolvente orgánico aprótico, y, si se requiere, se cicla 3-fitil-2,5,6-trimetilhidroquinona-1-acetato o un isómero de doble enlace de este obtenido como producto intermedio de la reacción para obtener acetato de α-tocoferilo.
Patentes similares o relacionadas:
Formas salinas de Alfa-TEA: composiciones y usos para tratar enfermedades, del 23 de Octubre de 2019, de RESEARCH DEVELOPMENT FOUNDATION: Un compuesto de la fórmula:**Fórmula** en la que X1+ es:**Fórmula** o**Fórmula** o un hidrato del mismo.
BENZOPIRANOS PRENILADOS AGONISTAS DE PPAR, del 4 de Julio de 2019, de UNIVERSITAT DE VALENCIA: La presente invención describe compuestos de fórmula I que comprenden una estructura central de benzopirano prenilado. Formula (I) Dichos compuestos […]
BENZOPIRANOS PRENILADOS AGONISTAS DE PPAR, del 26 de Junio de 2019, de UNIVERSITAT DE VALENCIA: Benzopiranos prenilados agonistas de PPAR. La presente invención describe compuestos de fórmula I que comprenden una estructura central de benzopirano […]
Utilización de por lo menos un co-producto de la industria del refinado de aceites vegetales para obtener un insaponificable total purificado de aceite vegetal, del 16 de Enero de 2019, de LABORATOIRES EXPANSCIENCE: Utilización de por lo menos un co-producto de la industria del refinado de aceites vegetales, tal como un destilado de desodorización de aceites vegetales y/o […]
Procedimiento para la obtención de fitosteroles y/o tocoferoles a partir de los residuos de una destilación de ésteres de aceites vegetales, de manera preferida a partir de los residuos de destilación procedentes de una transesterificación de aceites vegetales, del 16 de Agosto de 2017, de Verbio Vereinigte Bioenergie AG: Un procedimiento para la obtención de fitosteroles y/o tocoferoles a partir de los residuos de una destilación de ésteres de aceites vegetales, […]
Proceso para la producción de ácido 4-alcanoiloxi-2-metilbutanoico, del 9 de Agosto de 2017, de DSM IP ASSETS B.V.: Un proceso de producción de un compuesto de fórmula (I) **(Ver fórmula)** en la que R significa un resto alquilo C1-C15 o un resto alquenilo C2-C18, en el que un […]
Tocoferoles con estabilidad cromática incrementada, del 21 de Septiembre de 2016, de DSM IP ASSETS B.V.: Método para preparar tocoferol de fórmula (I) con una estabilidad cromática incrementada, que comprende la etapa de poner en contacto el tocoferol de […]
Tocoferoles con un contenido reducido de impurezas fenólicas, del 10 de Agosto de 2016, de DSM IP ASSETS B.V.: Un método de preparar un tocoferol o tocoferol protegido de fórmula (I) con un contenido reducido del compuesto fenólico o compuesto fenólico protegido […]