PROCEDIMIENTOs PARA PREVENIR Y TRATAR LA ENFERMEDAD DE ALZEHIMER (AD).
Utilización de un compuesto, constituido por
- un péptido de 5 a 15 aminoácidos que incluye una secuencia aminoácida,
seleccionada de entre el grupo constituido por DKELRI, DWELRI, YAEFRG, EAEFRG, DYEFRG, DRELRI, GREFRN, EYEFRG, DWEFRDA, SWEFRT y DKELR, conteniendo dicho péptido un residuo adicional de cisteína en el extremo C y
- un soporte proteico acoplado mediante dicho residuo de cisteína a dicho péptido,
para la preparación de una vacuna destinada a la enfermedad de Alzheimer (AD)
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/000162.
Solicitante: AFFIRIS AG.
Nacionalidad solicitante: Austria.
Dirección: KARL-FARKAS-GASSE 22,1030 WIEN.
Inventor/es: MATTNER, FRANK.
Fecha de Publicación: .
Fecha Concesión Europea: 24 de Febrero de 2010.
Clasificación Internacional de Patentes:
- A61K38/08 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 5 a 11 aminoácidos.
- A61K38/10 A61K 38/00 […] › Péptidos que tienen de 12 a 20 aminoácidos.
- A61K38/17A2
- C07K14/47A3
- C07K7/06A
Clasificación PCT:
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
Clasificación antigua:
- C07K14/47 C07K 14/00 […] › de mamíferos.
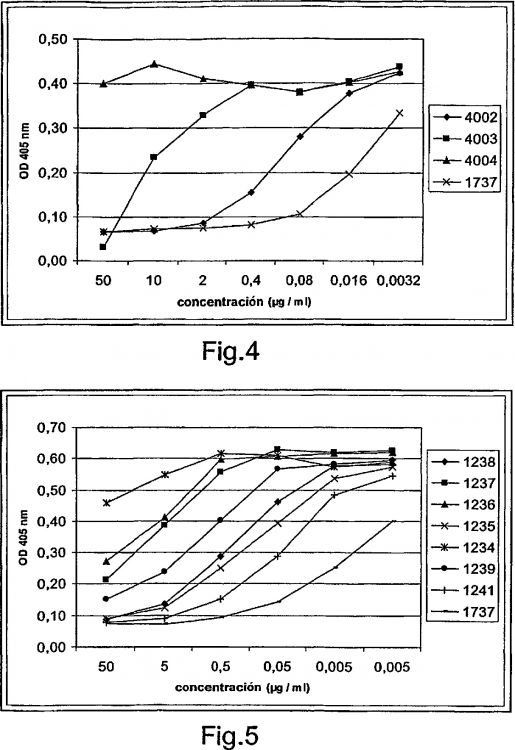
Fragmento de la descripción:
Procedimientos para prevenir y tratar la enfermedad de Alzheimer (AD).
La presente invención se refiere a procedimientos para prevenir y tratar la enfermedad de Alzheimer (AD).
El péptido amiloide-ß (Aß) juega un papel central en la neuropatología de la enfermedad de Alzheimer (AD) (Roher et al, 1993: "ß-amyloid-(1-42) is a major component of cerebrovascular amyloid deposits: Implications for the pathology of Alzheimer disease", PNAS 90:10836). Las formas familiares de la enfermedad se han relacionado con mutaciones en la proteína precursora amiloide (APP) y en los genes de la presenilina. Las mutaciones relacionadas con la enfermedad en estos genes dan lugar al aumento en la producción de la forma de 42 aminoácidos del péptido (Aß42), que es la forma predominante que se encuentra en las placas amiloides de la enfermedad de Alzheimer. Está disponible comercialmente un modelo animal para la enfermedad. El ratón transgénico PDAPP, que sobre-expresa la APP humana mutante (en la cual el aminoácido se encuentra en la posición 717 es F en vez de V), desarrolla progresivamente muchas de las características neuropatológicas de la enfermedad de Alzheimer en una forma cerebral dependiente y que depende también de la edad (Games et al., 1995: "Alzheimer-type neuropathology in transgenic mice overexpressing V717F ß-amyioid precursor protein", V717F, Nature 373:523).
Ya se han realizado estudios de vacunación con una vacuna "normal", no mimotópica. Se inmunizaron animales transgénicos con la Aß42 agregada, antes del inicio de las neuropatologías de tipo AD (6 semanas) o a una edad más avanzada (11 meses): la inmunización de animales jóvenes previno el desarrollo de la formación de las placas, de la distrofia neurítica y de la astrogliosis. El tratamiento de los animales viejos disminuyó de forma importante las neuropatologías de tipo AD. El enfoque de la vacunación experimental indujo el desarrollo de anticuerpos contra Aß42 capaces de atravesar la barrera hematoencefálica y de atacar las placas amiloides (Schenk et al, 1999: "Immunization with amyloid-ß-attenuates Alzheimer-disease-like pathology in the PDAPP mouse", Nature 400:173). Las placas son eliminadas posteriormente mediante diversos mecanismos, que incluyen la fagocitosis mediada por el receptor Fc (Bard et al 2000: "Peripherally administered antibodies against amyloid ß-peptides enter the central nervous system and reduce pathology in a mouse model of Alzheimer disease", Nature Med 6:916). Esta vacuna pudo asimismo retrasar los déficits de memoria (Janus et al, 2000: "Aß peptide immunization reduces behavioural impairment and plaques in a model of Alzheimer's disease", Nature 408:979).
Desde finales del año 1999, se han realizado estudios clínicos muy prometedores para AD. Se cree que la inmunización moviliza el sistema inmune para atacar las placas y limpia estos depósitos del cerebro humano afectado, aunque el mecanismo preciso que subyace necesita caracterizarse más detalladamente.
Estos ensayos clínicos se realizaron por la compañía farmacéutica Elan conjuntamente con su socio corporativo, American Home Products (vacuna terapéutica AN-1792, QS21 como adyuvante). Los ensayos clínicos de Fase I finalizaron con éxito en 2000. Los ensayos clínicos de Fase II comenzaron al final del 2001 para ensayar la eficacia en un conjunto de pacientes con una AD de media a moderada.
Ahora, estos ensayos clínicos de Fase II, se han discontinuado permanentemente debido a la neuroinflamación en diversos pacientes (Editorial 2002 "Insoluble problem?" Nature Med 8:191). Los síntomas incluían meningoencefalitis aséptica, que llevaron a la detención inmediata de estos ensayos clínicos por todo el mundo. En el peor caso, los pacientes afectados mostrarán haber expresado una respuesta inmune: un riesgo inherente a muchas inmunoterapias. Las respuestas autoinmunes podrían haberse anticipado dada la ubicuidad de APP, la cual transporta determinantes antigénicos en común con el producto proteolítico. Más recientemente, estudios adicionales se concentraron en la naturaleza de los anticuerpos agregados inducidos por la inmunización de Aß42 (en el hombre y en los ratones), revelando que la mayoría de los anticuerpos reconocen un pequeño dominio entre los aminoácidos 4 y 10 de Aß42 (Aß4-10). Los anticuerpos murinos pudieron bloquear la fibrilogénesis Aß y rompió las fibras Aß preexistentes (McLaurin et al, 2002 "Therapeutically effective antibodies against amyloid-ß peptide target amyloid-ß residues 4-10 and inhibit cytotoxicity and fibrillogenesis", Nature Med 8:1263). De hecho, los anticuerpos humanos no reaccionan con la APP expuesta en la superficie de las células o con cualquier otro producto proteolítico no agregado del precursor (Hock et al 2002 "Generation of antibodies specific for ß-amyloid by vaccination of patients with Alzheimer disease", Nature Med 8:1270). Se observó una clara diferencia entre los sueros humanos y murinos: en contraste con los sueros humanos, los anticuerpos murinos detectan Aß monoméricos, oligoméricos y fibrilares. Esta es importante y puede constituir un prerequisito para la potencia terapéutica, ya que se acumula la evidencia de que los pequeños oligómeros de Aß, que no son reconocidos por los anti-Aß humanos, constituyen los mayores protagonistas tóxicos en la enfermedad (Walsh et al, 2002: "Naturally secreted oligomers of amyloid B protein potently inhibit hippocampal long-term potentiation in vivo", Nature 416:535). Así, una nueva estrategia potencial es la inmunización con una vacuna que contiene los aminoácidos 4-10 del ß-amiloide (en vez del Aß42 agregado). A pesar de la eficacia no conocida, esta estrategia puede también encarar los problemas autoinmunes, puesto que los pacientes será inmunizados directamente con un "auto" epítopo (células B lineales).
El documento WO 00/72880 A da a conocer la utilización de fragmentos N-terminales de Aß42 en una vacuna para la enfermedad de Alzheimer.
El documento WO 01/18169 A2 da a conocer un procedimiento para llevar a cabo una inmunización contra enfermedades que formen placas, utilizando tecnologías de exposición.
A pesar de estos decepcionantes desarrollos en recientes estrategias de vacunación de AD, una vacuna Aß se considera todavía como la forma más prometedora para combatir la AD. Sin embargo, es necesario urgentemente mejorar y obtener nuevas estrategias en para vacunación de AD. Especialmente, dicha vacuna no inducirá células T y/o B.
Por tanto, la presente invención proporciona la utilización de un compuesto constituido por
para la preparación de una vacuna para la enfermedad de Alzheimer (AD).
Según la presente invención, se utiliza un mimotopo Aß42 para la vacunación contra AD. El mimotopo induce la producción de anticuerpos contra Aß42 pero no contra la APP original. El mimotopo puede identificarse con un anticuerpo (monoclonal) y bibliotecas peptídicas (disponibles comercialmente) (por ejemplo, según Reineke et al. 2000 "Identification of distinct antibody epitopes and mimotopes from a peptide array of 5520 randomly generated sequences", J. Immunol Methods 267:37). Se utiliza un anticuerpo (monoclonal) que no reconoce a APP pero detecta sólo distintas especies Aß con ácido aspártico amino terminal (un ejemplo de dicho anticuerpo se describe en Johnson-Wood et al 1997: "Amyloid precursor protein processing and Ab42 deposition in a transgenic mouse model of Alzheimer disease", PNAS 94:1550). Se ha demostrado que dicho anticuerpo constituye una herramienta ideal para identificar mimotopos vacunales apropiados durante la presente invención. Aunque dichos anticuerpos monoclonales mostraran que tenían efectos beneficiosos en un modelo murino de AD cuando se administraron directamente a los ratones (Bard et al., 2000: "Peripherally administered antibodies against amyloid ß-peptide enter the central nervous system and reduce pathology in a mouse model of Alzheimer disease", Nature Med 6:916), nunca se ha propuesto utilizarlos como herramientas de búsqueda de mimotopos para aislar compuestos vacunales AD.
En la técnica anterior, se concentraron...
Reivindicaciones:
1. Utilización de un compuesto, constituido por
para la preparación de una vacuna destinada a la enfermedad de Alzheimer (AD).
2. Utilización según la reivindicación 1, caracterizada porque dicho péptido tiene una longitud comprendida entre 6 y 12 aminoácidos.
3. Utilización según la reivindicación 1 ó 2, caracterizada porque el soporte proteico es KLH.
4. Utilización según cualquiera de las reivindicaciones anteriores, caracterizada porque la vacuna comprende además hidróxido de aluminio.
5. Utilización según cualquiera de las reivindicaciones anteriores, caracterizada porque la vacuna contiene el compuesto en una cantidad comprendida entre 0,1 ng y 10 mg.
6. Vacuna contra la enfermedad de Alzheimer que comprende un compuesto constituido por
7. Vacuna según la reivindicación 6, caracterizada porque el soporte proteico es KLH.
8. Vacuna según la reivindicación 6 ó 7, caracterizada porque comprende además hidróxido de aluminio.
9. Vacuna según cualquiera de las reivindicaciones 6 a 8, caracterizada porque contiene el compuesto en una cantidad comprendida entre 0,1 ng y 10 mg.
Patentes similares o relacionadas:
Composiciones nutricionales que contienen un componente de péptido y sus usos, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional para su uso para reducir la incidencia de la diabetes mellitus, en donde dicha composición nutricional comprende: (i) […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Péptidos para inhibir la angiogénesis, del 15 de Julio de 2020, de The Board of Trustees of the University of Illionis: Un peptido aislado para su uso en la inhibicion de la angiogenesis en un paciente que lo necesita, en donde el peptido comprende la secuencia de aminoacidos de KFARLWTEIPTAIT […]
Péptido que tiene actividad antiinflamatoria, y uso del mismo, del 8 de Julio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en una secuencia de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2 o SEQ ID NO: 3.
Péptido que tiene actividades antiinflamatoria, osteogénica y promotora del crecimiento del cabello, y uso del mismo, del 24 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que tiene actividad antiinflamatoria, que consiste en la secuencia de aminoácidos SEQ ID NO: 2.
Combinaciones de inhibidores de puntos de control inmunitarios, del 24 de Junio de 2020, de LYTIX BIOPHARMA AS: Un compuesto que tiene la fórmula Lys Lys Trp Trp Lys Lys Trp Dip Lys, o una sal, éster o amida del mismo; para su uso en el tratamiento […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.
Péptido que tiene actividades antiinflamatoria, osteogénica y de fomento del crecimiento del pelo, y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Péptido que tiene actividad antiinflamatoria, que consiste en secuencias de aminoácidos de SEQ ID NO: 3.