LIGANDO DE DOBLE ESPECIFICIDAD Y SU USO.
Un ligando de doble especificidad que comprende un dominio variable único de cadena pesada de inmunoglobulina que tiene una especificidad de unión a un primer antígeno o epítopo y un dominio variable único de cadena ligera de inmunoglobulina complementaria que tiene una especificidad de unión a un segundo antígeno o epítopo,
en el que dichos dominios no comparten la misma especificidad, y en el que los dominios variables unen sus respectivos antígenos o epítopos simultáneamente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2002/003014.
Solicitante: DOMANTIS LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: 980 GREAT WEST ROAD BRENTFORD, MIDDLESEX TW8 9GS REINO UNIDO.
Inventor/es: TOMLINSON,IAN,DOMANTIS LIMITED, WINTER,GREG,MRC LABORATORY OF MOLECULAR BIOLOGY, IGNATOVICH,OLGA,DOMANTIS LIMITED.
Fecha de Publicación: .
Fecha Solicitud PCT: 28 de Junio de 2002.
Fecha Concesión Europea: 11 de Agosto de 2010.
Clasificación Internacional de Patentes:
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C07K16/30 C07K 16/00 […] › de células tumorales.
- C07K16/40 C07K 16/00 […] › contra enzimas.
- C07K16/46D
Clasificación PCT:
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/13 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Inmunoglobulinas.
- C12N15/79 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a huéspedes eucariotas.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/542 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con inhibición estérica o modificación de la señal, p. ej. extinción de fluorescencia.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación antigua:
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/13 C12N 15/00 […] › Inmunoglobulinas.
- C12N15/79 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a huéspedes eucariotas.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/542 G01N 33/00 […] › con inhibición estérica o modificación de la señal, p. ej. extinción de fluorescencia.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
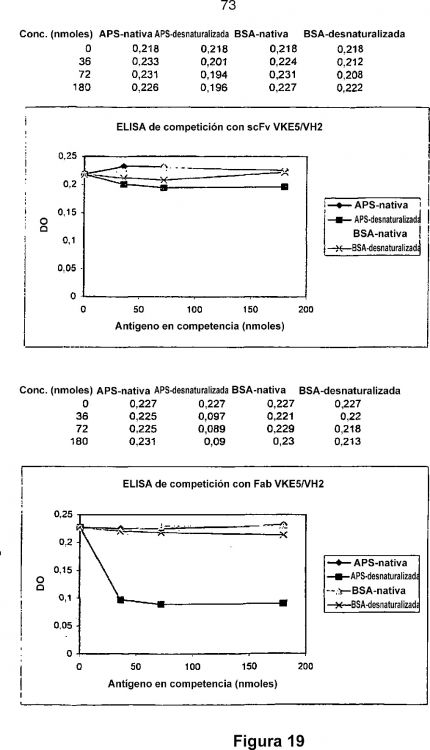
Fragmento de la descripción:
La presente invención se refiere a un procedimiento para preparar ligandos de doble especificidad que comprenden una primera región de dominio variable único de inmunoglobulina que se une a un primer antígeno o epítopo, y una segunda región de dominio variable único de inmunoglobulina complementaria que se une a un segundo antígeno o epítopo. También se describen los ligandos de doble especificidad y sus usos.
Introducción
El dominio de unión al antígeno de un anticuerpo comprende dos regiones separadas: un dominio variable de cadena pesada (VH) y un dominio variable de cadena ligera (VL: que puede ser Vκ oVλ). El propio sitio de unión al antígeno está formado por 6 bucles polipeptídicos: 3 de dominio VH (H1, H2 y H3) y 3 de dominio VL (L1, L2 y L3). Mediante la reordenación combinatoria de segmentos de genes se produce un repertorio principal diverso de genes de V que codifican los dominios VH y VL. El gen de VH se produce por recombinación de 3 segmentos de genes, VH, D y JH. En los seres humanos hay aproximadamente 51 segmentos VH funcionales (Cook y Tomlinson (1995) Immunol. Today, 16: 237), 25 segmentos D funcionales (Corbett y col. (1997) J. Mol. Biol., 268: 69) y 6 segmentos JH funcionales (Ravetch y col. (1981) Cell, 27: 583), dependiendo del halotipo. El segmento VH codifica la región de la cadena de polipéptido que forma el primer y segundo bucles de unión al antígeno del dominio VH (H1 y H2), mientras que los segmentos VH, D y JH se combinan para formar el tercer bucle de unión al antígeno del dominio VH (H3). El gen de VL se produce por la recombinación de solo dos segmentos de genes, VL y JL. En los seres humanos, hay aproximadamente 40 segmentos VK funcionales (Schäble y Zachau (1993) Biol. Chem. Hoppe-Seyler, 374: 1001), 31 segmentos Vλ funcionales (Williams y col. (1996) J. Mol. Biol., 264: 220; Kawasaki y col. (1997) Genome Res., 7: 250), 5 segmentos Jκ funcionales (Hieter y col. (1982)
J. Biol. Chem., 257: 1516) y 4 segmentos Jλ funcionales (Vasicek y Leder (1990) J. Exp. Med.,
172: 609), dependiendo del halotipo. El segmento VL codifica la región de la cadena de polipéptido que forma el primer y segundo bucles de unión al antígeno del dominio VL (L1 y L2), mientras que los segmentos VL y JL se combinan para formar el tercer bucle de unión al antígeno del dominio VL (L3). Se cree que los anticuerpos seleccionados de este repertorio principal son suficientemente diversos para unirse a prácticamente todos los antígenos con una afinidad al menos moderada. Los anticuerpos de alta afinidad se producen por “maduración de afinidad” de genes reordenados, en los que se generan mutaciones puntuales y son seleccionadas por el sistema inmunitario basándose en la unión mejorada.
El análisis de las estructuras y secuencias de anticuerpos ha mostrado que 5 de los 6 bucles de unión al antígeno (H1, H2, L1, L2, L3) tienen un número limitado de conformaciones de la cadena principal o estructuras canónicas (Chothia y Lesk (1987) J. Mol. Biol., 196: 901; Chothia y col. (1989) Nature, 342: 877). Las conformaciones de la cadena principal se determinan por (i) la longitud del bucle de unión al antígeno, y (ii) restos particulares, o tipos de restos, en determinadas posiciones clave en el bucle de unión al antígeno y el marco conservado del anticuerpo. El análisis de las longitudes de los bucles y los restos clave ha permitido a los autores de la invención predecir las conformaciones de las cadenas principales de H1, H2, L1, L2 y L3 codificadas por la mayoría de las secuencias de anticuerpos humanos (Chothia y col. (1992) J. Mol. Biol., 227: 799; Tomlinson y col. (1995) EMBO J., 14: 4628; Williams y col. (1996) J. Mol. Biol., 264: 220). Aunque la región H3 es mucho más diversa en términos de secuencia, longitud y estructura (debido al uso de segmentos D), también forma un número limitado de confirmaciones de la cadena principal para longitudes de bucle cortas que dependen de la longitud y la presencia de restos particulares, o de tipos de restos, en posiciones clave en el bucle y el marco conservado del anticuerpo (Martin y col. (1996) J. Mol. Biol., 263: 800; Shirai y col. (1996) FEBS Letters, 399: 1.
Se conocen en la técnica anticuerpos biespecíficos que comprenden parejas complementarias de las regiones VH y VL. Estos anticuerpos biespecíficos deben comprender dos parejas de VH y VL, uniéndose cada pareja de VH/VL a un solo antígeno o epítopo. Los procedimientos descritos implican hibridomas híbridos (Milstein y Cuello AC, Nature 305:53740), minianticuerpos (Hu y col., (1996) Cancer Res 56:3055-3061), fragmentos bivalentes (Holliger y col., (1993) Proc. Natl. Acad. Sci. USA 90, 6444-6448; documento WO 94/13804), anticuerpos recombinantes quelantes (CRAbs; (Neri y col., (1995) J. Mol. Biol. 246, 367-373), biscFv (p. ej., Atwell y col., (1996) Mol. Immunol. 33, 1301-1312), anticuerpos estabilizados de "botón en ojal" (Carter y col., (1997) Protein Sci. 6, 781-788). En cada caso, cada especie de anticuerpo comprende dos sitios de unión al antígeno, cada uno formado por una pareja complementaria de dominios VH y VL. De esta forma, cada anticuerpo se puede unir a dos antígenos o epítopos diferentes al mismo tiempo, con la unión a cada antígeno o epítopo mediada por un dominio VH y su complementario VL. Cada una de estas técnicas presenta sus desventajas particulares; por ejemplo, en el caso de los hibridomas híbridos, las parejas VH/VL inactivas pueden reducir mucho la fracción de IgG biespecífica. Además, la mayoría de los procedimientos biespecíficos se basan en la asociación de diferentes parejas VH/VL o la asociación de cadenas de VH y VL para recrear los dos sitios de unión de VH/VL diferentes. Por lo tanto es imposible controlar la relación de sitios de unión a cada antígeno o epítopo en la molécula ensamblada y por lo tanto, muchas de las moléculas ensambladas se unirán a un antígeno o epítopo pero no al otro. En algunos casos ha sido posible diseñar las cadenas pesada o ligera en las interfases de subunidades (Carter y col., 1997) con el fin de mejorar el número de moléculas que tienen sitios de unión a ambos antígenos o epítopos, pero esto nunca da como resultado todas las moléculas que tienen unión a ambos antígenos o epítopos.
Existen algunas pruebas de que se pueden incorporar dos especificidades de unión de anticuerpos en el mismo sitio de unión, pero esto generalmente representa dos o más especificidades que corresponden a antígenos o epítopos estructuralmente relacionados, o a anticuerpos que tienen reactividad cruzada amplia. Por ejemplo, se han descrito anticuerpos de reactividad cruzada, normalmente cuando los dos antígenos tienen secuencia y estructura relacionadas, tales como la lisozima de clara de huevo de gallina y la lisozima de pavo (McCafferty y col., documento WO 92/01047) o el hapteno libre y el hapteno conjugado con vehículo (Griffiths AD y col. EMBO J. 1994 13:14 3245-60). En un ejemplo adicional, el documento WO 02/02773 (Abbott Laboratories), publicado después de la fecha de prioridad de la presente solicitud, describe moléculas de anticuerpo con “especificidad doble”. Las moléculas de anticuerpo a las que se hace referencia son anticuerpos preparados o seleccionados contra antígenos múltiples, de modo que su especificidad se extiende más que un solo antígeno. Cada pareja complementaria VH/VL en los anticuerpos del documento WO 02/02773 especifica una sola especificidad de unión para dos o más antígenos estructuralmente relacionados; los dominios VH y VL en dichas parejas complementarias no tienen cada una, una especificidad separada. Por lo tanto, los anticuerpos tienen una extensa especificidad única que abarca dos antígenos, que están estructuralmente relacionados. Además, se ha descrito que los autoanticuerpos naturales son polirreactivos (Casali y Notkins, Ann. Rev. Immunol. 7, 515-531), reaccionando con al menos dos (normalmente más) antígenos o epítopos diferentes que no están estructuralmente relacionados. También se ha mostrado que las selecciones de repertorios de péptidos aleatorios usando la tecnología de presentación en fagos de un anticuerpo monoclonal, identificará una variedad de secuencias de péptidos que se ajustan al sitio de unión al antígeno. Algunas de las secuencias están muy relacionadas, ajustándose a una secuencia consenso, mientras que otras son muy diferentes y se han denominado mimotopos (Lane y Stephen, Current Opinion in Immunology, 1993, 5, 268-271). Por lo tanto, está claro que el sitio de unión de un anticuerpo, que comprende los dominios VH y VL asociados y complementarios, tiene el potencial de unirse a muchos antígenos diferentes de un...
Reivindicaciones:
1. Un ligando de doble especificidad que comprende un dominio variable único de cadena pesada de inmunoglobulina que tiene una especificidad de unión a un primer antígeno o epítopo y un dominio variable único de cadena ligera de inmunoglobulina complementaria que tiene una especificidad de unión a un segundo antígeno o epítopo, en el que dichos dominios no comparten la misma especificidad, y en el que los dominios variables unen sus respectivos antígenos o epítopos simultáneamente.
2. El ligando de doble especificidad de la reivindicación 1, en el que el primer y el segundo epítopos están presentes en diferentes antígenos.
3. El ligando de doble especificidad de la reivindicación 1, en el que el primero y el segundo epítopos están presentes en el mismo antígeno.
4. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 3, en el que los VH y VL los proporciona un fragmento scFv de anticuerpo.
5. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 3, en el que los VH y VL los proporciona una región Fab de anticuerpo.
6. Una IgG que comprende un ligando de doble especificidad de una cualquiera de las reivindicaciones 1 a 3.
7. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 3, en el que las regiones variables están asociadas de forma no covalente.
8. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 3, en el que las regiones variables están asociadas de forma covalente.
9. Un ligando de doble especificidad según la reivindicación 8, en el que la asociación covalente está mediada por enlaces disulfuro.
10. Un ligando de doble especificidad según cualquier reivindicación precedente, que comprende un marco conservado universal.
11. Un ligando de doble especificidad según la reivindicación 10, en el que el marco conservado universal comprende un marco conservado VH seleccionado del grupo constituido por DP47, DP45 y DP38; y/o el marco conservado VL es DPK9.
12. Un ligando de doble especificidad según cualquier reivindicación precedente, que comprende el sitio de unión para un ligando genérico específico.
13. Un ligando de doble especificidad según cualquier reivindicación precedente, en el que una especificidad del mismo es por un agente eficaz para aumentar la semivida del ligando.
14. Un ligando de doble especificidad según cualquier reivindicación precedente, que tiene una especificidad por un antígeno seleccionado de proteínas humanas y animales, citocinas, receptores de citocinas, cofactores enzimáticos para enzimas y proteínas de unión a ADN.
15. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 13, que tiene especificidad por un antígeno seleccionado de ApoE, Apo-SAA, BDNF, Cardiotrofina1, EGF, receptor de EGF, ENA-78, Eotaxina, Eotaxina-2, Exodus-2, FGF-ácido, FGF-básico, factor de crecimiento de fibroblastos-10 (30), ligando FLT3, fractalcina (CX3C), GDNF, GCSF, GM-CSF, GF-β1, insulina, IFN-γ, IGF-I, IGF-II, IL-Iα, IL-1β, IL-2, IL-3; IL-4, IL-5, IL-6, IL-7, IL-8 (72 aa), IL-8 (77 aa), IL-9, IL-10, IL-11, IL-12, IL-13, IL-15, IL-16, IL-17, IL-18 (IGIF), inhibina α, inhibina β, IP-10, factor de crecimiento de queratinocitos-2 (KGF-2), KGF, leptina, LIF, linfotactina, sustancia inhibidora mulleriana, factor inhibidor de colonias de monocitos, proteína atractora de monocitos (30 véase antes), M-CSF, MDC (67 aa), MDC (69 aa), MCP-1 (MCAF), MCP-2, MCP-3, MCP-4, MDC (67 aa), MDC (69 aa), MIG, MIP-1α, MIP-1β, MIP-3α, MIP-3β, MIP-4, factor inhibidor de progenitores mieloides-1 (MPIF-1), NAP-2, neurturina, factor de crecimiento nervioso, β-NGF, NT-3, NT-4, oncostatina M, PDGF-AA, PDGF-AB, PDGF-BB, PF4, RANTES, SDF1α, SDF1β, SCF, SCGF, factor de células madre (SCF), TARC, TGF-α, TGFβ, TGF-β2, TGF-β3, factor de necrosis tumoral (TNF), TNF-α, TNF-β, receptor de TNF I, receptor de TNF II, TNIL-1, TPO, VEGF, receptor de VEGF 1, receptor de VEGF 2, receptor de VEGF 3, GCP-2, GRO/MGSA, GRO-β, GRO-γ, HCC1, 1-309, HER 1, HER 2, HER 3 y HER 4.
16. Un ligando de doble especificidad según una cualquiera de las reivindicaciones 1 a 13, que tiene una especificidad por un receptor para una citocina indicada en la reivindicación 15.
17. Un ligando de doble especificidad según la reivindicación 3, en el que el antígeno es un
antígeno indicado en la reivindicación 15 ó 16.
18. Ácido nucleico que codifica al menos un ligando de doble especificidad según cualquier reivindicación precedente.
19. Un vector que comprende el ácido nucleico según la reivindicación 18.
20. Un vector según la reivindicación 19, que además comprende los componentes necesarios para la expresión de un ligando de doble especificidad.
21. Un procedimiento para producir un ligando de doble especificidad según cualquiera de las reivindicaciones 1 a 17, que comprende un primer dominio variable único de cadena pesada de inmunoglobulina que tiene una primera especificidad de unión y un segundo dominio variable único de cadena ligera de inmunoglobulina complementario que tiene una segunda especificidad de unión, comprendiendo el procedimiento las etapas de:
a) seleccionar un primer dominio variable por su capacidad para unirse a un primer epítopo,
b) seleccionar un segundo dominio variable por su capacidad para unirse a un segundo epítopo,
c) combinar los dominios variables; y
d) seleccionar el ligando de doble especificidad por su capacidad para unirse a dichos
primer y segundo epítopos.
22. Un procedimiento según la reivindicación 21, en el que dicho primer dominio variable se selecciona para la unión a dicho primer epítopo en ausencia de un dominio variable complementario.
23. Un procedimiento según la reivindicación 21, en el que dicho primer dominio variable se selecciona para la unión a dicho primer epítopo en presencia de un tercer dominio variable complementario, en el que dicho tercer dominio variable es diferente de dicho segundo dominio variable.
24. Un procedimiento según cualquiera de las reivindicaciones 21 a 23, en el que las regiones variables derivan de inmunoglobulinas dirigidas contra dichos epítopos.
25. Un procedimiento según cualquiera de las reivindicaciones 21 a 24, en el que dichos primer y segundo epítopos están presentes en antígenos separados.
26. Un procedimiento según cualquiera de las reivindicaciones 21 a 24, en el que dichos 5 primer y segundo epítopos están presentes en el mismo antígeno.
27. Un procedimiento según cualquiera de las reivindicaciones 21 a 26, en el que el dominio variable deriva de un repertorio de dominios de anticuerpos únicos.
28. Un procedimiento de la reivindicación 27, en el que dicho repertorio se presenta en la superficie de un bacteriófago filamentoso y en el que los dominios únicos de anticuerpos se seleccionan por la unión del repertorio en el bacteriófago a un antígeno.
29. Un procedimiento de cualquiera de las reivindicaciones 21 a 28 precedentes, en el que 15 la secuencia de al menos un dominio variable se modifica por mutación o barajado de ADN.
Patentes similares o relacionadas:
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Terapia basada en anticuerpos de la amiloidosis por transtiretina (TTR) y anticuerpos de origen humano para ese propósito, del 22 de Julio de 2020, de Neurimmune Holding AG: Un anticuerpo anti-transtiretina (TTR) de origen humano o un fragmento de unión a antígeno del mismo, que es capaz de unirse a especies de TTR mutadas, mal plegadas, […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Redirectores de células T específicas de antígenos, del 1 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una nanoparticula que comprende en su superficie: (A) un anticuerpo que se une especificamente a un antigeno de celula diana o epitopo del mismo; y (B) un resto […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
Moléculas de unión con cadena J modificada, del 24 de Junio de 2020, de IGM BIOSCIENCES, INC: Una molécula de unión que comprende un anticuerpo de IgM, IgA, IgG/IgM o IgG/IgA con una cadena J modificada, donde la cadena J modificada comprende una cadena […]
Terapia de combinación para tratamiento de enfermedad, del 24 de Junio de 2020, de Mereo BioPharma 5, Inc: Un anticuerpo antagonista del ligando 4 tipo delta (DLL4) para su uso en un procedimiento para tratar el cáncer, inhibir el crecimiento tumoral, mejorar […]