PROCEDIMIENTO PARA LA PRODUCCION DE DIPEPTIDOS.
Un procedimiento para producir un dipéptido, que comprende: cultivar en un medio un microorganismo que tiene la capacidad de producir una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos donde la proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos es una proteína seleccionada del grupo que consiste en los siguientes apartados [1] a [11]:
[1] una proteína que tiene la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8; [2] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; [3] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; [4] una proteína que tiene una secuencia de aminoácidos que tiene una homología del 80% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 17 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; ES 2 347 875 T3 [5] una proteína que tiene la secuencia de aminoácidos mostrada en el SEQ ID NO: 37 o 38; null - 359 - [6] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en el SEQ ID NO: 37 o 38 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; [7] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 37 o 38 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; [8] una proteína que no tiene actividad péptido sintetasa ribosomal (referida en adelante como NRPS); [9] una proteína que tiene la secuencia de aminoácidos mostrada en el SEQ ID NO: 43; [10] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en el SEQ ID NO: 43 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; y [11] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 43 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos. ES 2 347 875 T3 y donde dicho microorganismo ha sido modificado genéticamente con el fin de que tenga la capacidad de producir al menos una de dichas una o más clases de aminoácidos; permitir que el dipéptido se forme y se acumule en el medio; y recuperar el dipéptido del null medio. - 360 -
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05013734.
Solicitante: KYOWA HAKKO KOGYO CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 1-6-1, OHTEMACHI, CHIYODA-KU,TOKYO 100-8185.
Inventor/es: HASHIMOTO,SHIN-ICHI, TABATA,KAZUHIKO.
Fecha de Publicación: .
Fecha Solicitud PCT: 24 de Junio de 2005.
Fecha Concesión Europea: 21 de Julio de 2010.
Clasificación Internacional de Patentes:
- C07K5/06A1
- C12N9/00L
- C12P21/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › que tienen una secuencia conocida de varios aminoácidos, p. ej. glutation.
Clasificación PCT:
- C07K5/06 C […] › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Dipéptidos.
Clasificación antigua:
- C07K5/06 C07K 5/00 […] › Dipéptidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
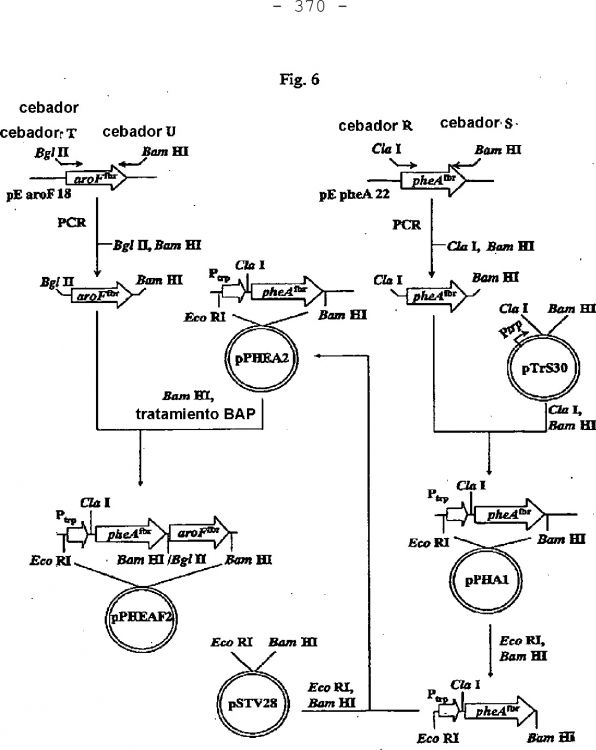
Fragmento de la descripción:
Antecedentes de la Invención
La presente invención se refiere a un procedimiento para producir un dipéptido que comprende cultivar en un 5 medio un microorganismo que tiene la capacidad de producir una proteína como se define en las reivindicaciones que tiene una actividad formadora de una
o más clases de aminoácidos y donde dicho microorganismo ha sido modificado genéticamente para que tenga la
10 capacidad de producir al menos una de dichas una o más clases de aminoácidos, permitir que el dipéptido se forme y se acumule en el medio, y recuperar el dipéptido del medio. En la actualidad, muchos de los aminoácidos son producidos mediante el denominado método de fermentación (Hiroshi Soda, et al., Amino Acid Fermentation, Gakkai Shuppan Center (1986) y Biotechnology 2a ed., Vol. 6, Products of Primary Metabolism, VCH Verlagsgesellschaft mbH, Weinheim (1996)). El método de fermentación utilizado en la presente memoria hace referencia a un método en el que se cultiva un microorganismo en un medio que comprende sustancias poco costosas tales como glucosa, ácido acético, metanol, amoníaco, sulfato de amonio y aguas de infusión de maíz para obtener un aminoácido deseado utilizando la actividad metabólica del microorganismo. El método de fermentación es excelente como método para producir aminoácidos a partir de materiales poco costosos con ligeras cargas medioambientales.
30 En cuanto al método de síntesis peptídica a gran escala, se conocen métodos de síntesis química (método en fase líquida y método en fase sólida), métodos de síntesis enzimática y métodos de síntesis biológica que utilizan técnicas de ADN recombinante. Actualmente, los métodos de síntesis enzimática y los métodos de síntesis biológica se emplean para la síntesis de péptidos de cadena larga mayores de 50 residuos, y los métodos de síntesis química y los métodos de síntesis enzimática se emplean principalmente para la síntesis de dipéptidos.
En la síntesis de dipéptidos mediante métodos de síntesis química, son necesarias operaciones tales como la introducción y eliminación de grupos protectores para grupos funcionales, y también se forman racematos. Los métodos de síntesis química son considerados de este modo poco ventajosos con respecto al coste y la eficacia. Son poco favorables también desde el punto de vista de la higiene medioambiental debido al uso de grandes cantidades de disolventes orgánicos y similares.
En cuanto a la síntesis de dipéptidos mediante métodos enzimáticos, se conocen los siguientes métodos: un método que utiliza la reacción inversa de la proteasa
(J. Biol. Chem., 119, 707-720 (1937)); métodos que utilizan aminoacil-ARN-t-transferasa termoestable (Solicitud de Patente Japonesa no Examinada, Publicada Núm. 146539/83, Solicitud de Patente Japonesa no Examinada, Publicada Núm. 209991/83, Solicitud de Patente Japonesa no Examinada, Publicada Núm. 209992/83 Solicitud de Patente Japonesa no Examinada, Publicada Núm. 106298/84); un método que utiliza la reacción inversa de la prolina-iminopeptidasa (documento WO 03/010307 folleto); y métodos que utilizan péptido sintetasa no ribosómica (referida en adelante como NRPS por sus siglas en inglés) (Chem. Biol., 7, 373-384 (2000), FEBS Lett., 498, 42-45 (2001), Patente de los Estados Unidos Núm.
5.795.738 y Patente de los Estados Unidos Núm. 5.652.116, documento EP 1 096 011).
Sin embargo, el método que utiliza la reacción inversa de la proteasa requiere la introducción y eliminación de grupos protectores para grupos funcionales de aminoácidos utilizados como sustratos, lo que ocasiona dificultades al aumentar la eficacia de la reacción de formación de péptidos y evitar la reacción peptidolítica. Los métodos que utilizan la aminoacil-ARN-t sintetasa termoestable tienen el defecto de que la expresión de la enzima y la prevención de reacciones secundarias que forman subproductos distintos de los productos deseados resultan difíciles. El método que utiliza prolinaiminopeptidasa requiere la amidación de uno de los aminoácidos utilizados como sustratos. Los métodos que utilizan NRPS son poco eficaces ya que es necesario el suministro de la coenzima 4'-fosfopanteteína.
Además de los defectos anteriores, estos métodos son poco ventajosos respecto a los costes de producción ya que todos ellos utilizan aminoácidos o sus derivados como sustratos.
Por otra parte, existe un grupo de péptido sintetasas que tienen un peso molecular de enzima inferior al de los NRPS y no requieren la coenzima 4'fosfopanteteína: por ejemplo, γ-glutamilcisteína sintetasa, glutatión sintetasa, D=alanil-D-alanina (D-Ala-D-Ala) ligasa, y poli-γ-glutamato sintetasa. La mayoría de las enzimas utilizan D-aminoácidos como sustratos o catalizan la formación de enlaces peptídicos en el grupo γ-carboxilo. Debido a tales propiedades, no pueden ser utilizadas para la síntesis de dipéptidos por medio de la formación de enlaces peptídicos en el grupo α-carboxilo del L-aminoácido.
Se ha informado de que una proteína que no tiene similitud con NRPS (producto del gen albC) es responsable de la síntesis de la estructura de la ciclo(Lfenilalanil-L-leucina) en Streptomyces noursei ATCC 11455 conocida como cepa productora del antibiótico albonoursina y de que la albonoursina fue detectada cuando la ciclo-dipéptido oxidasa se hizo actuar sobre el caldo de cultivo de Escherichia coli y streptomyces lividans en las que se había introducido el gen albC (Chemistry & Biol., 9, 1355-1364 (2002)). No obstante, no existe ningún informe de que el producto del gen albC forme un dipéptido de cadena lineal.
El único ejemplo conocido de una enzima susceptible de síntesis de dipéptidos por medio de la actividad para formar un enlace peptídico en el grupo α-carboxilo del Laminoácido es la bacilisina (antibiótico dipeptídico derivado de un microorganismo perteneciente al género Bacillus) sintetasa. Se sabe que la bacilisina sintetasa tiene la actividad sintetizadora de bacilisina [L-alanilL-anticapsina (L-Ala-L-anticapsina)] y L-alanil-L-alanina (L-Ala-L-Ala), pero no hay información a cerca de su actividad para sintetizar otros dipéptidos (J. Ind. Microbiol., 2, 201-208 (1987) y Enzimas. Microbial. Technol., 29, 400-406 (2001)).
En cuanto a los genes de la bacilisina biosintetasa de Bacillus subtilis 168 cuya información del genoma completo ha sido aclarada (Nature, 390, 249-256 (1997)), se sabe que la productividad de la bacilisina aumenta mediante la amplificación de operones de la bacilisina que contienen ORF ywfA-F (documento WO00/03009 folleto). No obstante, no se sabe si un ORF que codifica una proteína que tiene actividad ligadora de dos o más aminoácidos por medio de enlaces peptídicos está contenido en estos ORF, y si está contenido, qué ORF codifica la proteína. Los microorganismos en los cuales las actividades de una o más clases de peptidasas y una o más clases de proteínas que tienen actividad transportadora de péptidos se han reducido o perdido y que tienen la capacidad de producir un dipéptido han sido descritos en el documento EP 1 529 837.
Esto es, hasta ahora no se conoce ningún método para producir un dipéptido que conste de una o más clases de aminoácidos mediante fermentación.
Un objeto de la presente invención es proporcionar un procedimiento para producir un dipéptido que comprende cultivar en un medio un microorganismo que tiene la capacidad para producir una proteína como se define en las reivindicaciones que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos y donde dicho microorganismo ha sido modificado genéticamente con el fin de que tenga la capacidad de producir al menos una de dichas una o más clases de aminoácidos, permita la formación del dipéptido y se acumule en el medio, y recuperar el dipéptido del medio.
Compendio de la Invención
La presente invención se refiere a los siguientes apartados (1) a (14).
1. (1) Un procedimiento para producir un dipéptido, que comprende: cultivar en un medio un microorganismo que tiene la capacidad de producir una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos donde la proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos es una proteína seleccionada del grupo que consiste en los siguientes apartados [1] a [11]:
[1] una proteína que tiene la secuencia de aminoácidos mostrada...
Reivindicaciones:
1. Un procedimiento para producir un dipéptido, que comprende: cultivar en un medio un microorganismo que tiene la capacidad de producir una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos donde la proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos es una proteína seleccionada del grupo que consiste en los siguientes apartados [1] a [11]:
[1] una proteína que tiene la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8;
[2] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[3] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 1 a 8 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[4] una proteína que tiene una secuencia de aminoácidos que tiene una homología del 80% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 17 y que tiene actividad formadora del
dipéptido a partir de una o más clases de aminoácidos; [5] una proteína que tiene la secuencia deaminoácidos mostrada en el SEQ ID NO: 37 o 38;
[6] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en el SEQ ID NO: 37 o 38 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[7] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 37 o 38 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[8] una proteína que no tiene actividad péptido
sintetasa ribosomal (referida en adelante como NRPS); [9] una proteína que tiene la secuencia deaminoácidos mostrada en el SEQ ID NO: 43;
[10] una proteína que consiste en una secuencia de aminoácidos donde uno o más residuos de aminoácidos son suprimidos, sustituidos o añadidos en la secuencia de aminoácidos mostrada en el SEQ ID NO: 43 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos; y
[11] una proteína que consiste en una secuencia de aminoácidos que tiene una homología del 65% o más con la secuencia de aminoácidos mostrada en el SEQ ID NO: 43 y que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos. y donde dicho microorganismo ha sido modificado genéticamente con el fin de que tenga la capacidad de producir al menos una de dichas una o más clases de aminoácidos; permitir que el dipéptido se forme y se acumule en el medio; y recuperar el dipéptido del medio.
2. El procedimiento de acuerdo con la Reivindicación 1, donde la proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos es una proteína codificada por el ADN seleccionado del grupo que consiste en los siguientes apartados [1] a [8]:
[1] ADN que tiene la secuencia de nucleótidos mostrada en cualquiera de los SEQ ID NOS: 9 a 16 y 36;
[2] ADN que hibrida con ADN que tiene una secuencia de nucleótidos complementaria a la secuencia de nucleótidos mostrada en cualquiera de los SEQ ID NOS: 9 a 16 y 36 en condiciones restrictivas y que codifica una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[3] ADN que tiene una secuencia de nucleótidos que tiene una homología de 80% o más con la secuencia de nucleótidos mostrada en el SEQ ID NO: 18 y que codifica una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[4] ADN que tiene la secuencia de nucleótidos mostrada en el SEQ ID NO: 39 o 40;
[5] ADN que hibrida con ADN que tiene una secuencia de nucleótidos complementaria a la secuencia de nucleótidos mostrada en el SEQ ID NO: 39 o 40 en condiciones restrictivas y que codifica una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos;
[6] ADN que codifica una proteína que tiene actividad NRPS; [7] ADN que tiene la secuencia de nucleótidosmostrada en el SEQ ID NO: 44; y
[8] ADN que hibrida con ADN que tiene una secuencia de nucleótidos complementaria a la secuencia de nucleótidos mostrada en el SEQ ID NO: 44 en condiciones restrictivas y que codifica una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos.
3. El procedimiento de acuerdo con la Reivindicación 1, donde el microorganismo que tiene la capacidad de producir una proteína que tiene actividad formadora del dipéptido a partir de una o más clases de aminoácidos es un microorganismo que porta un ADN recombinante que comprende el ADN seleccionado del grupo que consiste en los apartados [1] a [8] de la Reivindicación 2.
4. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 1 a 3, donde la capacidad para producir un aminoácido se adquiere mediante un método seleccionado del grupo que consiste en los siguientes apartados [1] a [5]:
[1] un método en el que al menos uno de los mecanismos que regulan la biosíntesis del aminoácido se hace más flexible o se cancela;
[2] un método en el que la expresión de al menos una de las enzimas implicadas en la biosíntesis del aminoácido está intensificada;
[3] un método en el que el número de copias de al menos uno de los genes de las enzimas implicadas en la biosíntesis del aminoácido se incrementa;
[4] un método en el que al menos una de las rutas metabólicas que se ramifican a partir de la ruta biosintética del aminoácido a los metabolitos distintos del aminoácido se debilita o se bloquea; y
[5] un método en el que se selecciona una cepa celular que tiene una mayor resistencia a un análogo del aminoácido en comparación con la cepa de tipo salvaje.
5. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 1 a 4, donde el microorganismo es un microorganismo perteneciente al género Escherichia, Corynebacterium, Bacillus, Serratia, Pseudomonas o Streptomyces.
6. El procedimiento de acuerdo con la Reivindicación 5, donde el microorganismo perteneciente al género Escherichia, Corynebacterium, Bacillus, Serratia, Pseudomonas o Streptomyces es Escherichia coli, Corynebacterium glutamicum, Corynebacterium ammoniagenes, Corynebacterium lactofermentum, Corynebacterium flavum, Corynebacterium efficiens, Bacillus subtilis, Bacillus megaterium, Serratia marcescens, Pseudomonas putida, Pseudomonas aeruginosa, Streptomyces coelicolor o Streptomyces lividans.
7. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 1 a 4, donde el microorganismo es un microorganismo en el cual las actividades de una o más clases de peptidasas y una o más clases de proteínas que tienen actividad de penetración/transporte de péptidos (referidas en adelante también como proteínas de penetración/transporte de péptidos) se reducen o se pierden.
8. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 1 a 4, donde el microorganismo es un microorganismo en el que las actividades de tres o más clases de peptidasas se reducen o se pierden.
9. El procedimiento de acuerdo con la Reivindicación 7 u 8, donde la peptidasa es una proteína que tiene la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 45 a 48, o una proteína que tiene una secuencia de aminoácidos que tiene una homología del 80%
o más con la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 45 a 48 y que tiene actividad peptidasa.
10. El procedimiento de acuerdo con la Reivindicación 7 o 9, donde la proteína de penetración/transporte de péptidos es una proteína que tiene la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 49 a 53, o una proteína que tiene una secuencia de aminoácidos que tiene una homología de 80% o más con la secuencia de aminoácidos mostrada en cualquiera de los SEQ ID NOS: 49 a 53 y que tieneactividad de penetración/transporte de péptidos.
11. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 7 a 10, donde el microorganismo es un microorganismo perteneciente al género Escherichia, Bacillus o Corynebacterium.
12. El procedimiento de acuerdo con la Reivindicación 11, donde el microorganismo perteneciente al género Escherichia, Bacillus o Corynebacterium es Escherichia coli, Corynebacterium glutamicum, Corynebacterium ammoniagenes, Corynebacterium lactofermentum, Corynebacterium flavum, Corynebacterium efficiens, Bacillus subtilis o Bacillus megaterium.
13. El procedimiento de acuerdo con cualquiera de las Reivindicaciones 1 a 12, donde el aminoácido es un aminoácido seleccionado del grupo que consiste en L
alanina, L-glutamina, ácido L-glutámico, glicina, Lvalina, L-leucina, L-isoleucina, L-prolina, Lfenilalanina, L-triptófano, L-metionina, L-serina, Ltreonina, L-cisteína, L-asparagina, L-tirosina, L-lisina,
5 L-arginina, L-histidina, ácido L-aspártico, ácido L-αaminobutírico, L-4-hidroxiprolina, L-3-hidroxiprolina, Lornitina y L-citrulina.
14. El procedimiento de acuerdo con cualquiera de
10 las Reivindicaciones 1 a 13, donde el dipéptido es un dipéptido representado por la fórmula (I):
R1-R2 (I)
15 (donde R1 y R2, que pueden ser iguales o diferentes, representan cada uno un aminoácido seleccionado del grupo que consiste en L-alanina, L-glutamina, ácido Lglutámico, glicina, L-valina, L-leucina, L-isoleucina, Lprolina, L-fenilalanina, L-triptófano, L-metionina, L
20 serina, L-treonina, L-cisteína, L-asparagina, L-tirosina, L-lisina, L-arginina, L-histidina, ácido L-aspártico, ácido L-α-aminobutírico, L-4-hidroxiprolina, L-3hidroxiprolina, L-ornitina y L-citrulina.
25
Patentes similares o relacionadas:
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
PROCEDIMIENTO DE OBTENCIÓN DE SUBPRODUCTOS A PARTIR DE RESIDUOS DE CAFÉ Y APLICACIONES DE LOS MISMOS, del 13 de Julio de 2020, de UNIVERSIDAD DE GRANADA: Procedimiento de obtención de subproductos a partir de residuos de café y aplicaciones de los mismos. La presente invención consiste en un proceso […]
Biblioteca de péptidos y su uso, del 8 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Una biblioteca de péptidos que comprende una pluralidad de péptidos diferentes en la que los péptidos comprenden cada uno una secuencia de aminoácidos […]
Métodos para controlar la producción de proteasas, del 1 de Julio de 2020, de ROAL OY: Una célula hospedadora que comprende al menos un gen cromosómico inactivado en donde el gen cromosómico inactivado comprende una secuencia de ácido nucleico que codifica un […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Proceso para la purificación de daptomicina, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina que comprende: a) someter a la daptomicina a condiciones en las que una solución micelar de daptomicina se forma alterando el pH; y […]
Lipopéptidos de alta pureza, micelas de lipopéptidos y procesos para preparar los mismos, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina a partir de moléculas o agregados de alto peso molecular, en donde la daptomicina se proporciona en forma micelar, dicho […]
Métodos para ajustar los niveles de producción de carotenoides y composiciones en géneros de Rhodosporidium y Rhodotorula, del 15 de Abril de 2020, de TEMASEK LIFE SCIENCES LABORATORY LIMITED: Un método para ajustar el nivel de producción y la composición de carotenoides en un huésped fúngico que comprende: (a) manipular genéticamente […]