INMUNOENSAYO TURBIDIMETRICO PARA EVALUAR CISTATINA C HUMANA.
Un inmunoensayo turbidimétrico para evaluar Cistatina C humana en una muestra líquida corporal humana por medio de:
(a) formar una mezcla de ensayo poniendo en contacto dicha muestra con un conjugado de nanopartículas-anticuerpos, que comprende nanopartículas adecuadas para medición turbidimétrica, en la que dichas nanopartículas están recubiertas con un recubrimiento de material proteináceo que comprende anticuerpos de Cistatina C anti-humana o fragmentos que se unen al antígeno de los mismos, para unirse a dicha Cistatina C, en la que dichas nanopartículas recubiertas tienen un diámetro medio en el intervalo de más de 58 nm hasta 200 nm, y
(b) evaluar el contenido en Cistatina C humana midiendo el cambio en turbidez de dicha mezcla; en la que el recubrimiento es de tal forma que dichas nanopartículas están recubiertas con del 10% al 35% de anticuerpo que se une a Cistatina C humana por peso total del conjugado nanopartículas-anticuerpos
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2006/004182.
Solicitante: GENTIAN AS.
Nacionalidad solicitante: Noruega.
Dirección: KOLSRODVEIEN 120,1599 MOSS.
Inventor/es: SUNDE,KATHRIN, NILSEN,TOM.
Fecha de Publicación: .
Fecha Concesión Europea: 26 de Mayo de 2010.
Clasificación Internacional de Patentes:
- G01N33/543D6
Clasificación PCT:
- G01N33/543 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un soporte insoluble para la inmovilización de compuestos inmunoquímicos.
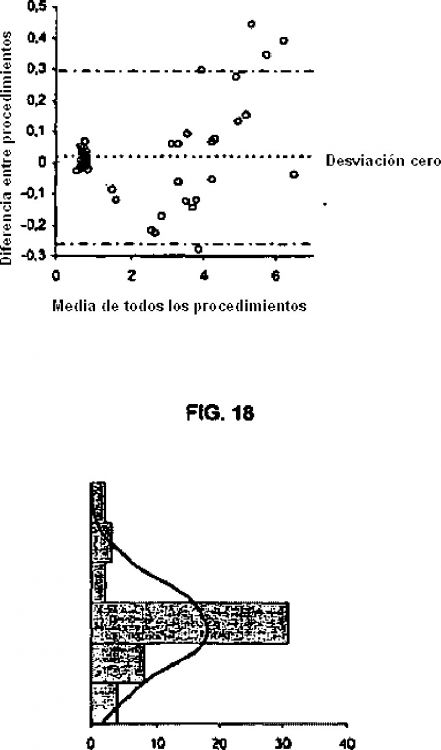
Fragmento de la descripción:
Inmunoensayo turbidimétrico para evaluar Cistatina C humana.
La presente invención se refiere a un inmunoensayo turbidimétrico mejorado para evaluar Cistatina C humana en una muestra líquida del cuerpo humano haciendo uso de conjugados de anticuerpos-nanopartículas específicos; un procedimiento para la evaluación de la velocidad de filtración glomerular de un paciente haciendo uso de dicho ensayo: kits de reacción correspondientes; conjugados de anticuerpos-nanopartículas mejorados y su uso para el fin medico arriba mencionado.
Antecedentes de la invención
La Cistatina C se descubrió y se caracterizó en 1981 por A. Grubb y H. Lovberg [Grubb A O, y col: Proc. Natl. Acad. Sci. USA 1982; 79]. La Cistatina C fue la primera proteína descubierta de la que después se ha denominado la superfamilia de proteínas cistatinas. La superfamilia de proteínas cistatinas es un grupo de proteínas que inhibe enzimas de la cisteín proteasa. Otras funciones biológicas de Cistatina C se están investigando en la actualidad. Al contrario que otros miembros de la superfamilia de la Cistatina, la Cistatina C está presente en todos los fluidos corporales, aunque la composición total de Cistatinas diferentes varía de fluido corporal a fluido corporal, y en diferentes compartimentos [Abrahamson M, y col: J. Biol. Chem. 1986; 261: 11282]. En 1990, Abrahamsson y col. demostró que la Cistatina C se produce a una velocidad estable y por todas (o casi todas) las células nucleadas en el cuerpo humano, siendo lo que se denomina una proteína "doméstica" [Abrahamson M, y col: Biochem. J. 1990; 268: 287-94].
La Cistatina C -con una masa molecular de 13 kD- se filtra libremente a través de la membrana glomerular normal del riñón, pero después se re-adsorbe y cataboliza en el "túbulo proximal", el compartimiento de los riñones que re-adsorbe la mayor parte de los péptidos y proteínas más pequeñas que pasan la membrana glomerular. De esta forma los riñones conservan estos materiales proteináceos para el cuerpo y dificultan la perdida de la orina (Jacobsson B, y col: Histopathology 1995; 26: 559-64.) [Heyms S B, y col: Am. J. Clin. Nutr. 1983; 37: 478].
La creatinina, hasta ahora el marcador normalmente usado para la velocidad de filtración glomerular (GFR), es una molécula de bajo peso molecular producida en células musculares. Por lo tanto, la velocidad de la formación y secreción de creatinina esta muy unido a la masa muscular del cuerpo. Se sabe bien que la masa muscular de un individuo en una población varía de forma considerable. Con frecuencia, los ancianos tienen una masa muscular baja en comparación con la masa corporal, también muchos pacientes pierden masa muscular a medida que su enfermedad progresa. Por lo general los niños tienen una masa muscular relativa diferente en comparación con los adultos, y los hombres tienen por término medio una masa muscular relativa superior que las mujeres. Por lo tanto, cuando la concentración de creatinina en suero se usa como marcador para la velocidad de filtración glomerular, el valor de creatinina en suero se puede encontrar dentro del intervalo de referencia incluso cuando se produce una reducción del 50% de la velocidad de filtración glomerular. [Shemesh O, y col: Kidn. Int. 1985; 28: 830-8]. También la dieta influye de forma significativa en el nivel en suero de creatinina, en especial una dieta rica en proteínas [Perrone R D, y col: Clin. Chem. 1992; 38: 1933-53].
Las mediciones de creatinina en suero y plasma no son "procedimientos convencionales de oro" fiables para medir la velocidad de filtración glomerular. El uso de inyecciones intravenosas de sustancias marcadas con isótopos como Cr-51-EDTA o Tc-99m-DTPA, o inyecciones de agentes yodados como yohexol, ha ganado, por lo tanto, algo de popularidad. Estos procedimientos son costosos, requieren mucho tiempo y las inyecciones son necesarias, y con frecuencia tomar muestras de sangre repetidas. En la publicación "Simple Cystatin C-Based Prediction Equations for Glomerular Filtration Rate Compared with the Modification of Diet in Renal Disease Prediction Equation for Adults and the Scwartz and the Counahan-Barratt Prediction Equations for Children", de Grubb y col. en Clinical Chemistry 51:8, 1420-1431, se demostró que simples mediciones de Cistatina C en sangre pueden reemplazar complicados procedimientos para medir la velocidad de filtración glomerular.
Originalmente la medición de Cistatina C usaba procedimientos bioquímicos clásicos, pero pronto se movió a inmunoensayos turbidimétricos y nefelométricos. La compañía Dade-Behring fue la primera en aplicar procedimientos de mediciones nefelométricas. Véase también Coll, E y col. Am. J. Kidney Disease 2000; 36, 2934. Los procedimientos nefelométricos son muy fiables. La desventaja de los procedimientos nefelométricos es que los propios instrumentos tienen una velocidad de procesamiento bastante baja en comparación con espectrofotómetros automáticos basados en la transmisión de la luz. Los nefelómetros producidos por Dade Behring, típicamente el nefelómetro BNII y los nefelómetros ProSpec, y Beckman Instruments, han entrado en el mercado de forma sustancial, pero están mucho menos extendidos que los instrumentos basados en mediciones de transmisión. Los nefelómetros también tienen una transferencia de muestras mucho más baja que los grandes instrumentos automáticos basados en mediciones de transmisión.
H. Stone y col. en el artículo "Analytical performance of a particle-enhanced nephelometric immunoassay for serum Cystatin C using rate analysis", en Clinical Chemistry Vol 8, pág. 1482-85, 2001, presentaron un procedimiento nefelométrico de velocidad. Sin embargo, los instrumentos nefelométricos tienen una capacidad limitada para un gran número de muestras y el número de instrumentos nefelométricos es limitado. Por lo tanto, se solicitó moverse a instrumentos espectrofotométricos homogéneos de absorción, ya que tales instrumentos son más abundantes y tienen una capacidad superior.
Dako Cytomation, Dinamarca, ha sido pionera en el campo de inmunoensayos turbidimétricos de Cistatina C. La técnica se describe en los siguientes artículos: "Cystatin C-The marker of choice for renal function testing" de C. Schmidt en European Clinical Laboratory, 10 Feb. 2004. "New improved automated particle enhanced turbidimetric immunoassay for quantitative determination of human Cystatin C in serum and plasma" de C. Schmidt, C. Kjoller y K Gronkjaer, una presentación descargada del sitio web de Dako Cytomation AS, julio 2005.
Sin embargo, las mediciones turbidimétricas se alteran por medio de la turbidez en muestras, como se describe en el artículo "Turbidity in immunoturbidimetric assays" de Dahr y col., en Ann. Clin. Biochem. Vol 27, pág. 509, 1990. En el 29º Congreso Nórdico de Química Clínica, Malmo, Suecia, 24 al 27 de abril, 2004, A. Grubb presentó resultados en la interferencia de triglicéridos en muestras de suero y plasma en los resultados de mediciones de Cistatina C. por lo tanto todavía existe una necesidad de mejorar el inmunoensayo turbidimétrico para la Cistatina C humana.
Una alternativa a los sistemas de inmunoensayos homogéneos serían los sistemas de inmunoensayo no homogéneos basados en la separación. La ventaja de los sistemas de inmunoensayos no homogéneos se caracteriza por una etapa de separación con lavado durante la realización del ensayo. La ventaja de estos sistemas es que, por medio del lavado, eliminan cualquier sustancia que interfiere. Además, permite la eliminación de anticuerpos no unidos y enzimas no unidas y otros restos fluorescentes o de color o que proporcionen señales. Por lo general, estos procedimientos no son competitivos, ya que la sustancia que se va a medir, en lo sucesivo denominada analito, no tiene que competir con análogos marcados para la unión a los anticuerpos. Este aspecto, y el uso de las etapas de lavado, hacen posible usar anticuerpos inmovilizados y anticuerpos marcados en exceso, proporcionando una sensibilidad alta y normalmente un nivel elevado de precisión, en especial si se usan anticuerpos de gran calidad.
Existen numerosos libros de texto sobre sistemas de inmunoensayo de fase sólida y otros no homogéneos. Los grandes sistemas automáticos están disponibles en el mercado. Abbott Diagnostic Division, EE.UU., comercializa reactivos para ImX, AxSYM y otros instrumentos de inmunoensayos no homogéneos automáticos; Roche Diagnostics, Alemania, comercializa reactivos para Elecsys y otros sistemas de inmunoensayos no homogéneos; y existen otros numerosos suministradores de reactivos y sistemas de inmunoensayos no homogéneos. Un sistema de inmunoensayo...
Reivindicaciones:
1. Un inmunoensayo turbidimétrico para evaluar Cistatina C humana en una muestra líquida corporal humana por medio de:
2. Un inmunoensayo turbidimétrico para evaluar Cistatina C humana en una muestra líquida corporal humana por medio de:
3. El procedimiento de la reivindicación 1, en el que dichos anticuerpos son anticuerpos policlonales, no humanos, no roedores, contra Cistatina C humana.
4. El procedimiento de la reivindicación 3, en el que dichos anticuerpos policlonales son anticuerpos aviares contra Cistatina C humana.
5. El procedimiento de una de las reivindicaciones 3 y 4, en la que al menos el 25% en peso de dichos anticuerpos policlonales o fragmentos se han obtenido por purificación por afinidad con Cistatina C humana.
6. El procedimiento de la reivindicación 1 ó 2, en el que los anticuerpos comprenden (a) anticuerpos monoclonales que se unen a un solo epitope de Cistatina C humana o (b) un conjunto de dos o más especies de anticuerpos monoclonales, en el que cada especie de anticuerpo monoclonal se une a un epitope diferente de Cistatina C humana o dos o más especies se unen a epitopes idénticos con fuerza de unión diferente.
7. El procedimiento de la reivindicación 6, en el que los anticuerpos monoclonales son de origen no humano.
8. El procedimiento de una cualquiera de las reivindicaciones anteriores, en el que las nanopartículas recubiertas están recubiertas con una mezcla de anticuerpo de Cistatina C anti-humana y al menos una proteína inerte.
9. El procedimiento de la reivindicación 8, en el que la proteína inerte es hidrófila, en particular seleccionada de hemocianina de lapa, haptoglobina, albúminas y transferrinas.
10. El procedimiento de una cualquiera de las reivindicaciones precedentes, en el que el cambio en turbidez se mide a través del cambio en dicha absorbancia de la luz de la mezcla del ensayo a una longitud de onda en el intervalo de 500 nm a 600 nm y a una temperatura en el intervalo de 10 a 50 grados Celsius.
11. El procedimiento de una cualquiera de las reivindicaciones precedentes, en el que dicho cambio en turbidez, expresado como unidades / cm de mAb, para luz de una longitud de onda de 546 nm es
más de 15 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 30 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 75 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 37º Celsius durante 260 segundos después de formar la mezcla; o
en el que dicho cambio en turbidez, expresado como unidades / cm de mAb, para luz de una longitud de onda de 505 nm es
más de 20 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 50 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 90 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 37º Celsius durante 260 segundos después de formar la mezcla; o
para luz de de una longitud de onda de 570 nm de
más de 10 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 30 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 80 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 37º Celsius durante 260 segundos después de formar la mezcla; o
para luz de de una longitud de onda de 546 nm de
más de 12 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 25 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 70 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 32º Celsius durante 600 segundos después de formar la mezcla; o
para luz de de una longitud de onda de 546 nm de
más de 8 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 20 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 50 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 37º Celsius durante 120 segundos después de formar la mezcla; o
para luz de de una longitud de onda de 648 nm de
más de 4 unidades/cm de mAb a una concentración de 9,9 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 7 unidades/cm de mAb a una concentración de 19,8 µg de Cistatina C por l en la mezcla de ensayo, o de
más de 15 unidades/cm de mAb a una concentración de 34,1 µg de Cistatina C por l en la mezcla de ensayo,
si dicha mezcla se mantiene a 37º Celsius durante 40 segundos después de formar la mezcla.
12. Un procedimiento de acuerdo con cualquiera de las reivindicaciones precedentes, caracterizado por -cuando se construye una curva de correlación contra procedimientos nefelométricos- se obtiene un valor de ordenada en el origen de menos de 0,15 mg/l de Cistatina C para el procedimiento turbidimétrico para un valor correspondiente de 0 mg/l de Cistatina C, como se obtiene por medio del procedimiento nefelométrico; y/o
caracterizado por -cuando se construyen una curva de correlación contra procedimientos de inmunoensayo no homogéneos- se obtiene un valor de ordenada en el origen de menos de 0,25 mg/l de Cistatina C para un valor correspondiente de 0 mg/l de Cistatina C, y/o
caracterizado por tener una interferencia de 15 mmol/litro de triglicéridos en la muestra experimental de menos del 6% sobre el valor medido de Cistatina C a un nivel de 1,2 mg de Cistatina C por litro, y/o
caracterizado por tener una desviación de linealidad por debajo del 5% en un intervalo de medición de 1,32 a 7,5 mg de Cistatina C por litro, y una desviación de linealidad por debajo del 15% en la región de medición del intervalo de medición de 0,75 a 1,32 mg de Cistatina C por litro.
13. Un procedimiento de acuerdo con cualquiera de las reivindicaciones 1 a 12, caracterizado por determinar la concentración de Cistatina C de una muestra midiendo la velocidad inicial del aumento de la absorbancia, (a) registrando directamente en el momento de la mezcla, o (b) registrando brevemente después de mezclar en combinación con una extrapolación hacia atrás a la absorbancia de aumento inicial, o (c) midiendo la diferencia de absorbancia entre dos o más momentos de tiempo menos de 1 minuto después de mezclar la muestra y los reactivos.
14. Un procedimiento para la evaluación de la velocidad de filtración glomerular de un mamífero, comprendiendo dicho procedimiento la evaluación turbidimétrica de Cistatina C humana de acuerdo con cualquiera de las reivindicaciones 1 a 13.
15. Un kit de reactivos o conjunto de reactivos para la realización del procedimiento de cualquiera de las reivindicaciones 1 a 14, que comprende (a) partículas, que comprenden inmunopartículas anti-Cistatina C como se define en una de las reivindicaciones precedentes 1 a 10 en forma seca o suspendida, (b) un tampón de ensayo en forma seca o disuelta, y, opcionalmente (c) mezcla(s) de calibrador y mezcla(s) de control cada una en forma seca o disuelta.
16. El kit de la reivindicación 15, en el que las partículas y el tampón de ensayo se proporcionan en combinación en forma seca o suspendida.
17. conjugados de nanopartículas-anticuerpos de acuerdo con la definición en cualquiera de las reivindicaciones 1 a 10.
18. El uso de conjugados de nanopartículas-anticuerpos de la reivindicación 17 en un inmunoensayo para la evaluación de Cistatina C humana o en un procedimiento de diagnóstico para la evaluación de la velocidad de filtración glomerular de un mamífero; o
en un inmunoensayo para la evaluación de Cistatina C humana o en un procedimiento de diagnóstico para la evaluación de la disfunción renal.
Patentes similares o relacionadas:
PARTICULAS DE LATEX CARBOXILADAS, del 31 de Mayo de 2010, de ROCHE DIAGNOSTICS GMBH F.HOFFMANN-LA ROCHE AG: Proceso para preparar partículas de látex carboxiladas, basado en la copolimerización de un monómero monoalquenil-aromático (A) y un ácido carboxílico alifático […]
 ENSAYOS AGLUTRIMETRICOS EN SANGRE, del 9 de Abril de 2010, de ACCUMETRICS, INC: Procedimiento para determinar la presencia o el efecto de un componente en una muestra, utilizando un sistema de agregación que comprende partículas a las que […]
ENSAYOS AGLUTRIMETRICOS EN SANGRE, del 9 de Abril de 2010, de ACCUMETRICS, INC: Procedimiento para determinar la presencia o el efecto de un componente en una muestra, utilizando un sistema de agregación que comprende partículas a las que […]
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Un sustrato para inmovilizar sustancias funcionales y un método para preparar las mismas, del 15 de Julio de 2020, de Temasek Polytechnic: Un sustrato sólido que tiene compuestos dispuestos sobre el mismo, en donde se inmoviliza una molécula funcional sobre los compuestos, teniendo cada compuesto una cadena que […]
Kit de reactivos utilizado para detectar gastrina-17 y método de preparación y aplicación para el kit de reactivos, del 15 de Julio de 2020, de Shenzhen New Industries Biomedical Engineering Co., Ltd: Un kit para detectar gastrina-17, caracterizado porque comprende un componente A y un componente B, en donde el componente A es un primer […]
Análisis biológico autónomo de alta densidad, del 1 de Julio de 2020, de BioFire Diagnostics, LLC: Recipiente para realizar reacciones de amplificación en un sistema cerrado que comprende una porción flexible que tiene una serie de blísteres […]
Chip de análisis y aparato de análisis de muestras, del 1 de Julio de 2020, de Takano Co., Ltd: Un chip de análisis que comprende: un sustrato conformado sustancialmente en forma de disco; un puerto de inyección formado […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]