HEXAPEPTIDOS NO PROTEOLIZABLES INHIBIDORES DE LA GLICOPROTEINA 41 DEL VIRUS DEL SIDA.
Hexapéptidos no proteolizables inhibidores de la glicoproteina 41 del virus del sida.
La presente invención se refiere a la identificación de hexapéptidos, (D), (L) o mixtos, preferiblemente D-hexapéptidos, que inhiben in vitro la fusión de un retrovirus a una célula diana proporcionando nuevas terapias contra la infección del virus de la inmunodeficiencia humana (VIH). Se sintetizan dos D-hexapéptidos sintéticos, Gly-Gln-Ile-Asp-Glu-Val y Gly-Gln-Ile-Asp-Gln-Val, con actividad anti-gp41, que han sido desarrollados en base a su capacidad para bloquear la actividad in vitro del péptido de fusión, una secuencia absolutamente conservada entre la mayoría de cepas y aislados clínicos del VIH. Dado el grado de conservación del FP, es previsible que la emergencia de variantes resistentes a estos compuestos sea bastante remota. Además, la presente invención se refiere a la utilización de dichos D-hexapéptidos como componentes únicos o en mezclas complejas como agentes profilácticos o terapéuticos de las infecciones retrovirales, especialmente de VIH tipo 1
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200503259.
Solicitante: UNIVERSIDAD DEL PAIS VASCO (UPV/EHU)
UNIVERSIDAD DE VALENCIA.
Nacionalidad solicitante: España.
Provincia: VIZCAYA.
Inventor/es: PEREZ PAYA, ENRIQUE, NIEVA ESCANDON,JOSE LUIS, GOMARA ELENA,MARIA JOSE, LORIZATE NOGALES,MAIER, HUARTE ARRAYAGO,NEREA, MINGARRO,ISMAEL.
Fecha de Solicitud: 30 de Diciembre de 2005.
Fecha de Publicación: .
Fecha de Concesión: 15 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K38/08 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 5 a 11 aminoácidos.
- C07K7/06A
Clasificación PCT:
- A61K38/08 A61K 38/00 […] › Péptidos que tienen de 5 a 11 aminoácidos.
- A61P31/18 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para el VIH.
- C07K7/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 5 a 11 aminoácidos.
- C12N7/06 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › por tratamiento químico.
Fragmento de la descripción:
Hexapéptidos no proteolizables inhibidores de la glicoproteína 41 del virus del SIDA.
Sector de la técnica
La presente invención se refiere a la identificación de hexapéptidos, preferiblemente D-hexapéptidos, que inhiben in vitro la fusión de un retrovirus a una célula diana proporcionando nuevas terapias contra la infección del virus de la inmunodeficiencia humana (VIH). Además, la presente invención se refiere a la utilización de dichos D-hexapéptidos como componentes únicos o en mezclas complejas como agentes profilácticos o terapéuticos de las infecciones retrovirales, especialmente de VIH tipo 1.
Estado de la técnica
La epidemia de SIDA ha experimentado un rápido crecimiento en los últimos 25 años (número estimado de enfermos a finales de 2004: 39,4 millones). El uso de las terapias antirretrovirales altamente activas (HAART) ha incrementado apreciablemente la esperanza de vida de los infectados por el VIH. Sin embargo, los tratamientos de larga duración han provocado la selección de variantes del virus resistentes a las HAART. Esta situación ha impuesto el desarrollo de nuevos compuestos eficaces en combatir dichas variantes. La adición al arsenal de compuestos anti-VIH del inhibidor de la fusión "enfuvirtide" (también conocido como Fuzeon, T-20, ó DP178) ha supuesto un gran avance para el control de los virus multirresistentes (1-3).
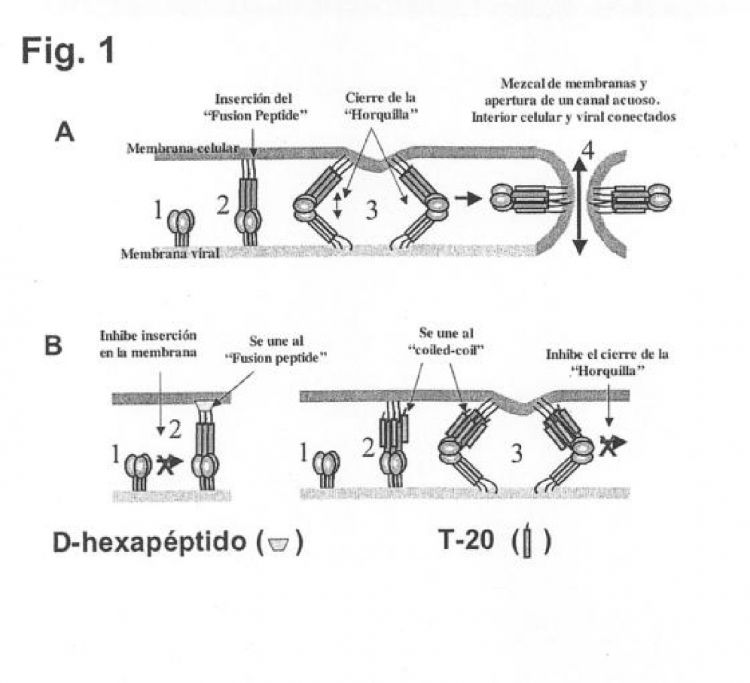
Este compuesto actúa sobre un proceso clave del ciclo infectivo: la fusión de las membranas vírica y celular promovida por la glicoproteína de la envoltura gp120/41 (4). Su principio activo es el péptido T-20 que imita una secuencia helicoidal de gp41 que empaqueta en los surcos hidrofóbicos formados en la zona de contacto entre las hélices de un "coiled-coil" trimérico imperfecto. El empaquetamiento se requiere para cerrar una horquilla que pinza las membranas y provoca su fusión. T-20 inhibe de forma competitiva el proceso de cierre de la pinza y, por tanto, inhibe la fusión (Fig. 1, panel superior).
Sin embargo, el alto coste de producción de "enfuvirtide" y la emergencia de variantes del virus resistentes a este compuesto han puesto en entredicho su utilización generalizada en la terapia del anti-VIH. Por tanto, es necesario trabajar en el desarrollo de nuevos compuestos alternativos y eficaces inhibidores de la fusión, de menor coste, y que puedan ser incluidos dentro de estrategias integradas para el control de la enfermedad. Si estos compuestos actuaran según un mecanismo diferente al del "enfuvirtide", serían utilizables de forma concertada en la eliminación de virus que hayan desarrollado resistencia a los tratamientos HAART. Además podrían representar una alternativa a las terapias de inhibición de la fusión estándar en los casos de resistencia al "enfuvirtide".
La secuencia amino-terminal de la proteína fusogénica gp41 de VIH-1, es hidrofóbica y altamente conservada entre las diferentes cepas, variantes y aislados clínicos (5). Esto es debido a que se requiere para que la proteína desempeñe la función fusogénica (revisado en 6). De acuerdo a su función, esta secuencia se denomina "péptido de fusión" (FP en lo sucesivo). Su alto grado de conservación y su funcionalidad hacen de esta secuencia una diana terapéutica adecuada para el desarrollo de inhibidores anti-gp41. Datos previos indican que determinados oligopéptidos son capaces de interferir con la actividad fusogénica de gp41 (7) así como con la interacción del FP sintético con liposomas (8).
En la solicitud de patente WO 03/104262 A2 se describen péptidos diseñados para inhibir la fusión de la proteína gp41 del VIH a células diana, así como en la solicitud de patente WO 2004/047730 A2 se describe un compuesto químico de peso molecular entre 200 y 1200 Daltons, y logP de -2.0 a +5.5, capaz de actuar recíprocamente con la cavidad hidrofóbica y bloquear la formulación de la fusión con el "coiled coil" de la gp41.
Pero todos estos métodos para tratar de prevenir la infección por VIH y de curar el SIDA aún son limitados. Por lo tanto, todavía existe la necesidad de desarrollar nuevos inhibidores virales, especialmente inhibidores que no sean tóxicos o tengan una toxicidad aceptablemente baja.
Existen diversos métodos de síntesis de péptidos que se distinguen por el estado físico de la fase en la que tiene lugar dicha síntesis, es decir en fase líquida o fase sólida (véanse por ejemplo, las solicitudes de patente WO 2005/063791 A2, WO 2005/063792 A2 y WO 2005/063793 A2). En la fase sólida, un primer aminoácido o péptido se une a un soporte insoluble, tal como una resina. Grupos sucesivos de aminoácidos o péptidos se van añadiendo hasta que se ha obtenido el péptido deseado. Entonces, dicho péptido se separa de la resina, se aísla y se identifica.
Teniendo en cuenta estos precedentes, nosotros decidimos sintetizar y aislar D-hexapéptidos (no hidrolizables por las proteasas celulares) que interfirieran con FP como posibles nuevos agentes "inhibidores de fusión" por VIH, y que funcionaran según un mecanismo diferente al de "enfuvirtide". Nuestra previsión es que estas secuencias actúan bloqueando la inserción del FP en la membrana blanco celular y/o interfiriendo con los procesos de auto-ensamblaje que ocurren en su superficie (Fig. 1, panel inferior).
Bibliografía
1. Wild, C. T., Shugars, D.C., Greenwell, T.K., McDanal, C.B., y Matthews, D.J. (1994). Peptides corresponding to a predictive alpha-helical domain of human immunodeficiency virus type 1 gp41 are potent inhibitors of virus infection. Proc. Natl. Acad. Sci. USA 91, 9770-9774.
2. Kilby, J.M., Hopkins, S., Venetta, T.M., et al. (1998) Potent supression of HIV-1 replication in humans by T-20, a peptide inhibitor of gp41-mediated virus entry. Nature Medicine 4, 1302-1307.
3. Schneider, S.E., Bray, B.L., Mader, C.J. et al. (2005). Development of HIV fusion inhibitors. J. Peptide Sci. 11, 744-753.
4. Doms, R. W., y Moore, J. P. (2000). HIV-1 membrane fusion: targets of opportunity. J. Cell Biol. 151, F9-F13.
5. Gallaher, W. R. (1987). Detection of a fusion peptide sequence in the transmembrane protein of the human immunodeficiency virus. Cell 50, 327-328.
6. Nieva J.L., y Agirre, A. (2003). Are fusion peptides a good model to study viral cell fusion? Biochim. Biophys. Acta, 1614, 104-115.
7. Owens, R.J., Tanner, C.C., Mulligan, M.J., Srinivas, R., y Compans, R.W. (1990). Oligopeptide inhibitors of HIV-induced syncytium formation. AIDS Res. Hum. Retroviruses 6, 1289-1296.
8. Pereira, F.B., Goñi, F.M., y Nieva, J.L. (1997). Membrane fusion induced by the HIV-1 fusion peptide: modulation by factors affecting gp41 activity and potential anti-HIV compounds. AIDS Res. Hum. Retroviruses 13, 1203-1211.
Descripción de la invención
En la presente invención se describe la identificación de dos D-hexapéptidos sintéticos, con actividad anti-gp41, que han sido desarrollados en base a su capacidad para bloquear la actividad in vitro del péptido de fusión, una secuencia absolutamente conservada entre la mayoría de cepas y aislados clínicos del VIH.
Dado el grado de conservación del FP, es previsible que la emergencia de variantes resistentes a estos compuestos sea bastante remota.
La presente invención consiste en la síntesis e identificación de dos D-hexapéptidos (Fig. 2, #2 y #5) como inhibidores efectivos de la actividad fusogénica de gp41. Estos péptidos han sido identificados mediante un proceso de rastreo posicional en librerías peptídicas. De hecho creemos que todos los D-hexapéptidos que resultarían de sustituir la posición 5 con cualquiera de los (D) estereoisómeros de los aminoácidos conocidos presentaría la misma actividad inhibitoria frente al VIH. La actividad de dichos péptidos se manifiesta como inhibición de la interacción de la secuencia FP con membranas y como inhibición de la facultad de fusionar células cuando gp120/41 se expresa en la superficie de las células en cultivo (Figs. 3-5). Se demuestra que los péptidos tienen secuencias de aminoácidos características ya que un péptido relacionado de secuencia parecida (con un único cambio químicamente no conservativo de residuo de aminoácido en la posición 2) no presenta actividad anti- gp41 (Figs. 2, 3)....
Reivindicaciones:
1. Hexapéptidos, destinados al tratamiento del SIDA al inhibir la actividad fusogénica de la glicoproteína viral gp 41, del VIH, caracterizados por las secuencias Gly-Gln-Ile-Asp-Glu-Val ó Gly-Gln-Ile-Asp-Gln-Val.
2. Uso de hexapéptidos caracterizados por las secuencias Gly-Gln-Ile-Asp-Glu-Val o Gly-Gln-Ile-Asp-Gln-Val para la elaboración de una composición farmacéutica destinada al tratamiento o prevención del SIDA.
3. Composición farmacéutica destinada al tratamiento o prevención del SIDA que comprende hexapéptidos caracterizados por las secuencias Gly-Gln-Ile-Asp-Glu-Val ó Gly-Gln-Ile-Asp-Gln-Val.
4. Virus VIH incapaz de infectar células humanas caracterizado porque presenta unido a la glicoproteína gp 41 un hexapéptido caracterizado por las secuencias Gly-Gln-Ile-Asp-Glu-Val ó Gly-Gln-Ile-Asp-Gln-Val produciendo, la unión del hexapéptido, la inhibición de la actividad fusogénica de la glicoproteína viral gp 41 y, por consiguiente, impidiendo la entrada del virus en la célula huésped.
Patentes similares o relacionadas:
Composiciones nutricionales que contienen un componente de péptido y sus usos, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional para su uso para reducir la incidencia de la diabetes mellitus, en donde dicha composición nutricional comprende: (i) […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Péptidos para inhibir la angiogénesis, del 15 de Julio de 2020, de The Board of Trustees of the University of Illionis: Un peptido aislado para su uso en la inhibicion de la angiogenesis en un paciente que lo necesita, en donde el peptido comprende la secuencia de aminoacidos de KFARLWTEIPTAIT […]
Péptido que tiene actividad antiinflamatoria, y uso del mismo, del 8 de Julio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en una secuencia de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2 o SEQ ID NO: 3.
Péptido que tiene actividades antiinflamatoria, osteogénica y promotora del crecimiento del cabello, y uso del mismo, del 24 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que tiene actividad antiinflamatoria, que consiste en la secuencia de aminoácidos SEQ ID NO: 2.
Combinaciones de inhibidores de puntos de control inmunitarios, del 24 de Junio de 2020, de LYTIX BIOPHARMA AS: Un compuesto que tiene la fórmula Lys Lys Trp Trp Lys Lys Trp Dip Lys, o una sal, éster o amida del mismo; para su uso en el tratamiento […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.
Péptido que tiene actividades antiinflamatoria, osteogénica y de fomento del crecimiento del pelo, y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Péptido que tiene actividad antiinflamatoria, que consiste en secuencias de aminoácidos de SEQ ID NO: 3.