HETEROCICLOS SUSTITUIDOS.
Compuestos de fórmula
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/001097.
Solicitante: INTERMED DISCOVERY GMBH.
Nacionalidad solicitante: Alemania.
Dirección: OTTO-HAHN-STRASSE 15,44227 DORTMUND.
Inventor/es: BACON, KEVIN, BENET-BUCHHOLZ, JORDI, DR., URBAHNS, KLAUS, MULLER, HARTWIG, STADLER,MARC, MAYER-BARTSCHMID,ANKE, SEIP,STEPHAN, FUCHIKAMI,KINJI, BRUNING,MICHAEL-ALEXANDER, TOGAME,HIROKO, DODO,REIKO, REINEMER,PETER, MATSUKAWA,SATOKO.
Fecha de Publicación: .
Fecha Concesión Europea: 11 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- C07D207/277 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo.
- C07D491/04 C07D […] › C07D 491/00 Compuestos heterocíclicos que contienen en el sistema cíclico condensado, a la vez uno o más ciclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo, y uno o más ciclos que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos en los grupos C07D 451/00 - C07D 459/00, C07D 463/00, C07D 477/00 ó C07D 489/00. › Sistemas orto-condensados.
- C12P17/10 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 17/00 Preparación de compuestos heterocíclicos que contienen O, N, S, Se o Te como únicos heteroátomos del ciclo (C12P 13/04 - C12P 13/24 tienen prioridad). › nitrógeno como único heteroátomo del ciclo.
- C12P17/18E
- C12R1/465 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Streptomyces.
Clasificación PCT:
- A61P35/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D207/26 C07D 207/00 […] › Pirrolidonas-2.
- C07D491/04 C07D 491/00 […] › Sistemas orto-condensados.
Clasificación antigua:
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07D207/26 C07D 207/00 […] › Pirrolidonas-2.
- C07D491/04 C07D 491/00 […] › Sistemas orto-condensados.

Fragmento de la descripción:
Heterociclos sustituidos.
La presente invención se refiere a heterociclos sustituidos, a su procedimiento de preparación y a su utilización en medicamentos, especialmente para el tratamiento de enfermedades inflamatorias, esto es asma o cáncer.
La proteinasa multicatalítica o proteasoma es una estructura celular altamente conservada que es responsable de la proteolisis ATP-dependiente de la mayoría de las proteínas celulares. El proteasoma 20S (700 kDa) contiene al menos cinco actividades proteolíticas distintas que conllevan un nuevo tipo de mecanismo que implica un residuo treonina en el sitio activo (Coux, O., Tanaka, K. y Goldberg, A. 1996 Ann. Rev. Biochem. 65:801-47).
Aunque el proteasoma 20S contiene el núcleo proteolítico, no puede degradar proteínas in vivo a no ser que se compleje con una terminación (cap) 19S en cualquiera de los extremos de su estructura, el que contiene a su vez múltiples actividades ATPasa. Esta estructura de mayor tamaño se conoce como proteasoma 26S y degrada rápidamente las proteínas que han sido el blanco de la degradación mediante la adición de múltiples moléculas del polipéptido de 8,5 kDa ubiquitina.
Ha quedado bien establecido ahora que el proteasoma es un sistema proteolítico extralisosomal principal que está involucrado en las vías de degradación, resultando en numerosas y diversas funciones celulares, tales como la división celular, procesamiento de antígenos y degradación de proteínas reguladoras de vida corta como factores de transcripción, productos oncogénicos y ciclinas (revisado en Ciechanover, A. 1994 Cell 79:13-21). La función primaria del proteasoma consiste en catalizar la proteólisis de proteínas en pequeños péptidos. Sin embargo, se ha demostrado también que la vía ubiquitina-proteasoma puede catalizar el procesamiento proteolítico regulado de un gran precursor inactivo en una proteína activa. Al respecto, el caso mejor documentado incluye la activación del factor de transcripción NF-?B (Palombella, V.J., Rando, O.J., Goldberg, A.L., y Maniatis, T. 1994 Cell 78:773-785). La forma activa del NF-?B es un heterodímero compuesto por una subunidad p65 y una p50. Esta última está presente en el citosol celular en una forma precursora inactiva, a saber p105, polipéptido de 105 kDa precursor de p50. El procesamiento proteolítico de p105 para generar p50 tiene lugar a través de la vía ubiquitina-proteasoma. Además, los p50 y p65 procesados se mantienen en el citosol como complejo inactivo con la proteína de inhibición I?B. Las señales inflamatorias activan NF-?B mediante el inicio de la vía de señalización para la degradación completa de I?B y estimulan también el procesamiento de p105 en p50. Por tanto, se necesitan dos eventos proteolíticos, ambos dirigidos por la vía ubiquitina-proteasoma, para la activación inducida por la señal de NF-?B.
Una vez activado, NF-?B se transloca hacia el núcleo, en el que desempeña un papel central en la regulación de un conjunto notablemente diverso de genes involucrados en las respuestas inmunes e inflamatorias (Grilli y col., International Review of Cytology (1993) 143:1-62). Por ejemplo, se necesita NF-?B para la expresión de diversos genes implicados en la respuesta inflamatoria, como el gen TNF-a y los genes que codifican las moléculas de adhesión celular E-selectina, P-selectina, ICAM y VCAM (Collins, T., Lab. Invest. (1993) 68:499). Se necesita también NF-?B para la expresión de un amplio número de genes de citoquinas, como IL-2, IL-6, factor estimulante de colonias de granulocitos e IFN-ß. La óxido nítrico-sintetasa inducible se encuentra también bajo el control regulador de NF-?B. Los inhibidores del proteasoma bloquean la degradación de I?Ba y la activación de NF-?B (Palombella y col., WO 95/25533 publicada el 28 de Sept., 1995; Traenckner y col., EMBO J. (1994) 13: 5433). Los inhibidores del proteasoma bloquean también la expresión TNF-a-inducida de las moléculas de adhesión de leucocitos E-selectina, VCAM-1 y ICAM-1 (Read, y col., Immunity (1995) 2:493).
El hecho de que el proteasoma desempeñe un papel crítico en la activación de NF-?B podría ser explotado clínicamente vía la utilización de inhibidores dirigidos hacia la proteólisis del proteasoma. En ciertas enfermedades, la función normal del NF-?B activo puede resultar perjudicial para la salud humana, tal como se observa en las respuestas inflamatorias. Así, los inhibidores de la activación de NF-?B, debido a su capacidad para impedir la secreción de diversas moléculas inflamatorias, tales como las moléculas de adhesión celular o citoquinas, pueden ser potencialmente útiles en el tratamiento de trastornos inflamatorios tales como aquellos que incluyen, por ejemplo, alergia, EPOC, inflamación de las vías aéreas y asma, ARDS (síndrome de distrés respiratorio agudo), SIDA, osteoartritis y artritis reumatoide; enfermedades inflamatorias del intestino, incluyendo colitis ulcerativa y enfermedad de Crohn; sepsis, rechazo de transplantes e isquemia o lesión por reperfusión, incluyendo derrame cerebral e infarto de miocardio. Debido a que la activación de NF-?B es esencial también para la angiogénesis, los inhibidores del proteasoma pueden ser útiles en el tratamiento de enfermedades asociadas a la neovascularización anormal.
En un primer momento se describió la p53 como una oncoproteína, pero se ha demostrado posteriormente que estaba involucrada en numerosos procesos celulares (revisado por Ko, L.J. and Proves, C. 1996 Genes Dev. 10, 1054-1072). Se ha demostrado que p53 induce la apoptosis en varias líneas celulares hematopoyéticas (Oren, M., 1994 Semin. Cancer Biol. 5, 221-227) mediante la acción de muchos estímulos diferentes, incluyendo lesión del ADN, infección viral y eliminación de factores de crecimiento. Sin embargo, es importante observar que la apoptosis puede ser inducida de una forma p53-independiente, por ejemplo por la acción de glucocorticoides. La inducción de p53 conduce a la detención del crecimiento celular en la fase G1 del ciclo celular, así como a la muerte celular por apoptosis. Ambas funciones permiten que p53 controle la lesión del ADN, reduciendo así la propagación de mutaciones de ADN cuando las células se dividen. La p53 secuestra las células en G1 mediante la inducción del inhibidor de la quinasa ciclina-dependiente, p21, que a su vez provoca una acumulación de la forma hipofosforilada del producto genético del retinoblastoma. Se piensa que p53 actúa como punto de verificación en la célula después de la lesión del ADN, causa en primer lugar una detención de la división celular y apoptosis. Es conocido que la degradación de p53 se realiza a través de la vía ubiquitina-proteasoma y la interrupción de la degradación de p53 es una forma posible de inducción de la apoptosis. Otra utilidad potencial de los inhibidores del proteasoma puede encontrarse en el tratamiento de enfermedades que resulten de la proliferación celular anormal.
El hecho de que la vía ubiquitina-proteasoma es crítica para la destrucción regulada de las ciclinas que dirigen la salida de la mitosis y permiten que las células progresen hacia la siguiente fase del ciclo celular está bien documentado. Por tanto, inhibiendo la degradación de las ciclinas mediante la utilización de inhibidores del proteasoma provoca la detención del crecimiento. Así, otra utilidad potencial de los inhibidores del proteasoma consiste en su utilización en el tratamiento de enfermedades que resultan de una división celular acelerada. Éstas incluyen cáncer, enfermedades cardiovasculares como miocarditis, restenosis después de la angioplastia, enfermedades renales como lupus, enfermedad poliquística renal, infecciones fúngicas, enfermedades dermatológicas como psoriasis, cicatrización anormal de heridas, queloides, enfermedades inmunológicas como autoinmunidad, hipersensibilidad aguda y retardada, enfermedad injerto contra huésped, rechazo de transplantes y enfermedades neuroinmunológicas como esclerosis múltiple y encefalomielitis aguda diseminada.
Se descubrió que varios metabolitos microbianos inhibían el proteasoma. Por ejemplo, se han indicado algunos compuestos peptídicos procedentes de estreptomicetos, tales como la serie TMS-96 (Y. Koguchi y col., J. Antibiot., 1999, 52, 63-65 y J. Antibiot., 2000, 53, 1069-1076) y hongos como la serie TMC-95 (J. Kohno y col., J. Org. Chem., 2000, 65, 990-995) como fuertes inhibidores para este objetivo. Se ha reivindicado también que los metabolitos de actinomicetos no peptídicos que poseen una porción beta-lactona o sus análogos químicos respectivos interactúan fuertemente con este objetivo. Entre ellos se encuentran las salinosporamidas provenientes...
Reivindicaciones:
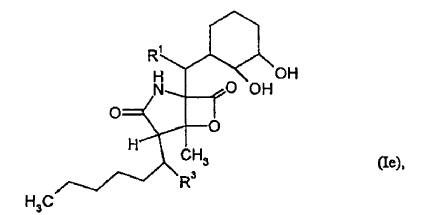
1. Compuestos de fórmula
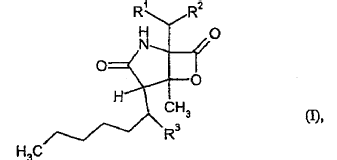
donde
R1 representa hidrógeno, hidroxi o metilcarboniloxi,
R2 representa ciclohexilo o ciclohex-2-enilo, donde el ciclohexilo puede estar sustituido con 0 a 2 grupos
R3 representa hidrógeno o hidroxi.
y sus sales, solvatos o solvatos de las sales.
2. Compuestos de fórmula (I) según la reivindicación 1, de fórmula
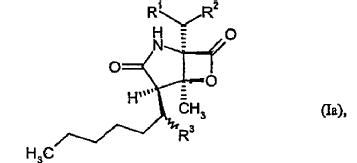
donde R1, R2 y R3 tienen el significado descrito más arriba
y sus sales, solvatos o solvatos de las sales.
3. Compuestos de fórmula (I) según la reivindicación 1, tales como
(1R,4R,5S)-1-[(S)-(1S)-2-ciclohexen-1-il(hidroxi)metil]-4-hexil-5-metil-6-oxa-2-azabiciclo[3.2.0]heptan-3,7-diona
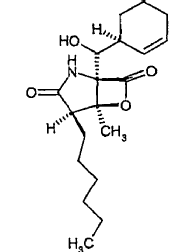
(1R,4R,5S)-1-[(S)-(1S)-2-ciclohexen-1-il(hidroxi)metil]-4-[1-hidroxihexil]-5-metil-6-oxa-2-azabiciclo[3.2.0]heptan-3,7-diona

y
(1R,4R,5S)-1-[(1R)-2-ciclohexen-1-ilmetil]-4-hexil-5-metil-6-oxa-2-azabiciclo[3.2.0]heptan-3,7-diona
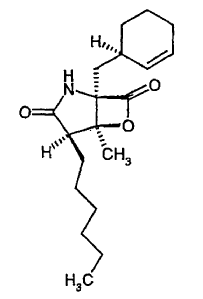
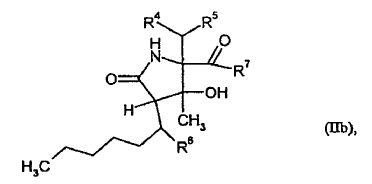
4. Compuestos de fórmula
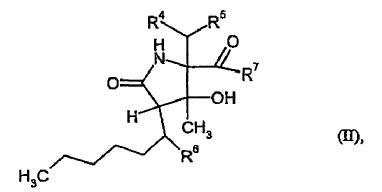
donde
R4 representa hidrógeno o hidroxi,
R5 representa ciclohexilo o ciclohex-2-enilo, donde el ciclohexilo puede estar sustituido con 0 a 2 grupos hidroxi,
R6 representa hidrógeno o hidroxi, y
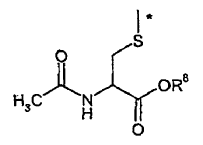
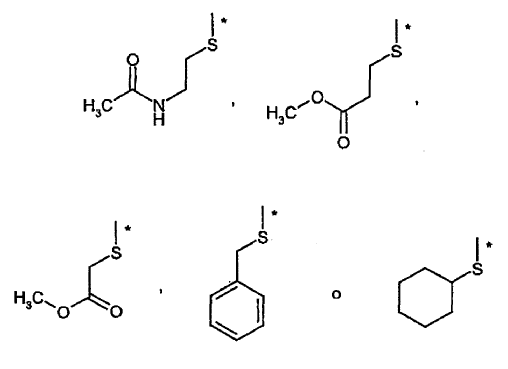
R7 representa hidroxi o un sustituyente de fórmula seleccionada de entre el grupo formado por
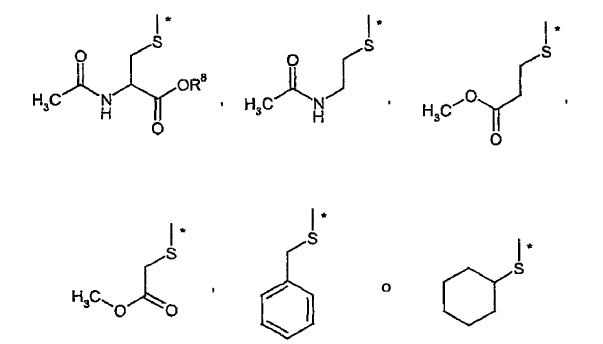
donde R8 representa hidrógeno o metilo y * representa la posición de conexión a la molécula
y sus sales, solvatos o solvatos de las sales.
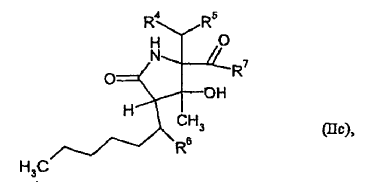
5. Compuestos de fórmula (II) según la reivindicación 4, con la fórmula
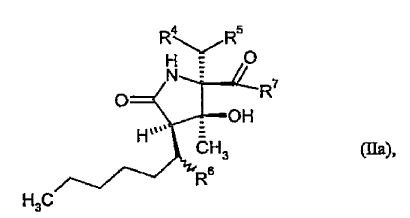
donde R4, R5, R6 y R7 tienen el significado descrito en la reivindicación 4,
y sus sales, solvatos o disolvatos de las sales.
6. Compuestos de fórmula (II) según la reivindicación 4, tales como
(3S,4R)-2-[(S)-(1S)-2-ciclohexen-1-il(hidroxi)metil]-3-hidroxi-4-[1-hidroxihexil]-3-metil-5-oxo-D-prolina

N-acetil-S-({(2R,3S,4R)-2-[(S)-(1S)-2-ciclohexen-1-il(hidroxi)metil]-4-hexil-3-hidroxi-3-metil-5-oxo-2-pirrolidinil}carbonil)cisteína
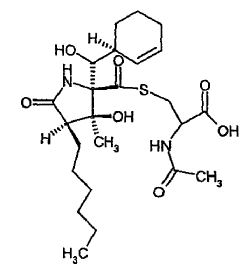
y N-acetil-S-({(2R,3S,4R)-2-[(S)-(1S)-2-ciclohexen-1-il(hidroxi)metil]-4-hexil-3-hidroxi-3-metil-5-oxo-2-pirrolidinil}carbonil)cisteinato de metilo
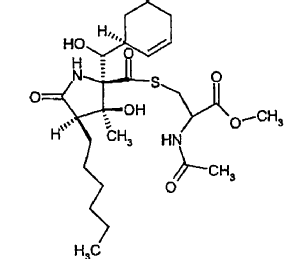
7. Procedimiento para sintetizar los compuestos de fórmula general (I) y (Ia), donde la fórmula (I) contiene los compuestos de fórmulas (Ib), (Ic), (Id) y (Ie) según la reivindicación 1 ó 2, y procedimiento para sintetizar los compuestos de fórmula general (II) y (IIa), donde la fórmula (II) contiene los compuestos de fórmulas (IIb), (IIc) y (IId) según la reivindicación 4 ó 5, caracterizado porque
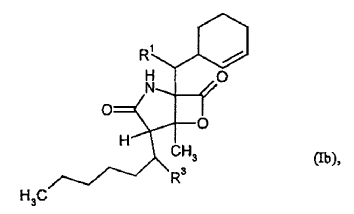
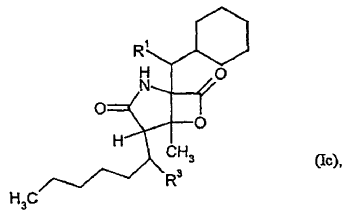
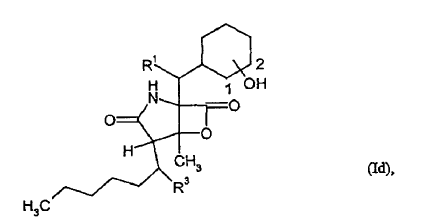
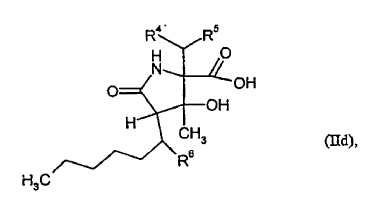
8. Composición que contiene al menos un compuesto de fórmula general (I), (Ia), (II) o (IIa) según las reivindicaciones 1 a 6 y un diluyente farmacológicamente aceptable.
9. Composición según la reivindicación 8 para el tratamiento de procesos inflamatorios agudos y crónicos o cáncer.
10. Procedimiento para la preparación de las composiciones según las reivindicaciones 8 y 9, caracterizado porque los compuestos de fórmula general (I), (Ia), (II) y (IIa) según las reivindicaciones 1 a 6 junto con los productos auxiliares habituales se llevan a una forma de aplicación apropiada.
11. Utilización de los compuestos de fórmula general (I), (Ia), (II) o (IIa) según las reivindicaciones 1 a 6 para la preparación de medicamentos.
12. Utilización según la reivindicación 11 para la preparación de medicamentos para el tratamiento de procesos inflamatorios agudos y crónicos o cáncer.
13. Compuesto según las reivindicaciones 1 a 6 para su utilización en el control de procesos inflamatorios agudos y crónicos en humanos y animales.
14. Compuesto según las reivindicaciones 1 a 6 para su utilización en el control de procesos cancerosos en humanos y animales.
15. Microorganismo con número de designación DSM 15324 y de SEQ ID NO: 1.
16. Microorganismo con el número de designación DSM 15324 y SEQ ID NO: 1 para la preparación de los compuestos de fórmulas (I), (Ia), (II) y (IIa).
Patentes similares o relacionadas:
Imidazopirazinas tricíclicas fusionadas como moduladores de la actividad de TNF, del 27 de Mayo de 2020, de UCB Biopharma SPRL: Un compuesto de fórmula (I) o un N-óxido del mismo, o una sal o un solvato farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde n representa un número […]
Nuevos compuestos antibacterianos, del 1 de Abril de 2020, de AZIENDE CHIMICHE RIUNITE ANGELINI FRANCESCO A.C.R.A.F. S.P.A.: Compuesto de fórmula: : A-L1-Y-L2-R-B en el que: A es un grupo cíclico que presenta la fórmula (II) siguiente: **(Ver fórmula)** […]
Derivados de quinazolinona como inhibidores de fosfatidilinositol 3-quinasa, del 9 de Octubre de 2019, de GILEAD SCIENCES, INC.: Un compuesto que tiene la estructura de Fórmula (I):**Fórmula** en donde: X, Y y Z se seleccionan independientemente de C(R') y N, en donde al menos uno […]
Derivados tetracíclicos activos como plaguicidas con sustituyentes que contienen azufre, del 18 de Septiembre de 2019, de SYNGENTA PARTICIPATIONS AG: Un compuesto de fórmula I,**Fórmula** en donde A1 representa S, O o NCH3; A2, A3, A4 y A5, independientemente entre sí, representan CR3 o N; […]
6H-isocromeno[3,4-c]piridinas y benzo[c][1,7]naftiridin-6-(5H)-onas como inhibidores de la cinasa asociada a adaptador 1 (AAK1), del 22 de Mayo de 2019, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I)**Fórmula** o una sal farmacéuticamente aceptable del mismo, en donde: X se selecciona entre O y NR5; R1 y R2 se seleccionan independientemente […]
Proceso para la producción de compuestos de triprenilfenol, del 8 de Mayo de 2019, de TMS Co., Ltd: Un método de producción de un compuesto de triprenilfenol de Stachybotrys microspora, comprendiendo el método: en primer lugar, cultivar un hongo filamentoso usando un medio […]
Derivados de heterociclil-butanamida, del 22 de Febrero de 2019, de MERCK PATENT GMBH: Los compuestos de la fórmula I**Fórmula** en la que W representa**Fórmula** en la que * indica el punto de unión al resto propileno, X […]
Formas cristalinas de 2-((4S)-6-(4-clorofenil)-1-metil-4H-benzo[c]isoxazolo[4,5-e]azepin-4-il)acetamida, del 13 de Febrero de 2019, de Constellation Pharmaceuticals, Inc: Forma A monohidrato cristalina de 2-((4S)-6-(4-clorofenil)-1-metil-4H-benzo[c]isoxazolo[4,5-e]azepin- 4-il)acetamida, en la que la forma cristalina está caracterizada […]