FORMULACIONES DE ANTIBIOTICO IONOFORO.
Una suspensión acuosa de al menos un antibiótico ionóforo capaz de posterior dilución,
comprendiendo dicha suspensión:
un producto molido que comprende un antibiótico ionóforo o antibióticos ionóforos molido con al menos los siguientes agentes de dispersión:
(i) un glicol y
(ii) al menos uno de un lignosulfonato y un poliglucósido, en la que el antibiótico ionóforo o antibióticos ionóforos tienen un tamaño de partícula media menor de 20 µm (micrómetros), y
al menos agua y un agente de suspensión seleccionado entre goma xantano y goma guar
Tipo: Resumen de patente/invención. Número de Solicitud: W0100290NZ.
Solicitante: ELI LILLY & COMPANY( NZ) LIMITED.
Nacionalidad solicitante: Nueva Zelanda.
Dirección: 9 GLADDING PLACE,MANUKAU CITY, AUCKLAND SOUTH.
Inventor/es: AGNEW, KIM, EWING, MELVILLE, HEWITT,WILLIAM,AUSTIN, HANHAM,CRAIG,RICHARD, PURDY,KEVIN,GRANT.
Fecha de Publicación: .
Fecha Concesión Europea: 26 de Agosto de 2009.
Clasificación Internacional de Patentes:
- A61K47/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
- A61K47/34 A61K 47/00 […] › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K47/36 A61K 47/00 […] › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00Z6
- A61K9/14H4
- A61K9/14H6
Clasificación PCT:
- A61K47/10 A61K 47/00 […] › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
- A61K47/34 A61K 47/00 […] › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K47/36 A61K 47/00 […] › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/14 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
Clasificación antigua:
- A61K47/10 A61K 47/00 […] › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
- A61K47/34 A61K 47/00 […] › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K47/36 A61K 47/00 […] › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/14 A61K 9/00 […] › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
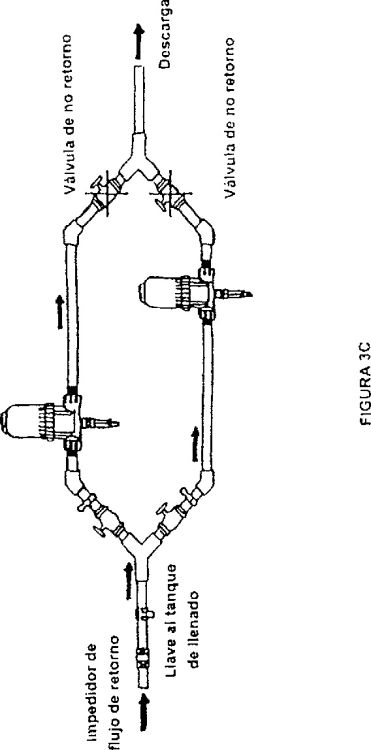
Fragmento de la descripción:
Formulaciones de antibiótico ionóforo.
La presente invención se refiere a composiciones antibióticas ionóforas y particularmente, pero no solamente, a composiciones antibióticas ionóforas capaces de dilución en agua, adecuadas para inclusión directamente o mediante un tanque de suministro en el agua de bebida de un animal para administrar y/o auto administrar, un antibiótico ionóforo o antibióticos ionóforos.
Antecedentes
La administración de antibióticos ionóforos tal como monensina a animales (preferiblemente rumiantes) es conocida que logra ventajas en dosificaciones apropiadas, en un cierto número de fines diferentes. Estos incluyen el tratamiento o prevención de cetosis y/o hinchamiento, el incremento de la producción de leche, incremento de contenido de proteína de leche en leche, incremento de la fijación de minerales, incremento de la ganancia de peso, y/o incremento de la eficacia de conversión del pienso (en rumiantes), ventajas de reproducción deseables y como un substituto de la leche. Véase Patente de EE.UU. 3.829.557.
A este respecto, los presentes inventores se remiten a la Memoria Descriptiva de la Patente Europea 0 139 595 A2 de KOFFOLK (1949) LTD, la cual se refiere a una composición antibiótica ionófora líquida para rumiantes y aves, en donde el antibiótico se disuelve en un disolvente orgánico soluble en agua no tóxico en lugar de un disolvente orgánico soluble en agua y, durante su uso, la solución resultante se mezcla con un pienso líquido, un concentrado de vitamina líquido o agua de bebida. Se sugiere estabilidad en reposo.
La composición de la EP 0 139 595 indica que, debido a que la monensina y su sal sódica es solo ligeramente soluble en agua, esta generalmente se administra en una forma seca en un pienso animal y/o en composiciones de reemplazo de leche líquida seca. Se indica igualmente ser cierto lo anterior para otro antibiótico ionóforo, lasolacid, el cual se informa en la Patente de EE.UU. 3.715.372 que es completamente insoluble en agua.
La composición de la EP 0 139 595 usa como un disolvente orgánico para el antibiótico ionóforo un disolvente seleccionado entre el grupo comprendido por propileno glicol, glicerol, etanol e isopropanol y mezclas de los mismos.
El Ejemplo 1 de la EP 0 139 595, indica que se mezclaron 250 g de un micelio que contenía monensina al 10% a temperatura ambiente con 1250 cm3 de propileno glicol durante 2 horas mediante exposición de la mezcla a ultrasonidos. Se da una indicación de que se encontró el 50% de la monensina en solución en el propileno glicol.
La monensina se encuentra usualmente disponible comercialmente como la sal sódica del ácido. La monensina sódica se encuentra disponible en dos formas, fundamentalmente una forma cristalina o una forma micelial. La forma micelial tiene únicamente aproximadamente un 20% de actividad, en tanto que la forma cristalina tiene más del 90% de monensina sódica activa.
La referencia dada en la presente memoria a la "monensina" en los casos que el contexto lo permite, abarca todas las formas de la misma, incluyendo monensina, sales de metales alcalinos de monensina y ésteres de monensina e incluye mezclas. Lo mismo es de aplicación para los otros antibióticos ionóforos.
En la Memoria Descriptiva de la Patente de Nueva Zelanda de los presentes inventores 272574/272940(equivalente a la PCT/NZ96/00068, WO 97/03650), los autores divulgamos un concentrado de suspensión de base acuosa de un antibiótico ionóforo o antibióticos ionóforos tal como monensina.
En un aspecto, en la NZ 272574/272940, dicha invención se define como un concentrado de suspensión de base acuosa de un antibiótico ionóforo o antibióticos ionóforos capaces de dilución acuosa (si se desea) y capaces (con o sin dicha dilución acuosa) de ser administrados oralmente a un animal mediante un régimen de dosificación activo (por ejemplo, mediante inyección), comprendiendo o incluyendo dicho concentrado
(I) al menos un antibiótico ionóforo en
(II) un sistema acuoso que contiene
El antibiótico ionóforo preferido de NZ 272574/272940 es monensina sódica. Preferiblemente está presente un agente o agentes anticongelantes en el cual el antibiótico(s) ionóforo no es más que escasamente (tal como glicol o poliglicol). Adicionalmente, está presente preferiblemente un agente anti-espuma (por ejemplo, simeticona y un vehículo en partículas tal como dióxido de silicio para eso).
La NZ 272574/272940 divulga igualmente un procedimiento de inyección de un animal con un antibiótico ionóforo este tipo, el cual implica la administración oralmente a tal animal de una forma diluida de las composiciones, siendo dicha dilución con agua.
Los presentes inventores han encontrado que el monopropileno glicol es un pobre disolvente de la monensina. Aunque en la NZ 272574/272940 los inventores nos hemos referido al monopropileno glicol como que es un agente anticongelante en el cual el antibiótico ionófero es escasamente soluble, los autores estimamos que dicha solubilidad hasta el grado referido en el Ejemplo 1 de la EP 0 13 595, puede lograrse cuando se induce con ultrasonidos o calentamiento.
La forma de monensina cristalina usada para los ejemplos en la NZ 272574/272940 tiene un tamaño de partícula media del orden de aproximadamente 40 µm (micrómetros) y, con el fin de mantener dichas grandes partículas en suspensión, se ha requerido para tal fin de un sistema soporte agresivo.
Así, a pesar de las avances representados por la invención divulgados en la NZ 272574/272940 (que proporciona composiciones útiles para un sistema activo de administración de antibióticos ionóforos a rumiantes), y a pesar de las afirmaciones de la EP 0 135 595, continúa siendo una necesidad substancial composiciones que contengan antibióticos ionóforos que sean inherentemente pobremente solubles o insolubles en sistemas con base acuosa, adecuados para administraciones de sistemas pasivos a rumiantes. Dichas composiciones deben, para evitar una sobre-dosificación o dosificación tóxica, permanecer substancialmente homogéneas durante períodos prolongados de tiempo.
La presente invención investiga alternativas a dichos sistemas agresivos y está dirigida a una composición dosificable capaz de dispersión de manera estable en forma de una suspensión en agua de bebida altamente diluida para animales.
La presente invención se basa tanto en un tamaño de partícula media más pequeña preferida del antibiótico ionóforo, como en un régimen asociado que incluye procedimientos de fabricación relacionados, usos, etc.
La presente invención reconoce igualmente, inter alia, los beneficios terapéuticos, de energía y productividad en los cuales la monensina o cualquier otro antibiótico ionóforo adecuado (véase el listado en la memoria descriptiva de nuestra memoria descriptiva de patente anteriormente mencionada, y más adelante) para ser usada como un tratamiento en abrevadero.
Sistemas de tratamiento en abrevadero
Actualmente se conocen tres tipos de sistema de tratamiento en abrevadero para agua de bebida para animales no usados hasta ahora con un antibiótico ionóforo.
Existen en uso tres tipos:
1. Sistemas...
Reivindicaciones:
1. Una suspensión acuosa de al menos un antibiótico ionóforo capaz de posterior dilución, comprendiendo dicha suspensión:
un producto molido que comprende un antibiótico ionóforo o antibióticos ionóforos molido con al menos los siguientes agentes de dispersión:
en la que el antibiótico ionóforo o antibióticos ionóforos tienen un tamaño de partícula media menor de 20 µm (micrómetros), y
al menos agua y un agente de suspensión seleccionado entre goma xantano y goma guar.
2. La suspensión de acuerdo con la reivindicación 1, en la que el antibiótico ionóforo o antibióticos ionóforos tienen un tamaño de partícula media menor de 5 µm (micrómetros).
3. La suspensión de acuerdo con la reivindicación 1 o la reivindicación 2, en la que el antibiótico ionóforo o antibióticos ionóforos están en la forma cristalina.
4. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en la que el antibiótico ionóforo es monensina.
5. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en la que el glicol es un líquido.
6. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en la que el glicol es monopropileno glicol.
7. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en la que el producto molido comprende un poliglucósido.
8. La suspensión de acuerdo con la reivindicación 7, en la que el poliglucósido es alquil poliglucósido.
9. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 8, en la que el producto molido comprende un lignosulfonato.
10. La suspensión de acuerdo con una cualquiera de las reivindicaciones 1 a 9, en la que el producto molido comprende además un agente anti-espuma.
11. Un procedimiento de formación de una suspensión acuosa de al menos un antibiótico ionóforo capaz de posterior dilución, comprendiendo dicho procedimiento:
la molienda de un antibiótico ionóforo o antibióticos ionóforos con al menos los siguientes agentes de dispersión:
en el que el antibiótico ionóforo o antibióticos ionóforos están reducidos a un tamaño de partícula media menor de 20 µm (micrómetros) y la molienda es en condiciones soportadas por un líquido, y
formulación posterior de la suspensión con al menos agua y un agente de suspensión seleccionado entre goma xantano y goma guar.
12. El procedimiento de acuerdo con la reivindicación 11, en el que el antibiótico ionóforo o antibióticos ionóforos están reducidos a un tamaño de partícula media menor de 5 µm (micrómetros).
13. El procedimiento de acuerdo con la reivindicación 11 ó 12, en el que el antibiótico ionóforo o antibióticos ionóforos están en la forma cristalina.
14. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a 13, en el que el antibiótico ionóforo es monensina.
15. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a 14, en el que el glicol es un líquido.
16. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a 15, en el que el glicol es monopropileno glicol.
17. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a16, en el que la molienda se realiza en presencia de un poliglucósido.
18. El procedimiento de acuerdo con la reivindicación 17, en el que el poliglucósido es alquil poliglucósido.
19. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a 18, en el que la molienda se realiza en presencia de un lignosulfonato.
20. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 11 a 19, en el que la molienda es en la presencia de un agente anti-espuma.
Patentes similares o relacionadas:
Uso de cannabinoides en el tratamiento de convulsiones atónicas en el síndrome de Lennox-Gastaut, del 29 de Julio de 2020, de GW Research Limited: Cannabidiol (CBD) para su uso en el tratamiento de las convulsiones en el síndrome de Lennox-Gastaut en el que el CBD está en forma de un extracto de cannabis […]
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Potenciador de la conservación, del 29 de Julio de 2020, de DSM IP ASSETS B.V.: Una composición tópica que comprende fitantriol y eritrulosa.
Reducción de tejido adiposo, del 22 de Julio de 2020, de Dobak, John, Daniel: Una formulacion farmaceutica inyectable que comprende: (i) polidocanol en una cantidad del 0,5 % p/v al 2,0 % p/v; e (ii) un alcohol C3-C6 en una cantidad del […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Preparaciones de hidrogel térmico reversible para su uso en el tratamiento de trastornos del urotelio, del 15 de Julio de 2020, de UroGen Pharma Ltd: Una composición de hidrogel termorreversible mucoadhesiva biocompatible que incorpora toxina botulínica y que comprende al menos un agente de gelificación […]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Composición calmante para animales que comprende al menos un ácido graso y nepetalactona, del 15 de Julio de 2020, de VIRBAC: Composición calmante para mamíferos no humanos, que comprende entre 1% y 50% en peso/peso de al menos un ácido graso que comprende entre 5 […]