DIMEROS DE CICLODEXTRINAS Y SUS DERIVADOS, SUS PROCEDIMIENTOS DE PREPARACION Y SU UTILIZACION EN PARTICULAR PARA LA SOLUBILIZACION DE SUSTANCIAS FARMACOLOGICAMENTE ACTIVAS.
Compuesto que responde a la fórmula general siguiente:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FR2004/002998.
Solicitante: CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS)
UNIVERSITE JOSEPH FOURIER
CONSEJO SUPERIOR INVESTIGACIONES CIENTIFICAS (CSIC)
UNIVERSIDAD DE SEVILLA.
Nacionalidad solicitante: Francia.
Dirección: 3, RUE MICHEL-ANGE,75794 PARIS CEDEX 16.
Inventor/es: DEFAYE, JACQUES, GOMEZ GARCIA,MARTA, ORTIZ MELLET,CARMEN, GARCIA FERNANDEZ,JOSE MANUEL, BENITO,JUAN,M, YU,JIAN-XIN.
Fecha de Publicación: .
Fecha Concesión Europea: 11 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- A61K47/40 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Ciclodextrinas; Sus derivados.
- C08B37/00M2B
Clasificación PCT:
- A61K47/40 A61K 47/00 […] › Ciclodextrinas; Sus derivados.
- C08B37/16 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › C08B 37/00 Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21). › Ciclodextrina; Sus derivados.
Clasificación antigua:
Fragmento de la descripción:
Dímeros de ciclodextrinas y sus derivados, sus procedimientos de preparación y su utilización en particular para la solubilización de sustancias farmacológicamente activas.
La presente invención se refiere a nuevos derivados dímeros de ciclodextrinas, así como a sus procedimientos de preparación. La presente invención se refiere asimismo a la utilización de estos nuevos derivados para la solubilización de sustancias farmacológicamente activas en un medio acuoso.
Las ciclodextrinas, o ciclomaltooligosacáridos, son unos oligosacáridos cíclicos que son conocidos por su aptitud para incluir en su cavidad unas moléculas diversas, de tamaño adaptado al de la estructura hospedante. El carácter generalmente apolar de estas asociaciones conduce a incluir preferentemente unas estructuras moleculares de tipo hidrófobo, permitiendo en particular la solubilización en el agua y los medios biológicos de compuestos poco o nada solubles en estos medios, y eventualmente mejorar su estabilización. Estas propiedades se utilizan actualmente en particular para el transporte de medicamentos.
La solubilidad relativamente baja en agua de las ciclodextrinas, y en particular de la más accesible de ellas en el plano económico, la ß-ciclodextrina (18 g/l, es decir 15 mmol/l, a 25ºC) limita sin embargo su utilización con este objetivo. Por otro lado, como las ciclodextrinas no poseen ninguna capacidad de reconocimiento frente a receptores biológicos en el organismo, estas entidades no se pueden utilizar para el apuntado y la vectorización de principios activos.
Para remediar este hecho establecido, las ciclodextrinas han sido modificadas químicamente para mejorar su solubilidad en el agua por un lado y, por otro lado, para incorporar en su estructura unas señales de reconocimiento celular. De esta forma, las solicitudes internacionales WO 95/19994, WO 95/21870 y WO 97/33919, y la solicitud de patente europea EP 0 403 366 describen unos derivados de ciclodextrinas de las cuales una o más funciones alcohol primario están sustituidas con unos grupos monosacarídicos u oligosacarídicos a través de un átomo de oxígeno o de azufre, o bien a través de un grupo tiourea, así como su utilización. Estas ciclodextrinas ramificadas son en particular susceptibles de servir de hospedante para el taxol y sus derivados, en particular el Taxotère®, que son unos agentes antitumorales y antiparasitarios, tal como se describe por P. Potier en Chem. Soc. Rev., 21, 1992, p. 113-119. Se obtienen así unos complejos de inclusión, lo que permite solubilizar en el agua estos agentes antitumorales. A título de ejemplo, la solubilidad en el agua del Taxotère® que es de 0,004 g/l, y puede ser aumentada hasta 6,5 g/l mediante la adición de 6I-S-a-maltosil-6I-tiociclomaltoheptaosa a su suspensión acuosa, tal como se describe en el documento WO 95/19994.
El documento EP-A-0 605 753 describe unos complejos de inclusión del taxol utilizando unas ciclodextrinas ramificadas tales como las maltosil-ciclodextrinas, para aumentar la solubilidad de este diterpeno en el agua.
Unos derivados de ciclodextrinas que comprenden uno o varios sustituyentes glicosilo o maltosilo unidos a la ciclodextrina mediante un átomo de azufre son descritos asimismo por V. Lainé et al. en J. Chem. Soc., Perkin Trans., 2, 1995, p. 1479-1487. Estos derivados han sido utilizados para solubilizar un agente antiinflamatorio tal como la prednisolona.
El documento WO 97/33919 describe los procedimientos de preparación de las tioureido-ciclodextrinas mediante el acoplamiento de las 6I-amino-6I-desoxiciclodextrinas o también de los derivados peraminados correspondientes con unos isotiocianatos de alquilo o unos mono- u oligosacáridos.
La incorporación de sustituyentes glucídicos sobre las ciclodextrinas conduce a unos derivados dotados de una solubilidad en el agua mucho más elevada si se la compara con la ciclodextrina de partida. Al mismo tiempo, este enfoque permite conferir a la ciclodextrina una afinidad particular para ciertos sitios biológicos, puesto que los sustituyentes glucídicos son bien conocidos como marcadores de reconocimiento celular. Así, este tipo de modificación de la ciclodextrina puede permitir el apuntado y la vectorización de una sustancia activa incluida en la cavidad de la ciclodextrina.
La afinidad de un marcador glucídico para un receptor específico de membrana celular (lectina) es por regla general baja. Para alcanzar unas afinidades útiles para el apuntado y la vectorización, se debe prever una presentación múltiple y simultánea del ligando. En el caso de derivados de ciclodextrinas monosustituidas en posición alcohol primario (es decir, unas ciclodextrinas en las que sólo uno de los grupos OH de la corona de los alcoholes primarios está sustituido), este problema puede ser parcialmente resuelto mediante la incorporación de estructuras glicodendríticas, tal como se describe por I. Baussanne et al. en Chem. Commun, 2000, p. 1489-1490 y por J. M. Benito et al. en Chem. Eur. J., 2003, en prensa. Sin embargo, el procedimiento de preparación de dichos compuestos es complicado.
Por otro lado, los resultados recientes descritos por I. Baussanne et al. en Chem Bio Chem 2001, p. 777-783 muestran que los derivados de la ß-ciclodextrina que comprenden unos sustituyentes de tipo glicosiltioureido, obtenidos a partir de la per-(C-6)-amina correspondiente, no muestran una afinidad suficiente frente a unas lectinas complementarias. Sin embargo, la capacidad de solubilización de estos derivados frente a agentes antitumorales de la familia del paclitaxel, tal como el docetaxel (Taxotère®) siegue siendo más baja que la observada en el caso de los derivados de las ciclodextrinas monosustituidas en posición alcohol primario.
En todos los ejemplos comentados de derivados de ciclodextrinas mono- o polisustituidas, se observa que la proporción molar de ciclodextrina:agente antitumoral solubilizado en el agua es significativamente inferior a 1:1. De hecho, la presencia de dos ciclos aromáticos en los derivados del Taxol y del Taxotère®, susceptibles de inclusión en la cavidad hidrófoba de la ciclodextrina, permite suponer un carácter ditópico para estas moléculas y, en consecuencia, una tendencia a la formación de complejos de tipo sándwich con los derivados de ciclodextrinas.
El documento D1 (WO 90/02141 A) se considera como representativo del estado de la técnica más próximo de las reivindicaciones 1 a 20 y describe unas ciclodextrinas unidas entre sí por el átomo de carbono en posición 6 de una de sus unidades glucosa (figuras 7B, 8A-D). Estas ciclodextrinas unidas son útiles para formar unos complejos con unas moléculas de principio activo que poseen dos sitios apolares o hidrófobos. El complejo así constituido es más soluble y más estable que el formado a partir de una ciclodextrina no unida (páginas 18-21, párrafo C. Linked Cyclodextrins
). Las dos ciclodextrinas pueden estar unidas mediante cualquier tipo de unión covalente; están preferentemente unidas entre sí por un grupo que forma dos uniones de tipo amina, amida, éter y/o éster. La longitud del grupo de unión puede ser variable con el fin de adaptarse al tamaño de las moléculas de principio activo a complejar. Uno de los procedimientos de preparación de estas ciclodextrinas unidas consiste en hacer reaccionar unas 6A-amino-6A-desoxi-beta-ciclodextrinas con un diéster m-nitrofenilo de ácido succínico. Un segundo procedimiento consiste en hacer reaccionar unos derivados tosilados de ciclodextrinas (6A-O-toluensulfonil ciclodextrinas) con una sal de ácido dicarboxílico (ácido succínico, glutárico, tereftálico).
En la actualidad, no existe ningún derivado de ciclodextrinas obtenido mediante un procedimiento simple, que permita aumentar la solubilización de sustancias ditópicas farmacológicamente activas y que presenten asimismo una afinidad suficiente frente a los receptores biológicos complementarios.
Uno de los objetivos de la presente invención es proporcionar nuevos derivados de ciclodextrinas dímeras que comprenden dos sub-unidades de ciclodextrina unidas en posición alcohol primario, que presentan no sólo un interés para la solubilización de las sustancias activas, en particular de los antitumorales de la familia del taxol tal como el Taxotère®, sino también una fuerte afinidad frente a los receptores membranarios específicos, lo que permite prever por medio de los mismos un transporte eficaz y selectivo de la sustancia ditópica activa hacia unos órganos dianas.
Otro objetivo...
Reivindicaciones:
1. Compuesto que responde a la fórmula general siguiente:
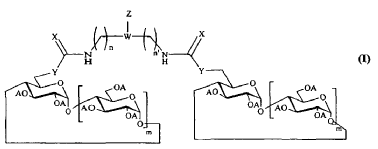
en la que:
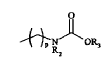
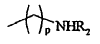

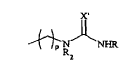

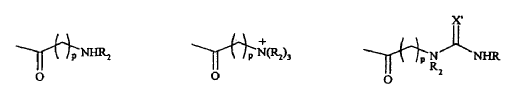
representando p un número entero comprendido entre 0 y 5, cuando W representa CH, y entre 2 y 5, cuando W representa N,
representando X' O o S,
representando R2 un átomo de hidrógeno o un grupo alquilo que comprende de 1 a 6 átomos de carbono, y siendo en particular un grupo metilo, etilo, propilo o butilo,
representando R3 un sustituyente que permite la hidrólisis del grupo carbamato con el fin de liberar la función amina, tal como los grupos terc-butilo, 9-fluorenilmetilo, bencilo, alilo o 2,2,2-tricloroetilo, y
representando R un átomo de hidrógeno, un grupo alquilo, lineal o ramificado, de 1 a 2 átomos de carbono, o un grupo aromático tal como el grupo fenilo, bencilo o naftilo, o unos derivados de estos grupos que contienen unos sustituyentes en el ciclo aromático tales como los sustituyentes metilo, etilo, cloro, bromo, yodo, nitro, hidroxilo, metoxilo o acetamido, o
representando R un elemento de reconocimiento biológico tal como un derivado de aminoácido, un péptido, un monosacárido, un oligosacárido, un elemento de multiplicación con varias ramificaciones, ramificaciones que comprenden unos grupos glucídicos que puede ser idénticos o diferentes, o también una sonda de visualización o de detección fluorescente o radioactiva.
2. Compuesto según la reivindicación 1, caracterizado porque n y n' son iguales.
3. Compuesto según la reivindicación 1 ó 2, caracterizado porque todos los grupos A representan un átomo de hidrógeno.
4. Compuesto según la reivindicación 3, caracterizado porque Y representa o bien un grupo NR1, o bien un grupo -NH-CO-(CH2)q-NR1-, o bien un grupo -S-(CH2)r-NR1-, y que responde respectivamente a una de las fórmulas siguientes:
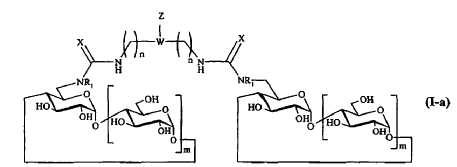
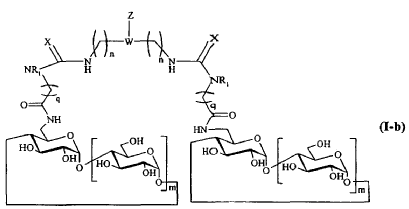
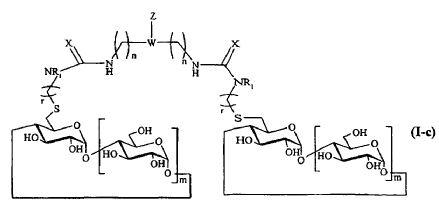
en las que n, m, q, r, X, W, Z y R1 son tal como se definen en la reivindicación 1.
5. Compuesto según la reivindicación 3 ó 4, caracterizado porque Z representa o bien un grupo -(CH2)p-NHR2, o bien un grupo -(CH2)p-N+(R2)3, o bien un grupo de fórmula
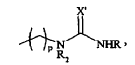
en la que X' representa un átomo de azufre, y
que responden respectivamente a una de las siguientes fórmulas:


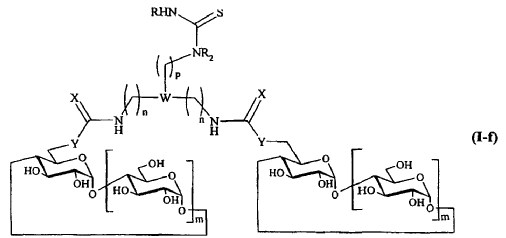
en las que n, m, p, X, W, Y, R y R2 son tal como se definen en la reivindicación 1.
6. Compuesto según cualquiera de las reivindicaciones 3 a 5, caracterizado porque W representa un átomo de nitrógeno, y porque Z representa o bien un grupo de fórmula -CO-(CH2)p-NHR2, o bien un grupo de fórmula -CO-(CH2)p-N+(R2)3, o bien un grupo de fórmula

en la que X' representa un átomo de azufre, o bien un grupo de fórmula
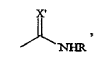
en la que X' representa un átomo de azufre, y que responde respectivamente a una de las siguientes fórmulas:
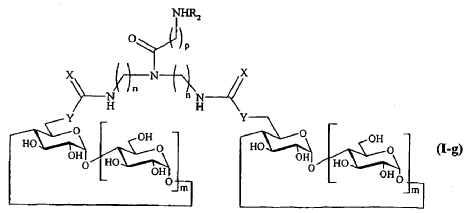
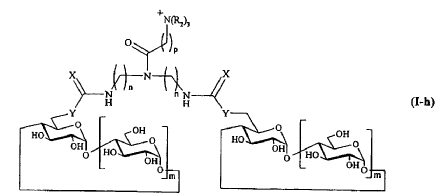
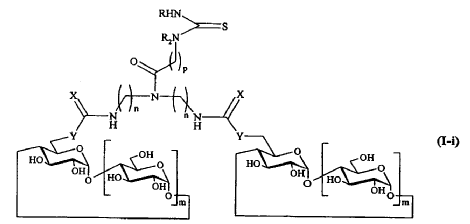

en la que n, m, p, X, Y, R y R2 son tal como se definen en la reivindicación 1.
7. Compuesto según cualquiera de las reivindicaciones 1 a 6, caracterizado porque R se selecciona de entre los siguientes grupos:

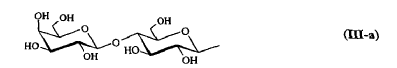
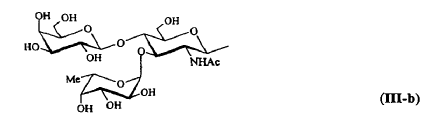
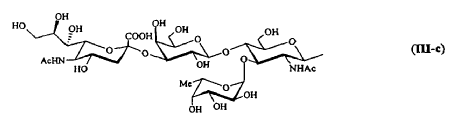
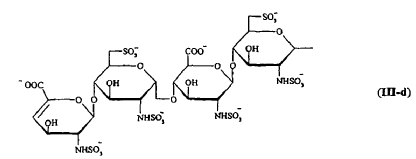
8. Compuesto según cualquiera de las reivindicaciones 1 a 6, caracterizado porque R comprende un elemento de ramificación derivado de tris(2-hidroximetil)metilamina, y representa uno de los siguientes grupos:
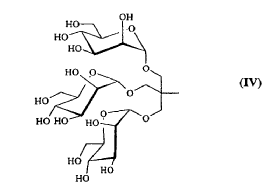
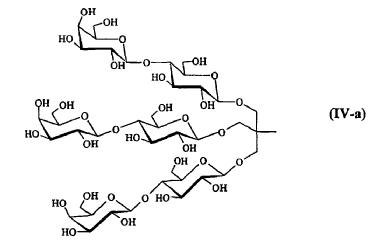
9. Compuesto según cualquiera de las reivindicaciones 1 a 6, caracterizado porque R comprende un elemento de ramificación derivado del pentaeritritol, respondiendo dicho compuesto a una de las siguientes fórmulas:

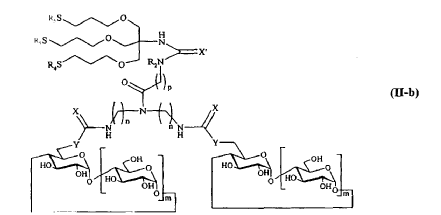
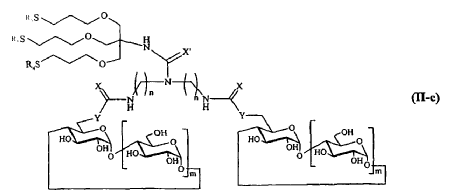
en las que m, n, p, X, X', Y son tal como se definen en la reivindicación 1, y R5 y R4 representan unos derivados glucídicos que pueden ser diferentes o idénticos o también una sonda fluorescente o radioactiva.
10. Compuesto según la reivindicación 9, caracterizado porque R5 y R4 representan uno de los siguientes grupos:
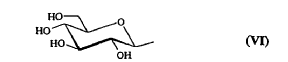
11. Compuesto según cualquiera de las reivindicaciones 1 a 6, caracterizado porque R comprende un elemento de ramificación derivado de tris(2-aminoetil)amina (TREN), respondiendo dicho compuesto a una de las fórmulas siguientes:
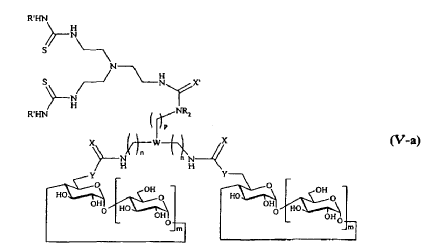
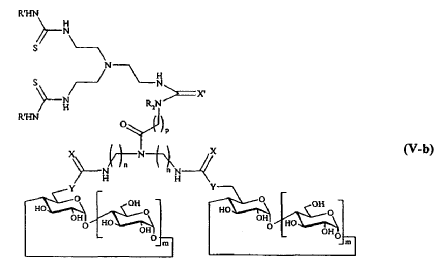
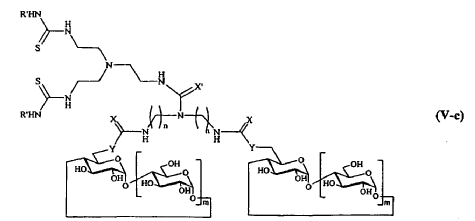
12. Compuesto según la reivindicación 11, caracterizado porque R' representa
13. Compuesto según una de las reivindicaciones 1 a 12, caracterizado porque m es igual a 6.
14. Procedimiento de preparación de un compuesto según la reivindicación 1, caracterizado porque comprende las siguientes etapas:

siendo m, A e Y tal como se definen en la reivindicación 1, y siendo A preferentemente un átomo de hidrógeno,
con un elemento de dimerización de tipo diisocianato o diisotiocianato, que contiene en particular una funcionalidad amina protegida en forma de un grupo carbamato o que contiene una funcionalidad de sal de amonio cuaternario cargada positivamente, de fórmula (VIII) siguiente:
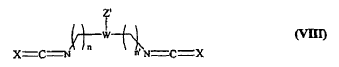
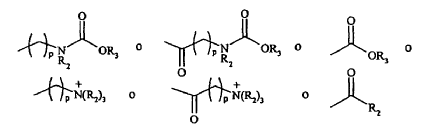
siendo p, R2 y R3 tal como se definen en la reivindicación 1, con el fin de obtener un compuesto según la reivindicación 1, que responde a la fórmula (IX) siguiente:
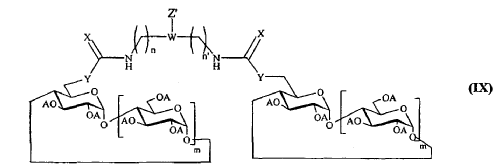
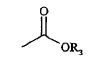
tal como se ha definido anteriormente, presente en los compuestos de fórmula (IX) mencionada anteriormente, en la que Z' contiene dicho grupo, con el fin de obtener un compuesto que contiene una funcionalidad amina libre y que responde a la fórmula (X) siguiente:
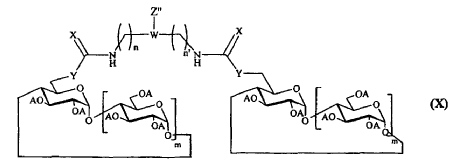
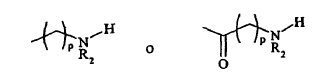
con el fin de obtener un compuesto según la reivindicación 1 que responde a la fórmula (XII) siguiente:

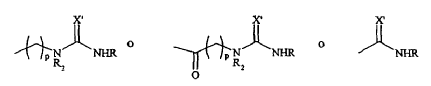
15. Complejo de inclusión de un compuesto según cualquiera de las reivindicaciones 1 a 13, con una molécula farmacológicamente activa, siendo la relación molar entre el compuesto según una de las reivindicaciones 1 a 13 y la molécula farmacológicamente activa de aproximadamente 10:1 a aproximadamente 1:2.
16. Complejo según la reivindicación 15, caracterizado porque la molécula farmacológicamente activa es una molécula ditópica, capaz de interactuar simultáneamente con dos sub-unidades de ciclodextrina, tal como una molécula que tiene dos ciclos aromáticos, como por ejemplo un derivado del Taxol, o un tamaño suficientemente grande, como por ejemplo un esteroide.
17. Complejo según cualquiera de las reivindicaciones 15 ó 16, caracterizado porque la molécula farmacológicamente activa es un agente antitumoral, que pertenece en particular a la familia del Taxol.
18. Composición farmacéutica que comprende un compuesto según cualquiera de las reivindicaciones 1 a 13, o un complejo de inclusión según una de las reivindicaciones 15 a 17, con un vehículo farmacológicamente aceptable.
19. Composición farmacéutica según la reivindicación 18, en forma de disolución acuosa.
20. Composición farmacéutica según cualquiera de las reivindicaciones 18 ó 19, caracterizada porque contiene por dosis unitaria entre aproximadamente 50 mg y aproximadamente 500 mg de uno de los compuestos según cualquiera de las reivindicaciones 1 a 13, o porque contiene por dosis unitaria entre aproximadamente 100 mg y aproximadamente 750 mg de uno de los complejos según una de las reivindicaciones 15 a 17.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
COMPOSICIÓN PARA AUMENTAR LA SOLUBILIDAD DE COMPUESTOS, del 9 de Junio de 2020, de ASÍN LLORCA, Manuel: La presente invención se refiere a una composición que comprende al menos una ciclodextrina, benzoato sódico, y sorbato potásico. La presente invención […]
Formulación farmacéutica basada en minoxidil para uso tópico y kit de la misma, del 3 de Junio de 2020, de Farmalabor S.r.l: Una disolución viscosa o formulación de gel para el tratamiento tópico de la alopecia androgenética, que comprende: - minoxidil como principio activo a una concentración […]
Método de producción de compuestos de inclusión de flavonoide, del 3 de Junio de 2020, de TAIYO KAGAKU CO., LTD.: Un método de producción de un compuesto de inclusión de flavonoide, que comprende una etapa de escisión que comprende tratar un flavonoide escasamente […]
Formulaciones transdérmicas de pergolida y utilizaciones de las mismas, del 3 de Junio de 2020, de Audevard: Formulación transdérmica de tipo sin parche para la utilización en el tratamiento de la enfermedad de Cushing equina en un equino, que comprende pergolida o una sal de la misma, […]
Formulación granular compleja con estabilidad mejorada, que comprende levocetirizina y montelukast, del 13 de Mayo de 2020, de HANMI PHARM. CO., LTD.: Una formulación granular compleja que comprende: (a) una primera parte granular que comprende levocetirizina o una sal farmacéuticamente aceptable de la misma, ciclodextrina […]
Activación de procaspasa 3 mediante terapia de combinación, del 19 de Febrero de 2020, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: Una composición que comprende: (a) un compuesto PAC-1: **(Ver fórmula)** (b) un segundo agente activo, en donde el segundo agente activo es bortezomib, […]
Complexación continua de ingredientes farmacéuticos activos, del 19 de Febrero de 2020, de Hovione Scientia Limited: Un procedimiento de preparación de un complejo de al menos una ciclodextrina y al menos un ingrediente farmacéutico activo que comprende las etapas de: a. Preparar una primera […]