CARACTERIZACION DE MOLECULAS.
Un método que comprende:
determinar un coeficiente de reparto,
asociado con, al menos, una biomolécula y una primera fase y la biomolécula y una segunda fase de un primer sistema acuoso multifásico en donde cada una de las fases primera y segunda es capaz de interaccionar con la biomolécula;
repetir dicha determinación de fases con la biomolécula en un segundo sistema acuoso multifásico que incluye al menos una fase diferente;
construir, a partir del coeficiente de reparto de la biomolécula en diferentes sistemas acuosos multifásicos, una firma de interacción, que es un conjunto de valores numéricos recogidos a partir de un conjunto de coeficientes de reparto específicos para la biomolécula;
determinar un estado de conformación de la biomolécula a partir de la firma de interacción por comparación de la firma de interacción con firmas de interacción de biomoléculas que tienen estados de conformación conocidos
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/36519.
Solicitante: ANALIZA, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 408 GLEN PARK DRIVE,BAY VILLAGE, OH 44140.
Inventor/es: CHAIT,ARNON, ZASLAVSKY,BORIS,Y.
Fecha de Publicación: .
Fecha Concesión Europea: 10 de Marzo de 2010.
Clasificación Internacional de Patentes:
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/537B
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación PCT:
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
Clasificación antigua:
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
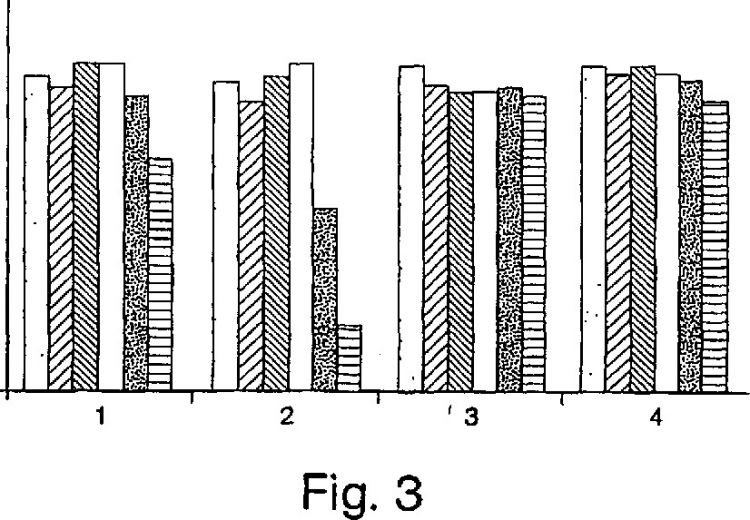
Fragmento de la descripción:
Caracterización de moléculas.
Campo de la invención
La invención se refiere en general a la caracterización de propiedades físicas y estructurales de moléculas e interacciones entre moléculas. Más particularmente, la invención se refiere al desarrollo y utilización de firmas obtenidas por reparto acuoso multifásico, que reflejan características estructurales y funcionales de biomoléculas y/o moléculas que interaccionan con biomoléculas.
Antecedentes de la invención
Esta invención se refiere en general al análisis y caracterización de biomoléculas, complejos que comprenden biomoléculas o especies análogas de las mismas. Los resultados del análisis, representados como firmas, pueden utilizarse para establecer relaciones entre propiedades de grandes números de especies, lo cual permite la selección de especies para usos específicos basados en la correlación de las propiedades de las especies que se han analizado y caracterizado utilizando los métodos de la invención.
Las biomoléculas son generalmente estructuras moleculares flexibles tridimensionales (3-D). Los miembros de una clase prototípica de biomoléculas, los polipéptidos, están constituidos normalmente por una disposición lineal de aminoácidos, es decir, comprenden secuencias de aminoácidos. La mayoría de los aminoácidos que están contenidos en los polipéptidos son los 20 aminoácidos conocidos comúnmente. En el caso de las proteínas, al igual que con otras biomoléculas, se sabe que los detalles particulares de la estructura 3-D de la proteína determinan gran parte de la información biológica específica para una biomolécula específica. Típicamente, los cambios en la estructura (conformación) 3-D están asociados con un efecto biológico específico. En este sentido, el estado de conformación de una biomolécula debe reflejar por tanto ciertos aspectos de la información biológica específica de la biomolécula.
Está reconocido en general que la información biológica de una biomolécula específica puede ser transferida a o de otra especie por interacciones no covalentes entre la biomolécula específica y la otra especie. Ejemplos de tal interacción no covalente incluyen sucesos de fijación en los cuales la fijación de una molécula más pequeña a la biomolécula induce cambios en la conformación de la biomolécula. En muchos casos, como será reconocido por los expertos en la técnica, estos cambios en la conformación de la biomolécula pueden dar como resultado cambios ulteriores en el comportamiento o las características de las biomoléculas implicadas. Estos cambios son a menudo muy importantes e incluyen cambios en cuanto a qué otras biomoléculas pueden ser fijadas por la biomolécula. Series de sucesos tales como éstos se encuentran en la raíz de muchos efectos biológicos específicos. Por tanto, el análisis de las estructuras biomoleculares presenta un interés significativo en la búsqueda de terapias eficaces y mejoras en biotecnología.
Como se practica generalmente, el análisis estructural de biomoléculas implica el examen de la estructura en varios niveles de detalle. Para las proteínas, esto incluye el análisis al nivel de secuencia de aminoácidos (estructura primaria), estructura secundaria (v.g. composición de hélice alfa o hoja beta), estructura terciaria (estructura atómica detallada en 3-D), y estructura cuaternaria (cuando la biomolécula está constituida por sub-dominios discretos). Las técnicas para evaluar cada uno de estos aspectos de la estructura son generalmente específicas para el tipo de información deseado. Por ejemplo, los métodos preferidos para determinar la secuencia primaria de una biomolécula son usualmente incapaces de proporcionar información acerca de las estructuras terciaria y las técnicas para proporcionar información estructural terciaria son inadecuadas para determinar la secuencia primaria. Fundamentalmente, los métodos e instrumentación que están disponibles para analizar la estructura de orden superior, es decir, la información de conformación, son complejos, lentos y difíciles de realizar. Esto no es sorprendente, dado que la información 3-D detallada implica, por definición, la resolución del tipo de átomos y sus coordenadas en el espacio en escala atómica. Es necesario un enfoque diferente para obtener rápidamente información estructural útil de orden superior con facilidad y sencillez.
Muchos procesos biológicos están mediados por interacciones de fijación no covalente entre una proteína y otra molécula. Ejemplos de éstos incluyen la participación de receptores, tales como los de hormonas, mensajeros y/o fármacos, y los socios de fijación para los receptores, tales como hormonas, mensajeros, fármacos y/o cualquier otro ligando. Tales interacciones y su papel en la mediación de los procesos biológicos son bien conocidos para los expertos en la técnica. Además, está reconocido generalmente que los procesos biológicos que implican la interacción de una biomolécula con otra incluyen las interacciones entre proteínas diferentes. Está reconocido también que la identificación y caracterización de las interacciones tales como las arriba descritas es de gran importancia en el proceso del descubrimiento y desarrollo de fármacos. Asimismo, está reconocido que los métodos para el análisis de las interacciones bioquímicas de fijación, particularmente para los propósitos de adquisición de ideas en lo que respecta a características estructurales, requieren demasiado tiempo y esfuerzo para poder aplicarse generalmente a números mayores de pares de fijación potencialmente relevantes o útiles.
La fijación de un receptor dado a su pareja de fijación puede detectarse por una diversidad de técnicas capaces de monitorizar los cambios en las características físico-químicas del receptor inducidas por la fijación o por las sensibles a la concentración de la pareja de fijación no fijada. Los métodos basados en el reemplazamiento por competición de un ligando específico fijado al receptor por una pareja de fijación son particularmente populares en la técnica. A menudo, el ligando de interés específico está marcado fluorescente o radiactivamente. Cuando se hace esto, la aparición del ligando en una forma libre no fijada como resultado de su reemplazamiento en el complejo con el receptor por una pareja de fijación se monitoriza fácilmente. Sin embargo, estas técnicas se ven dificultadas por el hecho de que sólo los compuestos con una afinidad para el receptor que exceda de la del ligando específico son capaces de reemplazar el ligando en cantidades significativas y permitir con ello su detección. Adicionalmente, existen problemas importantes de manipulación de residuos asociados con los métodos utilizados para hacer detectable un ligando, a saber, radiactividad y toxicidad.
En algunos casos, la fijación de un ligando es suficiente para cambiar la función de un receptor. Si ocurre esto, entonces puede utilizarse también la determinación de la fijación del ligando para determinar que la función del receptor ha cambiado también, v.g. actividad enzimática alterada o afinidad alterada para otras biomoléculas. En estos casos, la cuantificación de la fijación ligando-receptor es adecuada para cribado de compuestos capaces de afectar a la función y/o actividad del receptor. Sin embargo, un enfoque tan sencillo no siempre es adecuado o útil.
En muchos casos, la fijación de un ligando particular da como resultado una alteración específica de la actividad y/o función del receptor, en tanto que la fijación de otro ligando da como resultado una alteración específica diferente de la actividad y/o función. Estas diferencias en la respuesta a la fijación del ligando dependen de los detalles particulares de los cambios en la estructura 3-D del receptor (cambios conformacionales). Un ejemplo de esto es el efecto de diferentes compuestos estrogénicos sobre el receptor de estrógenos. En este caso, compuestos diferentes dan como resultado cambios conformacionales distintivos diferentes y estos diferentes cambios dan como resultado una actividad y/o función diferente del receptor de estrógenos. Así, cuando se somete a cribado una clase de compuestos en cuanto a su efecto sobre este receptor, o receptores con propiedades similares, cualquier medida de la afinidad del ligando para el receptor podría no proporcionar información adecuada en lo que respecta a la actividad farmacológica potencial de cualquier compuesto. Adicionalmente, la fuerza de la afinidad no está, por lo general, correlacionada con los detalles específicos de los cambios conformacionales en el receptor. Esta falta de correlación entre afinidad...
Reivindicaciones:
1. Un método que comprende:
determinar un coeficiente de reparto, asociado con, al menos, una biomolécula y una primera fase y la biomolécula y una segunda fase de un primer sistema acuoso multifásico en donde cada una de las fases primera y segunda es capaz de interaccionar con la biomolécula;
repetir dicha determinación de fases con la biomolécula en un segundo sistema acuoso multifásico que incluye al menos una fase diferente;
construir, a partir del coeficiente de reparto de la biomolécula en diferentes sistemas acuosos multifásicos, una firma de interacción, que es un conjunto de valores numéricos recogidos a partir de un conjunto de coeficientes de reparto específicos para la biomolécula;
determinar un estado de conformación de la biomolécula a partir de la firma de interacción por comparación de la firma de interacción con firmas de interacción de biomoléculas que tienen estados de conformación conocidos.
2. Un método de acuerdo con la reivindicación 1, en donde la biomolécula se proporciona en combinación con al menos una molécula auxiliar que afecta a la interacción entre la biomolécula y los sistemas acuosos multifásicos primero y segundo.
3. Un método de acuerdo con la reivindicación 2, en donde la molécula auxiliar es una pareja de fijación seleccionada de una hormona, mensajero, fármaco o ligando.
4. Un método de acuerdo con la reivindicación 3, en donde la pareja de fijación es un fármaco.
5. Un método de acuerdo con la reivindicación 1 ó 2, que comprende:
6. Un método de acuerdo con la reivindicación 5, que comprende repetir b)-d) al menos tres veces.
7. Un método de acuerdo con la reivindicación 5, en donde b) comprende:
8. Un método de acuerdo con la reivindicación 5 ó 6, en donde las fases de b) difieren en su capacidad para interaccionar con la biomolécula sobre la base de la topografía y el tipo de grupos en la biomolécula que están accesibles al disolvente.
9. Un método de acuerdo con la reivindicación 5, que comprende:
repetir a) a f), en donde la biomolécula en a) está modificada; y
comparar las firmas obtenidas para cada una de las biomoléculas.
10. Un método de acuerdo con la reivindicación 9, en donde el grupo de biomoléculas son una mezcla de biomoléculas que tienen una afinidad estructural estrecha.
11. Un método de acuerdo con la reivindicación 9, en donde el grupo de biomoléculas son una mezcla microheterogénea de biomoléculas.
12. Un método de acuerdo con la reivindicación 9, en donde el grupo de biomoléculas son biomoléculas fijadas a al menos un ligando de peso molecular bajo.
13. Un método de acuerdo con la reivindicación 9, en donde el grupo de biomoléculas son biomoléculas fijadas a otras biomoléculas.
14. Un método de acuerdo con la reivindicación 9, en donde el grupo de biomoléculas comprende proteínas fijadas a otras proteínas.
15. Un método de acuerdo con la reivindicación 9, en donde se conoce una actividad biológica de al menos una de las biomoléculas.
16. Un método de acuerdo con la reivindicación 1, comprendiendo el método:
17. Un método de acuerdo con la reivindicación 1, en donde los sistemas acuosos multifásicos primero y segundo se seleccionan del grupo constituido por sistemas polímero/polímero y sistemas polímero/sal.
18. Un método de acuerdo con la reivindicación 16, en donde los coeficientes de reparto se determinan como una función de la cantidad total de la biomolécula en el sistema para aumentar la precisión del valor del coeficiente de reparto.
19. Un método de acuerdo con la reivindicación 16, en donde cada sistema se calibra utilizando conjuntos seleccionados especialmente de compuestos de peso molecular bajo y alto que tienen coeficientes de reparto conocidos.
20. Un método de acuerdo con la reivindicación 16, en donde c) comprende medir experimentalmente la concentración de la biomolécula en un número menor que la totalidad de las fases resueltas para cada sistema y el coeficiente de reparto calculado utilizando el valor conocido para la biomolécula total presente.
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
ANTICUERPO MONOCLONAL O UNA PORCIÓN DE UNIÓN A ANTÍGENO DEL MISMO QUE SE UNE A LA PROTEÍNA L DEL VIRUS PARAINFLUENZA HUMANO (PIV); MÉTODO Y KIT PARA DETECTAR AL VIRUS PIV, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína L del virus parainfluenza humano (PIV), donde dichos […]
ANTICUERPOS MONOCLONALES ESPECÍFICOS PARA EL ANTÍGENO PB2 DEL VIRUS DE LA INFLUENZA HUMANA (FLU), SECUENCIAS NUCLEOTÍDICAS; MÉTODO Y KIT DE DIAGNÓSTICO DE INFECCIÓN PRODUCIDA POR FLU, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína PB2 del virus de la influenza humana (Flu), […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Un ensayo de la respuesta inmunológica mediada por células, del 17 de Junio de 2020, de Cellestis Limited: Un método para medir una actividad de respuesta inmunológica mediada por células, comprendiendo dicho método: (a) proporcionar una composición de incubación […]
Método de deducción de un valor de positividad de biomarcador en porcentaje para células seleccionadas presentes en un campo de visión, del 10 de Junio de 2020, de NOVARTIS AG: Método de deducción de un valor para el % de positividad de biomarcador (PBP) para todas las células u, opcionalmente, uno o más subconjuntos de las […]