PROCEDIMIENTO DE ANALISIS DE HEMOGLOBINA MEDIANTE ELECTROFORESIS CAPILAR; KIT PARA ELECTROFORESIS CAPILAR Y UTILIZACION DE RALENTIZADOR DE FLUJO EN DICHO PROCEDIMIENTO.
Procedimiento de separación de hemoglobinas en muestras biológicas mediante electroforesis capilar en solución libre (FSCE),
procedimiento en el que se hace pasar a la muestra que comprende dichas hemoglobinas por un capilar que contiene un tampón de análisis, que comprende al menos una etapa en la que se introduce la muestra en un tubo capilar que contiene una solución de al menos un tampón de análisis, caracterizado por que las hemoglobinas son hemoglobina A2 y las hemoglobinas C, D, E, S, F y/o A, y por que el tampón es de tipo zwitteriónico y se asocia a al menos un ralentizador de flujo seleccionado entre diaminas alifáticas, poliaminas alifáticas, sus derivados y sales aceptables; y sus mezclas
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05292431.
Solicitante: SEBIA.
Nacionalidad solicitante: Francia.
Dirección: PARC TECHNOLOGIQUE LEONARD DE VINCI, RUE LEONARD DE VINCI,91090 LISSES.
Inventor/es: ROBERT,FREDERIC, CLEMENT,JEAN-BAPTISTE, SIMONIN,DENIS.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Noviembre de 2005.
Fecha Concesión Europea: 30 de Junio de 2010.
Clasificación Internacional de Patentes:
- C07K14/805 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Hemoglobinas; Mioglobinas.
Clasificación PCT:
- C07K1/26 C07K […] › C07K 1/00 Procedimientos generales de preparación de péptidos. › Electroforesis.
- G01N27/447 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › utilizando la electroforesis.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
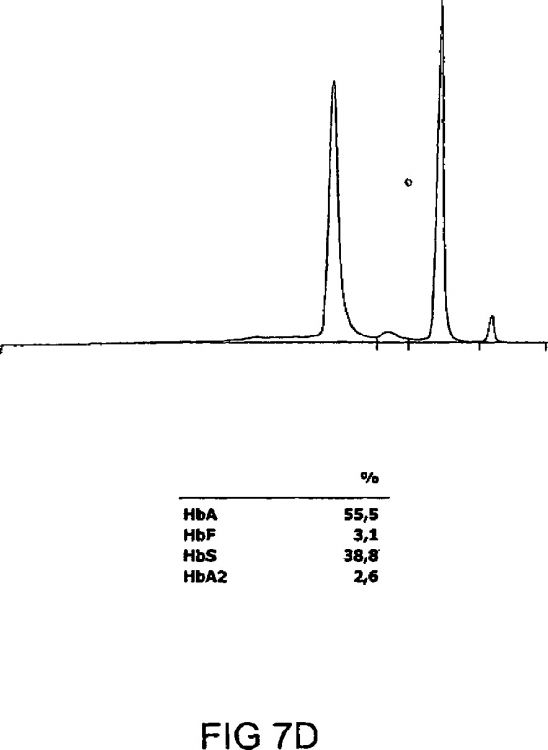
Fragmento de la descripción:
Procedimiento de análisis de hemoglobina mediante electroforesis capilar, kit para electroforesis capilar y utilización de ralentizador de flujo en dicho procedimiento.
La presente invención se refiere a un procedimiento de separación de hemoglobina mediante electroforesis capilar así como a composiciones tampón útiles para esta separación, y a kits de análisis de hemoglobina mediante electroforesis capilar.
Para analizar la hemoglobina A2 y las variantes de hemoglobina, particularmente, en los líquidos biológicos, como la sangre, con fines analíticos y particularmente de diagnóstico y para, por lo tanto, separar hemoglobinas mediante electroforesis, se conoce la utilización de técnicas de electroforesis capilar (EC). Por hemoglobinas, se entiende en este documento cualquier hemoglobina normal o no, y las variantes de estas hemoglobinas. Uno de los intereses de la electroforesis capilar se basa en el hecho de que solamente son necesarias cantidades muy pequeñas de los líquidos biológicos a analizar. Además, la separación mediante esta técnica puede ser muy rápida, en la medida en que pueden utilizarse fuertes voltajes sin que la muestra se caliente demasiado durante la separación.
De este modo, la técnica preferida es el análisis mediante isoelectrofocalización capilar (cIEF). Este método permite obtener una resolución elevada entre las diferentes formas de hemoglobina (Hempe) (7). Sin embargo, su automatización es difícil y, la necesidad de utilizar capilares revestidos, también llamados capilares recubiertos ("coated") para suprimir el flujo electro-osmótico, la hace difícilmente compatible con análisis realizados en serie.
Otra técnica llamada técnica de "doble recubrimiento dinámico" puede emplearse particularmente con los kits comercializados con el nombre de "Analis HbA2-CE kit" o "CEofix HbA2-CE kit" de Analis. Esta técnica implica un primer lavado del capilar con una solución que contiene un policatión a un pH de 4,7, seguido de un segundo lavado con un tampón de análisis que contiene un polianión, a un pH de 8,7. En este método de "doble recubrimiento" o doble revestimiento, la cantidad de cargas negativas presentes en la pared interna del capilar es aún más elevada que en un capilar desnudo, si bien el flujo electro-osmótico es aún mayor. Este método de doble recubrimiento dinámico no permite, sin embargo, la separación suficiente entre las fracciones HbA2, HbC y HbE. Esto hace al análisis cuantitativo de la fracción HbA2 imposible en presencia de fracciones HbC o HbE. Además, como las fracciones HbS y HbD tienen la misma posición electroforética, es necesario un análisis complementario en medio ácido para determinar el tipo de variante presente en la muestra. Finalmente, hay que volver a realizar el revestimiento doble entre cada análisis de muestra, lo que hace a este método pesado y difícil de emplear para ensayos a gran escala.
De acuerdo con el documento WO 97/04308, en electrocromatografía, se utilizan poliaminas libres para la separación de enantiómeros. Por otro lado, el documento US 5 447 612 describe que pueden utilizarse algunos sistemas tampón particulares para mantener los gradientes de pH requeridos en isoelectrofocalización.
Por otro lado, se han descrito separaciones de hemoglobinas en solución libre, pero éstas no responden a los criterios de precisión, de resolución o de rapidez esperados para racionalizar los análisis de las hemoglobinas en EC. El documento US 5 536 382 propone un método de análisis de los constituyentes de la muestra y describe particularmente muestras sanguíneas mezcladas previamente con un reactivo marcado específico. En FSCE, se describe el análisis de una hemoglobina glucosilada, siendo el reactivo marcado específico de la hemoglobina humana A1C. Ishoka (1) (1992) describe la separación de hemoglobinas utilizando un tampón borato (100 mM), a un pH de 9,98 en tiempos de migración del orden de 50 minutos, es decir incompatibles con el periodo de los análisis de las hemoglobinas tal como se realizan actualmente. El mismo tipo de tampón, en condiciones similares de concentración y de pH (Jenkins) (3), (4) y (5), solamente permite resoluciones insuficientes entre las fracciones HbA, HbF y HbS. Sahin (2) describe condiciones de pH más ácido, pero resultados muy insuficientes para la resolución entre las fracciones HbA, HbF, HbS y HbA2 con concentraciones (20 mM), menores de borato, o con barbital (50 mM), a un pH de 8,5, y también muy insuficientes para la resolución entre las fracciones HbA, HbS y HbA2 para el tampón Tris (1 M) a un pH de 8,0. Además, se utilizaron asociaciones de Tris/Arginina (Shihabi) (6), e incluso aunque éstas permiten la separación HbA/HbS, las fracciones HbC/HbE y HbA2 no se resolvieron. Finalmente, las patentes US 5 202 006 y US 5 439 825 que describen la utilización de barbital o de etilbarbital solamente permiten obtener resoluciones reducidas entre las principales Hb que son las HbA, HbF, HbS y HbC.
Sigue existiendo, por lo tanto, una necesidad de un método de análisis de hemoglobina y particularmente de la hemoglobina A2 que permita el análisis en una única etapa, y sin doble revestimiento, que pueda emplearse automáticamente y en serie, y que garantice una resolución satisfactoria entre las formas HbA2, HbC, HbD, HbE, HbS, HbF y HbA, particularmente.
La Solicitante ha demostrado ahora que, utilizando un tampón de análisis zwitteriónico asociado a un ralentizador de flujo, particularmente en EC en solución libre, es posible obtener una separación mejorada en gran medida de las fracciones mencionadas anteriormente, en una etapa única, evitando de este modo las separaciones complementarias, y sin doble revestimiento, lo que simplifica la realización. Preferiblemente, es un procedimiento de electroforesis capilar en solución libre el que se realiza (FSCE por Free Solution Capillary Electrophoresis).
De este modo, la presente invención se refiere a la separación mediante electroforesis capilar de hemoglobinas en muestras biológicas, procedimiento en el que se hace pasar a la muestra biológica que comprende dichas hemoglobinas por un capilar que contiene un tampón de análisis, que comprende al menos una etapa en la que se introduce la muestra en un tubo capilar que contiene una solución tampón de análisis, y en el que el tampón es de tipo zwitteriónico y está asociado a al menos un ralentizador de flujo. Esta etapa viene seguida, en general, de la separación de las hemoglobinas, mediante migración y detección de las diferentes variantes.
Como tampón zwitteriónico se utiliza, de acuerdo con la invención, un tampón zwitteriónico que tampona entre los valores de pH 8 y 10, y que comprende al menos una función amina y al menos una función ácida y al menos una función hidroxilo en posición opuesta a la función ácida. Por función ácida, se entiende en este documento la función ácido carboxílico o la función ácido sulfónico, particularmente. Este tampón zwitteriónico puede estar formado por una o dos moléculas: para el caso en el que la función amina es portada por una primera molécula sin función ácida, esta primera molécula está asociada a una segunda molécula que porta una función ácida, particularmente una función ácido carboxílico o sulfónico o tal como un aminoácido. Puede mencionarse, como ejemplo, la glicina como aminoácido.
De acuerdo con la invención, los ralentizadores de flujo son de tipo diamina o poliamina alifática o cíclica. Se seleccionan entre las diaminas o poliaminas alifáticas y/o las diaminas o poliaminas cíclicas, por ejemplo. Se prefieren las diaminas o poliaminas alifáticas. Como diamina alifática, pueden mencionarse como ejemplo 1,3-diaminopropano, 1,4-diaminobutano, 1,5-diaminopentano, 1,6-diaminohexano, N,N'-dimetil-1,6-hexanodiamina, N,N,N',N'-tetrametil-1,4-butanodiamina y sus derivados y sales aceptables. Como poliaminas alifáticas, pueden mencionarse como ejemplo dietilentriamina, espermina, tetraetilenpentamina y sus derivados y sales aceptables. Los ralentizadores de flujo pueden utilizarse en mezcla.
Como sal aceptable, pueden mencionarse las sales de clorhidrato o similares. Como derivados, pueden mencionarse por ejemplo, los derivados de los compuestos anteriores de los que uno o varios átomos de carbono de la cadena alifática se sustituye(n) con uno o varios grupos alquilo y/o uno o varios hidrógeno(s) de las aminas libres se sustitu- ye(n) con uno o varios grupos alquilo.
La solución tampón de análisis puede comprender...
Reivindicaciones:
1. Procedimiento de separación de hemoglobinas en muestras biológicas mediante electroforesis capilar en solución libre (FSCE), procedimiento en el que se hace pasar a la muestra que comprende dichas hemoglobinas por un capilar que contiene un tampón de análisis, que comprende al menos una etapa en la que se introduce la muestra en un tubo capilar que contiene una solución de al menos un tampón de análisis, caracterizado por que las hemoglobinas son hemoglobina A2 y las hemoglobinas C, D, E, S, F y/o A, y por que el tampón es de tipo zwitteriónico y se asocia a al menos un ralentizador de flujo seleccionado entre diaminas alifáticas, poliaminas alifáticas, sus derivados y sales aceptables; y sus mezclas.
2. Procedimiento de acuerdo con la reivindicación 1, caracterizado por que comprende además la separación de las hemoglobinas mediante migración y la detección de estas hemoglobinas.
3. Procedimiento de acuerdo con la reivindicación 1 ó 2, caracterizado por que la muestra es una muestra de sangre, normal o no, lavada, decantada, centrifugada o completa.
4. Procedimiento de acuerdo con una de las reivindicaciones 1 a 3, caracterizado por que la muestra es una muestra de sangre hemolizada.
5. Procedimiento de acuerdo con una de las reivindicaciones 1 a 4, caracterizado por que el tampón zwitteriónico está formado por una o dos moléculas, y comprende al menos una función amina, al menos una función ácida y al menos una función hidroxilo en posición opuesta a la función ácida.
6. Procedimiento de acuerdo con una de las reivindicaciones 1 a 5, caracterizado por que el tampón se selecciona entre Tricina, TAPS, TABS, AMPSO, Bicina o HEPBS, o la asociación de Tris, AMPD o Bis Tris Propano con un aminoácido.
7. Procedimiento de acuerdo con una de las reivindicaciones 1 a 6, caracterizado por que el tampón es Tricina.
8. Procedimiento de acuerdo con una de las reivindicaciones 1 a 7, caracterizado por que dicho ralentizador de flujo se selecciona entre 1,3-diaminopropano, 1,4-diaminobutano, 1,5-diaminopentano, 1,6-diaminohexano, dietilentriamina, espermina, N,N'-dimetil-1,6-hexanodiamina, tetraetilenpentamina, N,N,N',N'-tetrametil-1,4-butanodiamina y sus derivados o sales aceptables, y sus mezclas.
9. Procedimiento de acuerdo con una de las reivindicaciones 1 a 8, caracterizado por que dicho ralentizador de flujo se selecciona entre 1,4-diaminobutano, 1,5-diaminopentano, 1,6-diaminohexano, dietilentriamina, N,N,N',N'-tetrametil-1,4-butanodiamina y sus derivados o sales aceptables, y sus mezclas.
10. Procedimiento de acuerdo con una de las reivindicaciones 1 a 9, caracterizado por que el ralentizador de flujo es 1,4-diaminobutano.
11. Procedimiento de acuerdo con una de las reivindicaciones 1 a 10, caracterizado por que el ralentizador de flujo es 1,4-diaminobutano en forma de clorhidrato.
12. Procedimiento de acuerdo con una de las reivindicaciones 1 a 11, caracterizado por que la concentración de tampón en la solución tampón está comprendida entre 20 mM y 500 mM.
13. Procedimiento de acuerdo con una de las reivindicaciones 1 a 12, caracterizado por que la concentración de tampón en la solución tampón está comprendida entre 100 mM y 250 mM.
14. Procedimiento de acuerdo con una de las reivindicaciones 1 a 13, caracterizado por que la concentración de ralentizador de flujo en la solución tampón está comprendida entre 0,01 y 50 mM.
15. Procedimiento de acuerdo con una de las reivindicaciones 1 a 14, caracterizado por que la concentración de ralentizador de flujo en la solución tampón está comprendida entre 0,10 mM y 20 mM.
16. Procedimiento de acuerdo con una de las reivindicaciones 1 a 15, caracterizado por que la solución tampón comprende además un modificador de pH.
17. Procedimiento de acuerdo con la reivindicación 16, caracterizado por que el modificador de pH se selecciona entre hidróxido de litio, hidróxido de sodio, hidróxido de potasio, hidróxido de rubidio, hidróxido de cesio, hidróxido de francio y un hidróxido de mono-, di-, tri- o tetra-alquil amonio que tiene de 1 a 8 átomos de carbono en la parte alquilo.
18. Procedimiento de acuerdo con una de las reivindicaciones 1 a 17, caracterizado por que el capilar está desnudo.
19. Procedimiento de acuerdo con una de las reivindicaciones 1 a 18, caracterizado por que el capilar es de sílice fundida.
20. Procedimiento de acuerdo con una de las reivindicaciones 1 a 19, caracterizado por que el pH de la solución tampón de análisis está comprendido entre 8 y 10.
21. Procedimiento de acuerdo con una de las reivindicaciones 1 a 20, caracterizado por que la muestra se diluye previamente con una solución de dilución apropiada, una solución hemolizante o una solución tampón de análisis.
22. Utilización de un ralentizador de flujo seleccionado entre diaminas alifáticas, poliaminas alifáticas, sus derivados y sales aceptables, y sus mezclas, en un procedimiento de electroforesis capilar en solución libre, para separar hemoglobinas, en asociación con al menos un tampón zwitteriónico en una solución tampón, siendo las hemoglobinas, hemoglobina A2 y las hemoglobinas C, D, E, S, F y/o A.
23. Utilización de acuerdo con la reivindicación 22, en la que el tampón zwitteriónico está presente a una concentración de aproximadamente 20 a 500 mM, y el ralentizador está presente a una concentración de aproximadamente 0,01 a 50 mM.
24. Kit de análisis de hemoglobina mediante electroforesis capilar en solución libre, que comprende al menos una solución tampón de análisis que contiene (1) al menos un tampón de análisis de tipo zwitteriónico y (2) al menos un ralentizador de flujo seleccionado entre diaminas alifáticas, poliaminas alifáticas, sus derivados y sales aceptables y sus mezclas.
25. Kit de análisis de acuerdo con la reivindicación 24, caracterizado por que comprende además un modificador de pH.
26. Kit de análisis de acuerdo con la reivindicación 24 ó 25, caracterizado por que comprende además una solución hemolizante.
Patentes similares o relacionadas:
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Solución conservante para hemoproteína, y procedimiento de estabilización de hemoproteína, del 29 de Abril de 2020, de EIKEN KAGAKU KABUSHIKI KAISHA: Un procedimiento de estabilización de una hemoproteína, en el que se hace coexistir un ácido disulfónico o una de sus sales en una muestra que comprende una […]
MEDICAMENTO ÚTIL COMO SUSTITUTO SANGUÍNEO PARA TRATAR, A LA VEZ, LA ANEMIA AGUDA POR PÉRDIDA DE SANGRE Y LA INFECCIÓN BACTERIANA EN MAMÍFEROS, del 27 de Febrero de 2020, de UNIVERSIDAD AUSTRAL DE CHILE: La presente invención se refiere al uso de la hemoglobina extracelular aislada de purificada de un anélido nativo de Chile, preferentemente de la especie […]
Secreción de polipéptidos que contienen hemo, del 19 de Febrero de 2020, de Impossible Foods Inc: Método de producción de un polipéptido que contiene hemo seleccionado del grupo que consiste en una leghemoglobina, una eritrocruorina, una hemoglobina no simbiótica, […]
Elementos reguladores distales de bcl11a como dianas para la reinducción de la hemoglobina fetal, del 12 de Abril de 2019, de THE CHILDREN'S MEDICAL CENTER CORPORATION: Un método para producir una célula progenitora hematopoyética que tiene disminución del ARNm o la expresión proteica de BCL11A, el método comprende […]
Procedimiento para retirar hemoglobina no modificada de soluciones de hemoglobina reticulada que incluyen hemoglobina polimérica con aparato de tratamiento térmico de corta duración a altas temperaturas, del 21 de Febrero de 2018, de Billion King International Limited: Un procedimiento para la preparación de una composición farmacéutica que contenga un portador de oxígeno altamente purificado y termoestable, incluyendo […]
Composiciones hemoactivas y procedimientos para su fabricación y uso, del 10 de Enero de 2018, de FUSION MEDICAL TECHNOLOGIES, INC.: Material hemoactivo seco que comprende: un polímero biológicamente compatible reticulado que forma un hidrogel cuando se expone a la sangre; y un polímero […]
Composiciones de hemoglobina y métodos de uso, del 12 de Abril de 2017, de Boston Therapeutics, Inc: Un método para producir una molécula híbrida de hemoglobina, útil para formar un sustituto de sangre estable, a partir de hemoglobina contenida en una solución […]