Células huésped y procedimientos de uso.
Una cepa de Pichia modificada genéticamente, en la que la secuencia de ácido nucleico que codifica:
(i) PEP4, PRB1 y YMP1,
(ii) PEP4, PRB1 y YMP2, o
(iii) PEP4, PRB1 y YMP3
es modificada genéticamente para producir deficiencia de proteasa de al menos tres de las siguientes enzimas y/o tipo de enzima: aminopeptidasa de tipo Arg / Ala, aspartil proteasa, serín proteasa, serín proteasa secretada, serín proteasa Prb 1, aminopeptidasa de tipo Leu, en comparación con la cepa de tipo salvaje.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/025223.
Solicitante: GLAXOSMITHKLINE LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Corporation Service Company, 2711 Centreville Road, Suite 400 Wilmington, Delaware 19808 ESTADOS UNIDOS DE AMERICA.
Inventor/es: TAYLOR, ALEXANDER, H., JIN,YONG HWAN, JOWETT,JAMES D, ZHU,YUAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C12N1/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo.
PDF original: ES-2539378_T3.pdf



Fragmento de la descripción:
Células huésped y procedimientos de uso Campo de la invención La invención pertenece al campo de la ingeniería biomédica. Más particularmente, la presente invención se refiere a cepas de Pichia modificadas genéticamente y a procedimientos de producción de polipéptidos en las mismas.
Antecedentes de la invención Los polipéptidos y proteínas terapéuticas se pueden expresar en diversas células huésped, incluyendo células bacterianas, células de E. coli, células fúngicas o de levaduras, células de un microorganismo, células de insectos y células de mamíferos. Huéspedes fúngicos, tales como la levadura metiltrófica Pichia pastoris tiene claras ventajas para la expresión de proteínas terapéuticas, por ejemplo, no secreta grandes cantidades de proteínas endógenas, que tiene un fuerte promotor inducible, se puede cultivar en medios químicos definidos y puede producir altos títulos de proteínas recombinantes (Cregg y col., Mol. Biotech. 16:23-52 (2000) ) . Las levaduras y hongos filamentosos se han usado con éxito para la producción de proteínas recombinantes, tanto intracelulares y secretadas (Cereghino, J.
L. y J. M. Cregg 2000 FEMS Microbiology Reviews 24 (1) : 45 66; Harkki, A., et al. 1989 Bio-Technology 7 (6) : 596; Berka, R. M., et al. 1992 Abstr. Papers Amer. Chem.Soc.203: 121-BIOT; Svetina, M., et al. 2000 J. Biotechnol. 76 (23) : 245-251. Pichia es una célula huésped notable para la expresión de seroalbúmina humana recombinante (HSA) . Sin embargo, la expresión de otros polipéptidos terapéuticos, incluidos polipéptidos fusionados genéticamente con HSA se enfrenta a los obstáculos técnicos de la proteólisis no deseada y la glicosilación.
Las proteínas heterólogas expresadas en P. pastoris pueden contener azúcares de manosa adicionales resultantes en glicanos "ricos en manosa", así como grupos manosilfosfato que imparten una carga negativa en una proteína. Las proteínas glicosiladas, ya sea con glicanos ricos en manosa o mananos cargados tienen un alto riesgo de provocar una respuesta inmunitaria en los seres humanos (Takeuchi, Trends in Glycosci. & Glycotech., 9:S29-S35 (1997) ; Rosenfeld y col., J. Biol. Chem., 249:2319-2321 (1974) ) . Por consiguiente, sería deseable producir péptidos terapéuticos, polipéptidos y/o proteínas en sistemas de huéspedes fúngicas, de forma que patrón de glicosilación sea idéntico o al menos similar al de los seres humanos.
El documento US6051419 describe genes que influyen sobre la actividad proteolítica de Pichia. Daly et al. describen la expresión de proteínas heterólogas en Pichia (Journal of Molecular Recognition Vol. 18, No. 2, 119-138) . Los documentos WO9914347 1 y US6153424 describieron cepas de Pichia deficientes en proteasa. Gleeson et al describen la generación de cepas deficientes en proteasa y su uso en la expresión de proteínas heterólogas (Methods in Molecular Biology Vol. 103, 81-94) .
Por lo tanto, existe la necesidad de cepas de levadura, en particular cepas de Pichia que sean capaces de producir péptidos heterólogos, polipéptidos y/o proteínas con proteolisis reducida y/o glicosilación en comparación con las cepas de tipo salvaje. Además, existe la necesidad de identificar genes dentro de cepas de levadura, en particular cepas de Pichia, responsables de producir las proteínas implicadas en vías proteolíticas y de glicosilación.
Sumario de la invención La presente invención proporciona una cepa de Pichia modificada genéticamente en la que la secuencia de ácido nucleico que codifica:
(i) PEP4, PRB1 e YMP1,
(ii) PEP4, PRB1 e YMP2, o
(iii) PEP4, PRB1 e YMP3
es modificada genéticamente para producir deficiencia de proteasa de al menos tres de las siguientes enzimas y/o tipo de enzima: aminopeptidasa de tipo Arg / Ala, aspartil proteasa, serín proteasa, serín proteasa secretada, serín proteasa Prb 1, aminopeptidasa de tipo Leu, en comparación con la cepa de tipo salvaje.
Se describen cepas de Pichia modificadas genéticamente en las que al menos una secuencia de ácido nucleico que codifica un producto génico funcional y/o al menos un ácido nucleico necesario para la expresión de al menos un producto génico en dicha cepa de Pichia está modificada genéticamente, en el que dicho producto génico es responsable de la proteólisis y/o la glicosilación en dicha cepa de Pichia modificada genéticamente.
También se proporcionan en el presente documento procedimientos de producción de al menos un polipéptido heterólogo que comprende expresar dicho polipéptido heterólogo en una cepas de Pichia modificada genéticamente de la presente invención. Se describen péptidos expresados de forma heteróloga, polipéptidos y proteínas expresadas en las células huésped de la presente invención.
Se describe un polipéptido aislado que tiene al menos un 50 %, 55 %, 60 %, 65 %, 70 %, 75 %, 80 %, 85 %, 90 %, 95 %, 99 % y/o 100 % de identidad de secuencia con la SEC ID Nº 4, SEC ID Nº 6 y SEC ID Nº 8.
También se describe una cepa de células huésped genéticamente modificada en la que dicho padre de tipo salvaje parental de dicha célula huésped comprende un gen que codifica un polipéptido que tiene al menos 60 % de identidad de secuencia con las SEC ID Nº 4, 6 y 8, en la que dicho gen se modifica genéticamente en el genoma de dicha célula huésped de tal manera que el producto del gen o su actividad se reduce o se elimina en dicha célula huésped genéticamente modificada en comparación con dicha célula huésped de tipo salvaje.
Breve descripción de las figuras
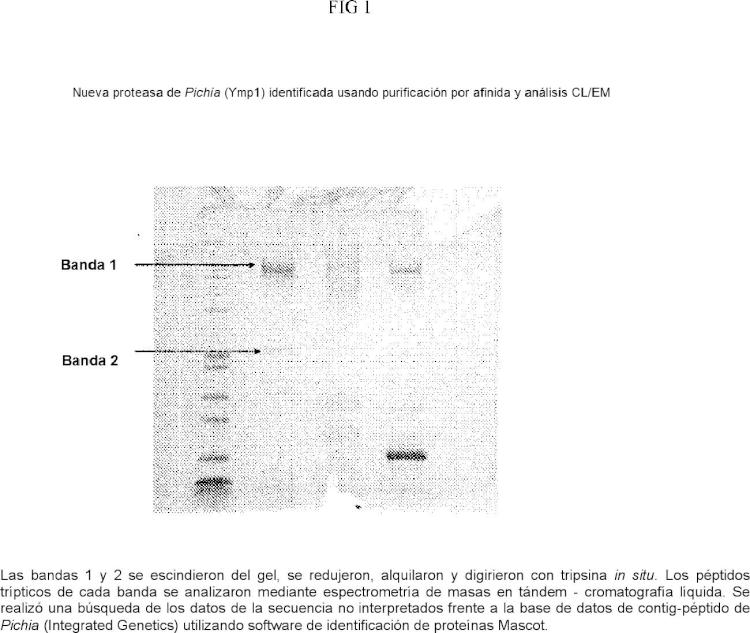
Figura 1: Nueva proteasa Ymp1 de Pichia identificada utilizando la purificación por afinidad y análisis CL/EM
Figura 2: Estructura predicha de YMP1 (SEC ID Nº 4) que muestra los aminoácidos 1-857 como la SEC ID Nº 15.
Figura 3: Ensayo de actividad de la proteasa de la cepa mutante ymp1
Figura 4: Ensayo zimográfico de la cepa mutante ymp1
Figura 5: Efecto de inactivación de ymp1 sobre la proteolisis de la proteína heteróloga (SEC ID Nº 1)
Figura 6: Efecto de inactivación de ysp2 sobre la proteolisis de la proteína heteróloga (SEC ID Nº 1)
Figura 7: Efecto de inactivación de ysp1 sobre la proteolisis de la proteína heteróloga (SEC ID Nº 1)
Figura 8: Efecto de inactivación de pep4 sobre la proteolisis de la proteína heteróloga (SEC ID Nº 1)
Figura 9: Estudio de estabilidad en tampón de las cepas mutantes ymp1, ymp3
Figura 10: Resultados del ensayo de zimoliasa par alas cepas de tipo salvaje (WT) y mutantes pmt1 y pmt4 de Pichia Figura 11: Análisis de glicosilación de proteínas heterólogas (SEC ID Nº 1) de la cepa mutante pmt4
Descripción detallada de la invención “Célula (s) huésped” como se usa en el presente documento se refiere a una célula que se ha introducido (por ejemplo, transformado, infectado o transfectado) o es capas de introducción (por ejemplo, transformación, infección o transfección) por una secuencia de polinucleótidos aislados. Las células huésped de origen de levadura y/u hongos filamentosos pueden incluir, entre otros, las siguientes familias, géneros y especies: Pichia pastoris, Pichia finlandica, Pichia trehalophila, Pichia koclamae, Pichia menabranaefaciens, Pichia methanolica, Pichia minuta (Ogataea minuta, Pichia lindneri) , Pichia opuntiae, Pichia thermotolerans, Pichi salictaria, Pichia guercum, Pichia pijperi, Pichia stiptis, Pichia sp., Saccharomyces castelii, Saccharomyces cerevisiae, Saccharomyces kluyveri, Saccharomyces sp., Hansenula polymorpha, Kluyveromyces sp., Kluyveromyces lactis, Candida albicans, Candida sp., Aspergillus fumigatus, Aspergillus nidulans, Aspergillus niger, Aspergillus or y zae, Trichoderma reesei, Chr y sosporium lucknowense, Fusarium sp., Fusarium gramineum, Fusarium venenatum, Physcomitrella patens y Neurospora crassa.
"Transformado" como se conoce en la técnica, es la modificación dirigida del genoma o apisona de un organismo a través de la introducción de ADN o ARN externo, o a cualquier otra introducción estable de ADN o ARN externo.
"Transfectada" como se conoce en la técnica, es la introducción de ADN o ARN externo en un microorganismo, incluyendo, pero no limitado a, ADN o ARN recombinante.
“Identidad”, como se conoce en la técnica, es una relación entre dos o más secuencias polipeptídicas o dos o más secuencias polinucleotídicas, según el caso, determinado comparando las secuencias. En la técnica, “identidad” también significa el grado de relación de la secuencia entre secuencias polipeptídicas o polinucleotídicas, como puede ser el caso según se determine mediante la correspondencia entre cadenas de... [Seguir leyendo]
Reivindicaciones:
1. Una cepa de Pichia modificada genéticamente, en la que la secuencia de ácido nucleico que codifica:
(i) PEP4, PRB1 y YMP1,
(ii) PEP4, PRB1 y YMP2, o
(iii) PEP4, PRB1 y YMP3
es modificada genéticamente para producir deficiencia de proteasa de al menos tres de las siguientes enzimas y/o tipo de enzima: aminopeptidasa de tipo Arg / Ala, aspartil proteasa, serín proteasa, serín proteasa secretada, serín proteasa Prb 1, aminopeptidasa de tipo Leu, en comparación con la cepa de tipo salvaje.
2. La cepa de Pichia modificada genéticamente de la reivindicación 1, en la que dicha cepa de Pichia modificada genéticamente es una forma modificada genéticamente de X-33 o SMD1163 de tipo salvaje.
3. La cepa de Pichia modificada genéticamente de la reivindicación 1 o 2, en la que dicha cepa de Pichia modificada genéticamente es una forma modificada genéticamente de Pichia pastoris, Pichia finlandica, Pichia trehalophila, Pichia koclamae, Pichia membranaefaciens, Pichia methanolica, Pichia minuta (Ogataea minute, Pichia lindneri) , Pichia opuntiae, Pichia thermotolerans, Pichia salictaria, Pichia guercum, Pichia pijperi, Pichia stiptis, Pichia sp. de tipo salvaje.
4. La cepa de Pichia modificada genéticamente de una cualquiera de las reivindicaciones 1 a 3, en la que el genoma de una cepa de tipo salvaje de dicha Pichia comprende un gen que tiene al menos un 85 % de identidad de secuencia con un gen seleccionado de las SEC ID Nº 3, 5, 7 y en la que cuando dicho gen que tiene al menos un 85 % de identidad de secuencia con las SEC ID Nº 3, 5 y 7 se deleciona, muta o rompe, dicha cepa de Pichia modificada genéticamente produce menos producto génico de dicho gen alterado que dicha cepa de tipo salvaje.
5. La cepa modificada genéticamente de una cualquiera de las reivindicaciones 1 a 3, en la que al menos una secuencia de ácidos nucleicos que codifican al menos uno del producto génico funcional siguiente o expresión de dicho producto génico está modificado genéticamente: SEC ID Nº 4, SEC ID Nº 6, y/o SEC ID Nº 8.
6. La cepa de Pichia modificada genéticamente de una cualquiera de las reivindicaciones precedentes que comprende además al menos un polinucleótido capaz de expresar al menos un polipéptido heterólogo.
7. La cepa de Pichia modificada genéticamente de la reivindicación 6, en la que dicho polinucleótido capaz de expresar al menos un polipéptido heterólogo es un vector y/o expresión episomal de un plásmido.
8. La Pichia modificada genéticamente de la reivindicación 7, en la que dicho polinucleótido capaz de expresar al menos un polipéptido heterólogo es transformada en el genoma de la Pichia.
9. La Pichia modificada genéticamente de cualquiera de las reivindicaciones 6 a 8 en la que dicho al menos un polipéptido heterólogo comprende al menos un agonista de GLP-1; o uno o más de los siguientes: al menos una proteína de unión a antígeno, al menos un dominio variable sencillo, y/o al menos un anticuerpo de dominio.
10. La Pichia modificada genéticamente de cualquiera de las reivindicaciones 6 a 8, en la que el al menos un polipéptido heterólogo tiene al menos una actividad de GLP-1.
11. La Pichia modificada genéticamente de cualquiera de las reivindicaciones 6 a 8, en la que el al menos un polipéptido heterólogo comprende al menos un fragmento y/o variante de GLP-1 humano fusionado con seroalbúmina humana.
12. La cepa de Pichia modificada genéticamente de una cualquiera de las reivindicaciones 6 a 9, en la que dicha cepa muestra una proteolisis reducida de dicho al menos un polipéptido heterólogo en dicha cepa en comparación con Pichia de tipo salvaje.
13. La cepa de Pichia modificada genéticamente de una cualquiera de las reivindicaciones 6 a 10, en la que dicha cepa muestra una glicosilación reducida o ausencia de glicosilación de dicho al menos un polipéptido heterólogo en dicha cepa en comparación con Pichia de tipo salvaje.
14. Un procedimiento de producción de un polipéptido heterólogo que comprende expresar dicho polipéptido heterólogo en una Pichia modificada genéticamente como se describe en una cualquiera de las reivindicaciones precedentes.
Las bandas 1 y 2 se escindieron del gel, se redujeron, alquilaron y digirieron con tripsina in situ. Los péptidos trípticos de cada banda se analizaron mediante espectrometría de masas en tándem -cromatografía líquida. Se realizó una búsqueda de los datos de la secuencia no interpretados frente a la base de datos de contig-péptido de Pichia (Integrated Genetics) utilizando software de identificación de proteínas Mascot.
Patentes similares o relacionadas:
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Formulación alimenticia a base de algas, productos de panadería, bollería y pastelería que la comprenden, método de obtención de la misma y su uso, del 10 de Junio de 2020, de JUAN Y JUAN INDUSTRIAL, S.L. UNIPERSONAL: Una formulación alimenticia caracterizada por que comprende microalgas frescas en forma de pasta de la especie Chlorella vulgaris, en una proporción comprendida entre el […]
Preparación de aceite microbiano que contiene ácidos grasos poliinsaturados, del 10 de Junio de 2020, de DSM IP ASSETS B.V.: Un aceite microbiano que comprende al menos el 50% de ácido araquidónico (ARA) basado en el aceite y que tiene un contenido en triglicéridos de al menos el 90%.
Microorganismo modificado para la producción optimizada de 2,4-dihidroxibutirato con eflujo de 2,4- dihidroxibutirato aumentado, del 27 de Mayo de 2020, de METABOLIC EXPLORER: Microorganismo Escherichia coli modificado genéticamente para producir 2,4-dihidroxibutirato por fermentación, en el que dicho microorganismo se […]
Cepas termoestables, productos y métodos de las mismas, del 29 de Abril de 2020, de Triphase Pharmaceuticals Pvt. Ltd: Un producto alimenticio que comprende un microorganismo termoestable de Lactobacillus, en donde el microorganismo termoestable se selecciona […]
Composición para inducir la proliferación o acumulación de células T reguladoras, del 29 de Abril de 2020, de The University of Tokyo: Composición para su uso en un método de tratamiento o prevención de una enfermedad infecciosa mediante la inducción de proliferación o acumulación […]
Métodos de cultivo semicontinuo repetido, del 5 de Febrero de 2020, de Mara Renewables Corporation: Un método de cultivo semicontinuo repetido de un microorganismo Thraustochytrid productor de aceite que comprende las etapas de: (a) proporcionar un recipiente que comprende […]