Análogos de MSH-alfa y MSH-gamma.
Péptido que consiste en de 14 a 16 restos aminoacídicos, en donde dicho péptido es un análogo de MSHα
o de MSHα que tiene la secuencia aminoacídica:
X - (aa1)n - Y - (aa2)m - Z
en donde X es una sonda aminoacídica ramificada que consiste en 3 restos de Lys que tiene la fórmula Ac-(Ac-Lys- Lys)Lys1-;
en donde (aa1)n es una secuencia aminoacídica que consiste en 4 o 5 restos aminoacídicos contiguos seleccionados del grupo que consiste en**Fórmula**y**Fórmula**
en donde Y es una secuencia aminoacídica que consiste en 4 restos aminoacídicos contiguos seleccionados del grupo que consiste en (SEQ ID n.º 16),**Fórmula**
e **Fórmula**y
en donde (aa2)m se selecciona del grupo que consiste en Gly y Asp; y
en donde Z es una secuencia aminoacídica que consiste en 2 o 3 restos aminoacídicos contiguos seleccionados del grupo que consiste en**Fórmula** y**Fórmula** .
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E13189492.
Solicitante: TXP Pharma GmbH.
Nacionalidad solicitante: Suiza.
Dirección: Schmiedgasse 2 6370 Stans SUIZA.
Inventor/es: BOESEN,THOMAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/685 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › alfa-melanotropina.
PDF original: ES-2538702_T3.pdf
Fragmento de la descripción:
Análogos de MSH-alfa y MSH-gamma Campo de la invención La presente invención se refiere a análogos peptídicos de las melanocortinas existentes o nativas naturales 5 melanotropina α (MSHα) y melanotropina γ (MSHγ) o variantes de las mismas, y su uso en el tratamiento de las afecciones inflamatorias y/o isquémicas.
Antecedentes de la invención Cada uno de los péptidos nativos melanotropina α (MSHα) y melanotropina γ (MSHγ) se sabe que son el agonista nativo de los receptores de melanocortinas de tipo 1 (MC1r) , de tipo 3 (MC3r) , de tipo 4 (MC4r) y de tipo 5 (MC5r) .
Los MCr pertenecen a la clase de los receptores acoplados a proteínas G. Todos los subtipos de los receptores se acoplan a una proteína G estimuladora, lo que significa que la estimulación del receptor implica el incremento de la producción de AMPc. La corticotropina (ACTH) es el ligando nativo del receptor de tipo 2 (MC2r) .
Los receptores de melanocortinas de tipo 1 (MC1r) y/o de tipo 3 (MC3r) se expresan en las células inmunocompetentes, entre ellas monocitos, macrófagos, neutrófilos, linfocitos T y células dendríticas. La estimulación del MCr1 y/o del MC3r está asociada a la modulación de una respuesta inflamatoria que incluye la atenuación de la producción de citocinas y la activación de los efectos prorresolución.
Los MCr se fijan a diferentes péptidos de MSH con diferente selectividad; la MSHα se fija con una alta afinidad al MC1r y con una afinidad un poco menor a MC3r, MC4r y MCr5. La afinidad de fijación de la MSHγ por el MC1r y el MC5r es débil, la fijación al MC4r es algo mejor y la fijación al MC3r es aún más alta (J. Med. Chem. 2005, 48, 1839
1848) . Se ha descrito que el MC2r se fija sólo a la ACTH, pero no a ninguno de los péptidos de MSH. Por consiguiente, la MSHα se puede considerar que es un agonista de todos los MCr, mientras que la MSHγ muestra selectividad por el MC3r.
La hipoxia (isquemia) y las lesiones por reperfusión son factores importantes en la fisiopatología humana. Los ejemplos de hipoxia de tejidos que predisponen a una lesión durante la reperfusión incluyen el choque circulatorio, la isquemia de miocardio, el accidente cerebrovascular, la isquemia renal temporal, la cirugía mayor y el trasplante de órganos. Ya que las enfermedades debidas a la isquemia son causas extremadamente frecuentes de morbimortalidad, y ya que el trasplante de órganos es cada vez más frecuente, se necesitan enormemente para mejorar la salud pública unas estrategias de tratamiento con capacidad para limitar las lesiones por reperfusión.
La fisiopatología que subyace a la isquemia/lesiones por reperfusión es compleja e implica no sólo una respuesta inflamatoria clásica a la reperfusión con la infiltración de neutrófilos, sino también la expresión de genes de citocinas que incluyen el factor α de la necrosis tumoral (TNF-α) , interleucina (IL) 1β, IL-6, IL-8, interferón γ y molécula 1 de adhesión intercelular (ICAM-1) dentro del tejido u órgano reperfundido. Además, se ha sugerido que el TNF-α producido localmente contribuye a la disfunción orgánica posisquémica, como en el corazón posinfarto, mediante el descenso directo de la contractilidad y la inducción de la apoptosis.
Debido a la naturaleza compleja de la isquemia y/o de las lesiones por reperfusión, los conceptos simples del tratamiento antiinflamatorio han resultado ser ineficaces. Por lo tanto, la mayoría de los estudios experimentales apuntan al hecho de que para proteger frente a las lesiones por reperfusión se necesita la interacción concomitante con más de una de las vías activadas.
Se ha demostrado que las melanocortinas tienen capacidad antiinflamatoria, antioxidativa y antiapoptósica, y que estimulan los efectos prorresolución, tales como la capacidad de los macrófagos para fagocitar los neutrófilos apoptósicos. El tratamiento con las hormonas nativas o los análogos conocidos de las mismas ha demostrado algunos efectos beneficiosos en modelos animales de isquemia/reperfusión y en la insuficiencia orgánica inducida por inflamación. Los análogos conocidos de las MSH incluyen uno o dos aminoácidos en la conformación D (estereoisómero D) y la adición de una sonda inductora estructural (SIE) en el extremo amino que consiste en, p. ej.,
6 restos consecutivos de lisina (Lys6) .
La solicitud de patente internacional WO 2007/022774 y Holder J. R. et al., Medicinal Research Reviews, 24, 325356 (2004) se refieren a los péptidos modificados con restos de polilisina sin ramificar.
Compendio de la invención La presente invención da a conocer análogos peptídicos de la MSHα y de la MSHγ que comprenden la secuencia 50 aminoacídica de la MSHα o de la MSHγ de humano, o variantes específicas de las mismas, en la parte del extremo carboxilo del péptido, y una sonda aminoacídica ramificada (SAR) en la parte del extremo amino del péptido. Estos reciben en conjunto en la presente memoria el nombre de análogos de la MSHα o de la MSHγ.
En un caso, los péptidos de acuerdo con la presente invención tienen una o varias propiedades mejoradas, por ejemplo, respecto a la fijación y/o activación de uno o varios de los receptores de melanocortinas, tales como MC1r y/o MC3r.
En algunos casos, los análogos de MSH que se dan a conocer en la presente memoria tienen una o varias propiedades mejoradas en comparación con el péptido nativo. Por ejemplo, en algunos casos, los análogos de la MSH que se dan a conocer en la presente memoria tiene mejorada la fijación a uno o varios de los receptores de melanocortinas, tales como MC1r y/o MC3r. En algunas realizaciones, los análogos de MSH que se dan a conocer en la presente memoria tienen mejorada la activación de uno o varios de los receptores de melanocortinas, tales como MC1r y/o MC3r.
Así pues, la presente invención se refiere a péptidos específicos que comprenden una modificación de la sonda aminoacídica ramificada o SAR en la parte del extremo amino del péptido y que comprende todo o al menos parte de la secuencia aminoacídica de la MSHα, de la MSHγ o una variante de las mismas.
En la presente memoria se describen péptidos que consisten en de 8 a 22 restos aminoacídicos que comprenden la secuencia aminoacídica:
X – (aa1) n–Y – (aa2) m–Z
en donde X comprende una sonda aminoacídica ramificada que tiene un primer resto de lisina (Lys1) seleccionado de Lys y D-Lys, en donde dicho primer resto de lisina está unido mediante un enlace peptídico a (aa1) n,
dicho primer resto de lisina está opcionalmente unido mediante enlaces peptídicos a un segundo resto de lisina (Lys2)
o a un segundo y un tercer resto de lisina (Lys3) para formar una cadena lineal de un total de 2 o 3 restos de lisina 20 seleccionados de Lys y D-Lys,
en donde la una o varias cadenas laterales de uno o más de cada uno de los dichos primer, segundo y/o tercer resto de lisina están modificados por la unión al grupo ε-amino de dicho uno o más de cada uno de dichos restos de lisina, de una molécula seleccionada independientemente del grupo que consiste en Lysq-Lys; (aa3) p-Lysq; Lysq- (aa3) p; [ (aa3) -Lys]p y [Lys- (aa3) ]p, en donde q es un número seleccionado de 0, 1, 2 y 3; p es un número seleccionado de 1,
y 3, y (aa3) es un resto aminoacídico seleccionado independientemente de Arg, His, Gly y Ala,
con la condición de que X consiste en de 2 a 9 restos de aminoácido,
en donde Y comprende una secuencia aminoacídica que consiste en 4 restos aminoacídicos contiguos seleccionados del grupo que consiste en His-Phe-Arg-Trp (SEQ ID n.º 16) ; His- (D-Phe) -Arg-Trp; His-Phe- (D-Arg) -Trp; His-Phe-Arg- (D-Trp) ; His- (D-Phe) -Arg- (D-Trp) ; His-NaI-Arg-Trp e His- (D-NaI) -Arg-Trp; y
en donde Z comprende una secuencia aminoacídica que consiste en 2 o 3 restos aminoacídicos contiguos seleccionados del grupo que consiste en Lys-Pro-Val; Lys-Pro- (D-Val) ; Arg-Phe-Gly; Arg- (D-Phe) -Gly; Arg-Phe y Arg- (D-Phe) ; y
en donde n es un número seleccionado de 0, 1, 2, 3, 4 y 5, y (aa1) puede ser independientemente cualquier resto aminoacídico natural o no natural, y
en donde m es 0 o 1, y (aa2) puede ser cualquier resto aminoacídico natural o no natural.
En un caso, (aa1) n es una secuencia que consiste en 4 o 5 aminoácidos contiguos (n = 4 o 5) y se selecciona del
grupo que consiste en (SEQ ID n.º 17) ,
(SEQ ID n.º 18) , (SEQ ID n.º 19) , (SEQ ID n.º 20) y (SEQ ID n.º 21) .
En un caso, (aa2) m es 1 aminoácido (m = 1) y se selecciona... [Seguir leyendo]
Reivindicaciones:
1. Péptido que consiste en de 14 a 16 restos aminoacídicos, en donde dicho péptido es un análogo de MSHα
o de MSHγ que tiene la secuencia aminoacídica: X – (aa1) n– Y – (aa2) m – Z
en donde X es una sonda aminoacídica ramificada que consiste en 3 restos de Lys que tiene la fórmula Ac- (Ac-LysLys) Lys1-; en donde (aa1) n es una secuencia aminoacídica que consiste en 4 o 5 restos aminoacídicos contiguos seleccionados
del grupo que consiste en (SEQ ID n.º 17) ,
(SEQ ID n.º 18) , (SEQ ID n.º 19) ,
(SEQ ID n.º 20) y (SEQ ID n.º 21) ; y
en donde (aa2) m se selecciona del grupo que consiste en Gly y Asp; y en donde Z es una secuencia aminoacídica que consiste en 2 o 3 restos aminoacídicos contiguos seleccionados del grupo que consiste en y .
2. Péptido de acuerdo con la reivindicación 1, en donde dicho péptido es un análogo de MSHα que consiste en 16 restos aminoacídicos y (aa 1) n se selecciona del grupo que consiste en
(SEQ ID n.º 17) , (SEQ ID n.º 18) ,
(SEQ ID n.º 19) ;
Y se selecciona del grupo que consiste en (SEQ ID n.º 16) ;
e ;
(aa2) m es Gly; y Z se selecciona del grupo que consiste en 3. Péptido de acuerdo con la reivindicación 1, en donde dicho péptido es un análogo de MSHγ que consiste en 14 o 15 restos aminoacídicos y (aa 1) n se selecciona del grupo que consiste en (SEQ ID n.º 20) y
(SEQ ID n.º 21) ;
Y se selecciona del grupo que consiste en (SEQ ID n.º 16) ;
y
4. Péptido de acuerdo con cualquiera de las reivindicaciones anteriores, en donde el extremo carboxilo de dicho péptido está modificado por amidación (-NH2) .
5. Péptido de acuerdo con cualquiera de las reivindicaciones anteriores, en donde dicho péptido se selecciona del grupo que consiste en:
6. Péptido de acuerdo con cualquiera de las reivindicaciones anteriores, en donde dicho péptido es capaz de 5 fijarse y activar los receptores de melanocortinas MC1r y/o MC3r.
7. Composición farmacéutica que comprende el péptido de acuerdo con cualquiera de las reivindicaciones 1 a
6.
8. Péptido de acuerdo con cualquiera de las reivindicaciones 1 a 6, para ser usado como un medicamento.
9. Péptido de acuerdo con cualquiera de las reivindicaciones 1 a 6, para ser usado en el tratamiento de una 10 afección isquémica y/o inflamatoria en el tejido de uno o varios órganos de un mamífero.
10. Péptido para ser usado de acuerdo con la reivindicación 9, en donde dicho órgano se selecciona del grupo que consiste en riñón, hígado, cerebro, corazón, músculos, médula ósea, piel, huesos, pulmones, las vías respiratorias, bazo, glándulas exocrinas, vejiga, glándulas endocrinas, órganos reproductivos, que incluyen las trompas de Falopio, ojo, oído, aparato circulatorio, el tramo gastrointestinal incluido el intestino delgado, colon, recto,
canal anal y glándula prostática.
11. Péptido para ser usado de acuerdo con cualquiera de las reivindicaciones 9 a 10, en donde dicha afección isquémica es una isquemia secundaria, tal como una isquemia debida a accidente cerebrovascular, lesión, choque septicémico, hipotensión sistémica, paro cardíaco debido a infarto de miocardio, arritmia cardíaca, enfermedad ateromatosa con trombosis, embolia de corazón o de vaso sanguíneo de cualquier órgano, vasoespasmo,
aneurisma aórtico o aneurismas en otros órganos, estenosis coronaria, infarto de miocardio, angina de pecho, pericarditis, miocarditis, mixodemia o endocarditis.
12. Péptido para ser usado de acuerdo con cualquiera de las reivindicaciones 9 a 10, en donde dicha afección isquémica y/o inflamatoria está asociada a cirugía, tal como cirugía mayor; entre ellas, cirugía cardiotorácica, cirugía abdominal, cirugía en la aorta y/o otros vasos sanguíneos mayores, reparación de una o varias válvulas cardíacas, injerto de revascularización coronaria (CABG) , cirugía en la raíz aórtica o la rama aórtica incluidas las arterias carótidas comunes, cirugía cardíaca combinada tal como sustitución de una o varias válvulas y CABG y cirugía de la raíz aórtica; síndrome inflamatorio de respuesta sistémica (SIRS) posquirúrgico y disfunción orgánica posquirúrgica, tal como insuficiencia renal posquirúrgica incluida la lesión renal aguda (LRA) , nefrotoxicidad e insuficiencia renal
crónica (IRC) .
13. Péptido para ser usado de acuerdo con cualquiera de las reivindicaciones 9 a 10, en donde dicha afección isquémica y/o inflamatoria está asociada al trasplante de órganos, tal como el trasplante de órganos sólidos que incluye trasplante de corazón, trasplante de pulmón, trasplante combinado de corazón y pulmón, trasplante de hígado y trasplante de riñón.
14. Péptido para ser usado de acuerdo con cualquiera de las reivindicaciones 9 a 10, en donde dicha afección isquémica y/o inflamatoria es la lesión por reperfusión.
15. Péptido para ser usado de acuerdo con las reivindicaciones 9 a 10, en donde dicha enfermedad inflamatoria se selecciona del grupo que consiste en artropatía (enfermedad de las articulaciones) , artritis reumatoide (AR) , gota, enfermedades inflamatorias del aparato digestivo y esclerosis múltiple.
Patentes similares o relacionadas:
Compuesto farmacéutico, del 25 de Diciembre de 2019, de VALLAURIX PTE. LTD: (C2H5)3 N - CH2 - CO - Nle - Glu - His - D-Phe - Arg - Trp - NH2 o una sal farmacéuticamente aceptable del mismo.
Compuesto farmacéutico, del 6 de Noviembre de 2019, de VALLAURIX PTE. LTD: Compuesto con estructura de fórmula Ac - Nle - Glu - His- D-Phe -X - Trp - NH2, en la que X es homoArg o norArg, o una sal farmacéuticamente aceptable del […]
Análogos de alfa-MSH terapéuticamente activos, del 25 de Febrero de 2019, de AbbVie Inc: Un péptido que asciende a un total de 19 residuos de aminoácidos, donde el péptido se selecciona del grupo que consiste en: Lys-Lys-Lys-Lys-Lys-Lys-Ser-Ser-Ile-Ile-Ser-His-Phe-Arg-Trp-Gly-Lys-Pro-Val […]
Terapia para el vitíligo, del 13 de Diciembre de 2017, de Clinuvel Pharmaceuticals Limited: Composición farmacéutica que comprende un análogo de alfa-MSH el cual es un derivado de alfa-MSH que exhibe actividad agonista para el receptor de melanocortina-1 […]
Terapia para el vitíligo, del 22 de Julio de 2015, de Clinuvel Pharmaceuticals Limited: Composición farmacéutica que comprende un análogo de alfa-MSH seleccionado del grupo que consiste de: [Nle4, D-Phe7]-alfa MSH [Nle4, D-Phe7]-alfa […]
Conjugados tripeptídicos agonistas de la MSH, del 12 de Marzo de 2014, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS): Conjugado tripeptídico de fórmula: a) 5 A-His-DPhe-Arg-NH2, o b) A-His-DPhe-Trp-NH2, en la que A representa el radical que corresponde […]
Análogos de alfa-MSH terapéuticamente activos, del 11 de Junio de 2013, de AbbVie Inc: Un péptido que consiste en la secuencia: Lys-Lys-Lys-Lys-Lys-Lys-Ser-Tyr-Ser-Met-Glu-His-Phe-Arg-Trp-Gly-Lys-Pro-Val (SEC. ID Nº: 1),donde el extremo amino terminal de […]
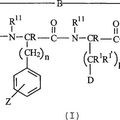 LIGANDOS DEL RECEPTOR DE MELANOCORTINA, del 16 de Octubre de 2008, de THE PROCTER & GAMBLE COMPANY: Ligandos del receptor de melanocortina. Se refiere a nuevos ligandos del receptor de melanocortina. Estos ligandos son análogos peptídicos cíclicos que preferiblemente […]
LIGANDOS DEL RECEPTOR DE MELANOCORTINA, del 16 de Octubre de 2008, de THE PROCTER & GAMBLE COMPANY: Ligandos del receptor de melanocortina. Se refiere a nuevos ligandos del receptor de melanocortina. Estos ligandos son análogos peptídicos cíclicos que preferiblemente […]