Antígenos de estreptococos del grupo B.
Un polipéptido aislado que comprende un fragmento antigénico de un polipéptido que consiste en la secuencia de aminoácidos expuesta en la SEC ID NO:
39 o en la SEC ID NO: 44, en la que el fragmento antigénico es capaz de inducir producción de un anticuerpo que es específico para estreptococo del grupo B.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10180962.
Solicitante: ID BIOMEDICAL CORPORATION OF QUEBEC.
Nacionalidad solicitante: Canadá.
Dirección: 525 CARTIER BOULEVARD WEST LAVAL, QC H7V 3S8 CANADA.
Inventor/es: RIOUX, CLEMENT, BRODEUR,BERNARD,R, BOYER,MARTINE, CHARLEBOIS,ISABELLE, HAMEL,JOSEE, MARTIN,DENIS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/09 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Streptococcus.
- C07K14/315 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Streptococcus (G), p. ej. Enterococci.
- C12N1/21 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › modificados por la introducción de material genético extraño.
- C12N15/31 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas microbianas, p. ej. enterotoxinas.
PDF original: ES-2540281_T3.pdf
Fragmento de la descripción:
Antígenos de estreptococos del grupo B.
Campo de la invención La presente invención se refiere a antígenos, más en particular a antígenos proteicos del patógeno bacteriano estreptococo del grupo B (GBS) que son útiles como componentes de vacunas para terapia y/o profilaxis. 5
Antecedentes de la invención Streptococcus son bacterias gram (+) que se diferencian por antígenos de carbohidratos específicos de grupos A a O encontrados sobre su superficie celular. Los grupos de estreptococos se distinguen adicionalmente por antígenos polisacarídicos capsulares específicos de tipo. Se han identificado varios serotipos para el estreptococo de grupo V (GBS) : Ia, Ib, II, III, IV, V, VI, VII y VIII. GBS también contiene proteínas antigénicas conocidas como "proteínas C" 10 (alfa, beta, gamma y delta) , algunas de ellas se han clonado.
Aunque GBS es un componente común de la flora vaginal y colónica humana normal este patógeno se ha reconocido como una causa principal de sepsis neonatal y meningitis neonatal, meningitis de aparición tardía en infantes, endometritis post-parto así como mastitis en cabañas lecheras. Mujeres embarazadas expuestas a GBS están en riesgo de infección post-parto y pueden transferir la infección al bebé según en niño atraviesa el canal del parto. 15 Aunque el organismo es sensible a los antibióticos, la alta velocidad de ataque y la rápida aparición de sepsis en neonatos y de meningitis en infantes da como resultado alta morbilidad y mortalidad.
Para encontrar una vacuna que proteja individuos de infección por GBS, los investigadores han recurrido a los antígenos específicos de tipo. Desgraciadamente estos polisacáridos han demostrado ser pobremente inmunógenos en seres humanos y están restringidos al serotipo particular a partir del que se origina el polisacárido. Adicionalmente, 20 el polisacárido capsular facilita una respuesta de independiente células T es decir, sin producción de IgG. Consecuentemente los antígenos polisacarídicos capsulares son inadecuados como un componente de vacuna para protección contra infección por GBS.
Otros se han centrado en el antígeno beta de la proteína C que demostró propiedades inmunógenas en modelos de ratones y de conejos. Esta proteína se encontró que es inadecuada como una vacuna humana debido a su propiedad 25 indeseable de interacción con alta afinidad y de una manera no inmunógena con la región Fc de la IgA humana. El antígeno alfa de proteína C es raro en serotipos de tipo III de GBS que es el serotipo responsable de la mayoría de las afecciones mediadas por GBS y es por lo tanto de poco uso como un componente de vacunas.
Michel et al.: "Infection and Immunity" vol. 59, n.º 6, junio de 1996, páginas 2023-2028 describen antígenos de proteínas C de estreptococos del grupo B. 30
Por lo tanto sigue habiendo una necesidad no satisfecha de antígenos de GBS que se pueden usar como componentes de vacunas para la profilaxis y/o terapia de infección por GBS.
Sumario de la invención De acuerdo con un aspecto, la presente invención proporciona un polipéptido aislado que comprende un fragmento antigénico de un polipéptido que consiste en la secuencia de aminoácidos expuesta en la SEC ID NO: 39 o en la SEC 35 ID NO: 44, en la que el fragmento antigénico es capaz de inducir producción de un anticuerpo que es específico para estreptococo del grupo B.
En otros aspectos, proporcionan la respectiva vacuna, el respectivo anticuerpo y el respectivo procedimiento de detección.
Breve descripción de los dibujos 40
La figura 1a es la secuencia de ADN de clon 1 (SEC ID NO :1) con secuencias de aminoácidos correspondientes para marcos de lectura abiertos;
la figura 1b es la secuencia de aminoácidos SEC ID NO: 2;
la figura 1c es la secuencia de aminoácidos SEC ID NO: 3;
la figura 1d es la secuencia de aminoácidos SEC ID NO: 4; 45
la figura 1e es la secuencia de aminoácidos SEC ID NO: 5;
la figura 1f es la secuencia de aminoácidos SEC ID NO: 6;
La figura 2a es la secuencia de ADN de clon 2 (SEC ID NO :7) con secuencias de aminoácidos correspondientes para marcos de lectura abiertos;
la figura 2b es la secuencia de aminoácidos SEC ID NO: 8; la figura 2c es la secuencia de aminoácidos SEC ID NO: 9; 50
la figura 2d es la secuencia de aminoácidos SEC ID NO: 10; la figura 2e es la secuencia de aminoácidos SEC ID NO: 11; la figura 2f es la secuencia de aminoácidos SEC ID NO: 12;
La figura 3a es la secuencia de ADN de clon 3 (SEC ID NO :13) con secuencias de aminoácidos correspondientes para marcos de lectura abiertos;
la figura 3b es la secuencia de aminoácidos SEC ID NO: 14;
la figura 3c es la secuencia de aminoácidos SEC ID NO: 15;
la figura 3d es la secuencia de aminoácidos SEC ID NO: 16; 5
la figura 3e es la secuencia de aminoácidos SEC ID NO: 17;
la figura 3f es la secuencia de aminoácidos SEC ID NO: 18;
la figura 3g es la secuencia de aminoácidos SEC ID NO: 19;
la figura 3h es la secuencia de aminoácidos SEC ID NO: 20;
la figura 3i es la secuencia de aminoácidos SEC ID NO: 21; 10
La figura 4a es la secuencia de ADN de clon 4 (SEC ID NO :22) con secuencias de aminoácidos correspondientes para marcos de lectura abiertos;
la figura 4b es la secuencia de aminoácidos SEC ID NO: 23;
la figura 4c es la secuencia de aminoácidos SEC ID NO: 24;
la figura 4d es la secuencia de aminoácidos SEC ID NO: 25; 15
la figura 4e es la secuencia de aminoácidos SEC ID NO: 26;
La figura 5a es la secuencia de ADN de clon 5 (SEC ID NO :27) con secuencias de aminoácidos correspondientes para marcos de lectura abiertos;
la figura 5b es la secuencia de aminoácidos SEC ID NO: 28;
la figura 5c es la secuencia de aminoácidos SEC ID NO: 29; 20
la figura 5d es la secuencia de aminoácidos SEC ID NO: 30;
la figura 5e es la secuencia de aminoácidos SEC ID NO: 31;
La figura 6a es la secuencia de ADN de clon 6 (SEC ID NO: 32) ;
la figura 6b es la secuencia de aminoácidos SEC ID NO: 33;
la figura 6c es la secuencia de aminoácidos SEC ID NO: 34; 25
la figura 6d es la secuencia de aminoácidos SEC ID NO: 35;
la figura 6e es la secuencia de aminoácidos SEC ID NO: 36;
La figura 7a es la secuencia de ADN de clon 7 (SEC ID NO: 37) ;
la figura 7b es la secuencia de aminoácidos SEC ID NO: 38;
la figura 7c es la secuencia de aminoácidos SEC ID NO: 39; 30
la figura 7d es la secuencia de aminoácidos SEC ID NO: 40;
la figura 7e es la secuencia de aminoácidos SEC ID NO: 41;
La figura 8 es la secuencia de ADN de una parte de clon 7 que incluye una secuencia señal (SEC ID NO: 42) ;
La figura 9 es la secuencia de ADN de una parte de clon 7 sin una secuencia señal (SEC ID NO: 43) ;
la figura 9a es la secuencia de aminoácidos (SEC ID NO: 44) ; 35
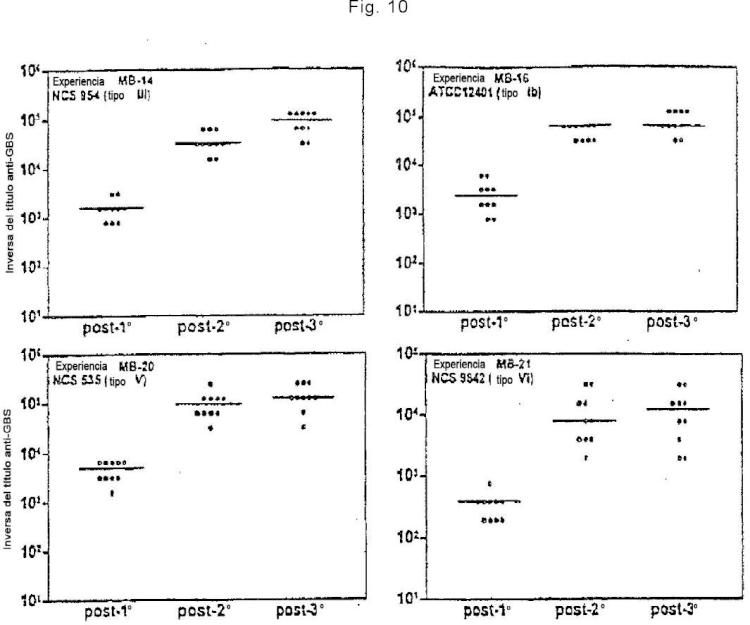
La figura 10 representa la distribución de títulos de ELISA en sueros a partir de ratones CD-1 inmunizados con proteína GBS recombinante correspondiente a la SEC ID NO: 39.
Descripción detallada de la invención La presente invención se refiere a la materia objeto de las reivindicaciones adjuntas.
Como se usa en el presente documento, "fragmentos", "derivados" o "análogos" de los polipéptidos de la invención 40 incluyen aquellos polipéptidos en los que uno o más de los residuos aminoacídicos están sustituidos por un residuo aminoacídico conservado o no conservado (preferentemente conservado) y que puede ser natural o artificial.
Los términos «fragmentos», «derivados» o «análogos» de polipéptidos de la presente invención incluyen también polipéptidos que están modificados por adición, deleción, sustitución de aminoácidos siempre que los polipéptidos retengan la capacidad para inducir una respuesta inmune. 45
Por la expresión «aminoácido conservado» se quiere decir una sustitución de uno o más aminoácidos por otros en los que el determinante antigénico (incluyendo su estructura secundaria y su naturaleza hidropática) de un antígeno dado está conservado completamente o parcialmente a pesar de la sustitución.
Por ejemplo, uno o más residuos de aminoácidos dentro de la secuencia pueden sustituirse por otro aminoácido de una polaridad similar, que actúa como un equivalente funcional, dando como resultado una alteración silenciosa. Los 50 sustitutos para un aminoácido dentro de la secuencia puede seleccionarse a partir de otros miembros de la clase a la que pertenece dicho aminoácido. Por ejemplo, los aminoácidos no polares (hidrófobos) incluyen... [Seguir leyendo]
Reivindicaciones:
1. Un polipéptido aislado que comprende un fragmento antigénico de un polipéptido que consiste en la secuencia de aminoácidos expuesta en la SEC ID NO: 39 o en la SEC ID NO: 44, en la que el fragmento antigénico es capaz de inducir producción de un anticuerpo que es específico para estreptococo del grupo B.
2. Una composición de vacunas que comprende el polipéptido aislado de acuerdo con la reivindicación 1 y un 5 vehículo, diluyente o coadyuvante farmacéuticamente aceptable.
3. La composición de vacunas de 2 para su uso en tratamiento terapéutico o profiláctico de infección bacteriana estreptocócica en un animal susceptible a infección estreptocócica.
4. La composición de vacunas de acuerdo con la reivindicación 3, en la que dicho animal es seleccionado de una res vacuna o un ser humano. 10
5. Un anticuerpo aislado, o fragmento de unión a antígeno del mismo, que se une específicamente a un polipéptido que consiste en la secuencia de aminoácidos expuesta en la SEC ID NO: 39 o en la SEC ID NO: 44.
6. El anticuerpo aislado, o fragmento de unión a antígeno del mismo, de la reivindicación 5 para su uso en el tratamiento de una infección estreptocócica.
7. Un procedimiento para detectar estreptococo de grupo B en una muestra biológica, comprendiendo dicho 15 procedimiento:
(a) incubar el anticuerpo, o fragmento de unión a antígeno del mismo, de acuerdo con la reivindicación 5 con la muestra biológica para formar una mezcla; y
(b) detectar anticuerpo específicamente unido o fragmento de unión a antígeno unido en la mezcla, que indica la presencia de estreptococo de grupo B. 20
Patentes similares o relacionadas:
Vacuna subunitaria contra Mycoplasma spp., del 1 de Julio de 2020, de Agricultural Technology Research Institute: Una composición para prevenir una infección por Mycoplasma spp., que comprende: un principio activo, que comprende una proteína de PdhA; y un adyuvante […]
Proteína mutante, del 19 de Febrero de 2020, de Cytiva BioProcess R&D AB: Una proteína de unión a inmunoglobulina que se une a regiones de una molécula de inmunoglobulina distintas de las regiones determinantes de […]
Nanoporos MSP y procedimientos relacionados, del 8 de Enero de 2020, de UNIVERSITY OF WASHINGTON: Porina de Mycobacterium Smegmatis (Msp) que tiene un vestíbulo y una zona de constricción que definen un túnel, en la que la Msp comprende una MspA mutante, […]
Complejos génicos sintéticos, del 28 de Agosto de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un método para reemplazar la regulación nativa de un conjunto de genes asociados colectivamente con una función con regulación sintética, comprendiendo […]
Métodos de despliegue de proteínas que contienen dominios Fc no covalentes sobre la superficie de células y métodos de selección de las mismas, del 10 de Julio de 2019, de MERCK PATENT GMBH: Método para el despliegue de proteínas sobre la superficie de una célula huésped, comprendiendo el método: (a) introducir en una célula huésped al menos uno o más polinucleótidos […]
Polipéptidos efectores desinmunizados de subunidad A de toxina Shiga para aplicaciones en mamíferos, del 19 de Junio de 2019, de MOLECULAR TEMPLATES, INC: Polipéptido que comprende una región efectora de la toxina Shiga, en el que: (i) la región efectora de la toxina Shiga tiene al menos un 95% de identidad de secuencia […]
Proteína de exportación de O-fosfoserina novedosa y procedimiento para producir O-fosfoserina usando la misma, del 5 de Junio de 2019, de CJ CHEILJEDANG CORPORATION: Un procedimiento para producir O-fosfoserina (OPS), que comprende cultivar un microorganismo que produce Ofosfoserina que se ha modificado para potenciar […]
Bacterias lácticas texturizantes, del 16 de Abril de 2019, de Dupont Nutrition Biosciences ApS: Cepa bacteriana láctica que comprende al menos una secuencia seleccionada entre el grupo constituido por las secuencias de nucleótidos SEC ID Nº 1, SEC ID Nº […]