Modelo de carcinogénesis por fusión de células madre.
Método para modelizar la migración de células cancerosas que incluye los pasos de:
a) proporcionar una célula madre derivada de médula ósea;
b) proporcionar una célula premaligna iniciada consistente en una célula con cambios genéticos o epigenéticos, incluyendo los cambios genéticos mutaciones genéticas, translocaciones, deleciones o amplificaciones, incluyendo los cambios epigenéticos cualquier cambio más allá de las secuencias de ADN que conduzca a una desregulación del crecimiento y la función celular, como metilación de ADN, modificación de cromatina o señalización de células alteradas, y siendo los cambios genéticos o epigenéticos suficientes para provocar una autorrenovación, invasión tisular o migración;
c) fusionar la célula madre derivada de médula ósea con la célula iniciada, creando así una célula fusionada; y
d) medir un indicador de migración para la célula fusionada.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/033366.
Solicitante: THE ARIZONA BOARD OF REGENTS, ON BEHALF OF THE UNIVERSITY OF ARIZONA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: P.O. BOX 210158 TUCSON AZ 85721-0158 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HARRIS, DAVID T., TSANG,TOM C, HE,XIANGHUI, PIPES,BRIAN L, MEADE-TOLLIN,LINDA C.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N5/08
PDF original: ES-2523857_T3.pdf
Fragmento de la descripción:
Modelo de carcinogénesis por fusión de células madre
ANTECEDENTES DE LA INVENCION Referencia cruzada a solicitudes relacionadas
Esta solicitud reivindica el derecho de prioridad de la solicitud provisional U.S. n° 6/711,249, titulada "Stem Cell Fusión Model of Carcinogensis", presentada el 25 de agosto de 25, cuyo contenido completo se incorpora aquí por referencia.
Campo de la invención
La invención se refiere a un sistema de células y a un método para modelizar, cribar fármacos contra células cancerosas e inhibir la migración de células cancerosas.
Descripción de la técnica relacionada
El cáncer ha sido difícil de tratar debido a la heterogeneidad y la inestabilidad genética. Como enfermedad humana, el cáncer ya fue descrito el año 16 a.C. en antiguas escrituras egipcias. Hipócrates, el médico griego, reconoció la diferencia entre tumores benignos y malignos y llamó "carcinos" a los tumores malignos. Actualmente, el cáncer es la segunda causa más importante de muerte en los países desarrollados.
Desde que el Presidente de los Estados Unidos Richard Nixon declarara una "guerra al cáncer" en la década de los 7, se ha acumulado un conocimiento enorme sobre el cáncer. En los dos últimos siglos se han propuesto muchas hipótesis sobre el desarrollo del cáncer. Las primeras hipótesis incluían las hipótesis irritativas, embrionarias y parasitarias. Más tarde, con el establecimiento de la oncología experimental, se Identificaron carcinógenos químicos. Se descubrieron docenas de oncogenes y genes supresores de tumores mediante análisis molecular de tumores humanos y animales experimentales. Estos estudios condujeron al establecimiento de la hipótesis de mutación genética, que ha predominado en lastres últimas décadas.
A pesar de su elegancia Intrínseca, la hipótesis actual de mutación genética no ha podido explicar muchas características Importantes del cáncer. De hecho, muchos Investigadores han estudiado a fondo la hipótesis de la mutación genética.
Recientemente, la "teoría de carcinogénesis de células madre" ha ganado impulso, gracias al mejor entendimiento de los Investigadores de las células madre y al descubrimiento de las "células madre cancerosas". La teoría de carcinogénesis de células madre sugiere que las células madre acumulan mutaciones genéticas y se convierten en células malignas. Sin embargo, dado que sigue dependiendo por completo de la hipótesis de mutación genética, la teoría de las células madre no puede revelar por completo qué provoca las características distintivas del cáncer, como la invasión y la metástasis.
Las mutaciones son eventos extraños. Los modelos matemáticos sugieren que se requiere un evento más frecuente para una transformación maligna. Ya se ha Indicado que la inestabilidad genómica puede ser la característica que posibilita las características del cáncer. Como fenotipo de la inestabilidad genómica, prácticamente en todos los cánceres humanos sólidos se ha observado aneuploldía, que es difícil de explicar mediante hipótesis de mutación genética. Se ha sugerido que la aneuploidía explica el cáncer como un mutágeno autónomo, pero el mecanismo que subyace a la aneuploidía sigue siendo poco claro.
Así, a pesar del progreso esencial realizado, el origen del cáncer sigue siendo enigmático. Dado que los modelos actuales de la carcinogénesis basados en la hipótesis de la mutación genética tienen limitaciones para explicar muchos aspectos del cáncer, los inventores han presentado un nuevo modelo de
carcinogénesis multietapa en el que se sugiere que el desarrollo del cáncer implica mutaciones genéticas y fusiones celulares. Específicamente, el cáncer puede resultar de una fusión entre una célula premaligna "alterada" y una célula madre derivada de médula ósea (bone marrow-derived stem cell - BMDSC). La "aneuploidía", que es una característica de malignidad, es una consecuencia directa de esta fusión celular. El modelo de "fusión de células madre" explica las notables similitudes entre las células malignas y las BMDSC. Este modelo también explica por qué no-mutágenos pueden ser carcinógenos y por qué procesos no mutágenos, como la cicatrización y la inflamación crónica, pueden promover la transformación maligna.
SUMARIO DE LA INVENCIÓN
En una realización de la invención, se proporciona un método para modelizar la migración de células cancerosas, que incluye los pasos de: (a) proporcionar una célula madre derivada de médula ósea; (b) proporcionar una célula premaligna iniciada que es una célula con cambios genéticos o epigenéticos, incluyendo los cambios genéticos mutaciones genéticas, translocaciones, deleciones o amplificaciones, incluyendo los cambios epigenéticos cualquier cambio más allá de las secuencias de ADN que conduzca a una desregulación del crecimiento y la función celular, como metilación de ADN, modificación de cromatina o señalización de células alteradas, y siendo los cambios genéticos o epigenéticos suficientes para provocar una autorrenovación, invasión tisular o migración; (c) fusionar la célula madre derivada de médula ósea con la célula iniciada, creando así una célula fusionada; y (d) medir un indicador de migración para la célula fusionada. La célula fusionada se puede obtener o cultivar a partir de una fusión previa de la célula madre derivada de médula ósea con la célula iniciada.
En otra realización de la invención, se proporciona un método para examinar un efecto de un agente biológico o químico en células tumorales, que incluye los pasos de: (a) proporcionar una célula fusionada derivada de la fusión de una célula madre derivada de médula ósea con una célula premaligna iniciada, siendo dicha célula iniciada una célula con cambios genéticos o epigenéticos, incluyendo los cambios genéticos mutaciones genéticas, translocaciones, deleciones o amplificaciones, incluyendo los cambios epigenéticos cualquier cambio más allá de las secuencias de ADN que conduzca a una desregulación del crecimiento y la función celular, como metilación de ADN, modificación de cromatina o señalización de células alteradas, y siendo los cambios genéticos o epigenéticos suficientes para provocar una autorrenovación, invasión tisular o migración; (b) poner en contacto la célula fusionada con un agente biológico o químico; y (c) determinar si la migración de células tumorales se ha promovido, inhibido o ha permanecido inalterada.
Los métodos de la invención representan un modelo de carcinogénesis nuevo y mejorado para estudios in vitro de migración de células tumorales y estudios in vivo utilizando animales trasplantados con médula ósea modificada con un gen marcador, por ejemplo transgénicos eGFP. Otras características y ventajas de la invención se desprenderán de la siguiente descripción detallada de determinadas realizaciones específicas junto con las figuras adjuntas.
BREVE DESCRIPCIÓN DE LAS FIGURAS
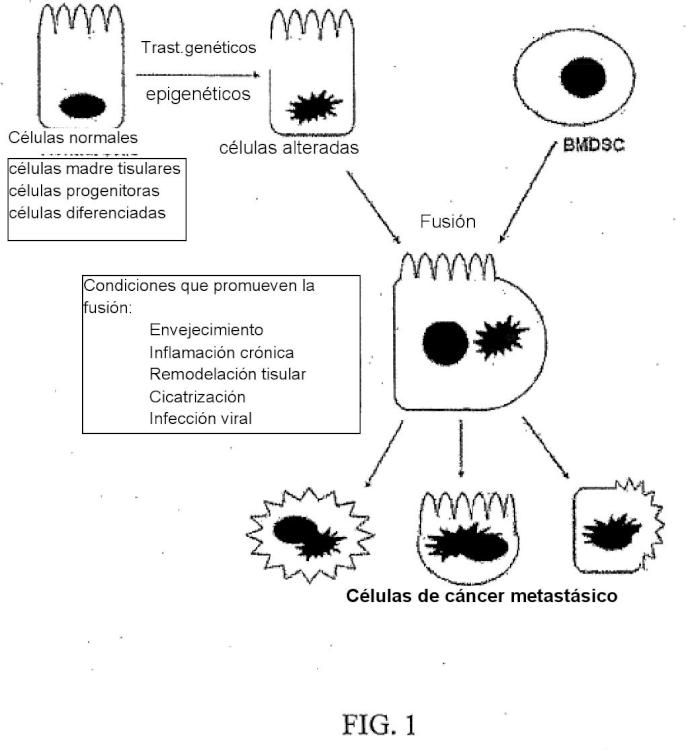
Figura 1: es una ilustración esquemática de una transformación maligna mediada por fusión entre
células madre derivadas de médula ósea y células tisulares "alteradas".
DESCRIPCIÓN DE LAS REALIZACIONES PREFERENTES
Tal como se utiliza aquí, "metástasis" significa la propagación de cáncer desde una parte del cuerpo a otra. Un tumor formado por células que se han propagado se denomina "tumor metastásico" o "metástasis".
El término "maligno" se refiere a células cancerosas, es decir anómalas, que se dividen sin control y que pueden invadir tejidos cercanos y propagarse a través de la corriente sanguínea y el sistema linfático a otras partes del cuerpo.
Los términos "célula alterada" o "célula genéticamente alterada" se definen aquí como cualquier célula con cambios genéticos o epigenéticos suficientes para desviarse de la vía de diferenciación normal de una célula madre derivada de médula ósea después de fusión con una BMDSC. Las células "alteradas" incluyen las llamadas "células premalignas iniciadas" en el modelo de carcinogénesis de múltiples pasos.
El término "célula de fusión" significa una célula formada por la fusión de una célula alterada y una célula madre derivada de médula ósea.
El origen de la malignidad sigue siendo controvertido, en especial en lo que respecta a los carcinomas, que representan más de un 9% de la malignidad en humanos. El modelo de carcinogénesis presentado por los inventores se centra en el origen del desarrollo de carcinomas altamente malignos. El evento clave en este modelo es un paso de fusión entre células madre derivadas de médula ósea (BMDSC) y células tisulares "alteradas" (Figura 1). Las poblaciones... [Seguir leyendo]
Reivindicaciones:
1. Método para modelizar la migración de células cancerosas que incluye los pasos de:
a) proporcionar una célula madre derivada de médula ósea;
b) proporcionar una célula premallgna iniciada consistente en una célula con cambios genéticos o eplgenétlcos, Incluyendo los cambios genéticos mutaciones genéticas, translocaclones, deleclones o amplificaciones, Incluyendo los cambios epigenétlcos cualquier cambio más allá de las secuencias de ADN que conduzca a una desregulación del crecimiento y la función celular, como metllaclón de ADN, modificación de cromatina o señalización de células alteradas, y siendo los cambios genéticos o epigenéticos suficientes para provocar una autorrenovación, invasión tisular o migración;
c) fusionar la célula madre derivada de médula ósea con la célula iniciada, creando así una célula fusionada; y
d) medir un indicador de migración para la célula fusionada.
2. Método según la reivindicación 1, caracterizado porque los pasos (a) y (b) incluyen obtener o cultivar la célula fusionada a partir de una fusión previa de la célula madre derivada de médula ósea con la célula iniciada.
3. Método según la reivindicación 1, caracterizado porque el paso (d) incluye un ensayo de rascado in
vitro.
4. Método según la reivindicación 1, caracterizado porque el paso (d) se lleva a cabo in vivo en un animal no humano.
5. Método según la reivindicación 1, caracterizado porque dicha célula del paso (b) es de origen epitelial.
6. Método para examinar un efecto de un agente biológico o químico en la migración de células tumorales, que incluye los pasos de:
a) proporcionar una célula fusionada derivada de una fusión de una célula madre derivada de médula ósea con una célula premaligna iniciada, siendo dicha célula iniciada una célula con cambios genéticos o epigenéticos, incluyendo los cambios genéticos mutaciones genéticas, translocaciones, deleciones o amplificaciones, incluyendo los cambios epigenéticos cualquier cambio más allá de las secuencias de ADN que conduzca a una desregulación del crecimiento y la función celular, como metilación de ADN, modificación de cromatina o señalización de células alteradas, y siendo los cambios genéticos o epigenéticos suficientes para provocar una autorrenovación, invasión tisular o migración;
b) poner en contacto dicha célula fusionada con un agente biológico o químico; y
c) determinar si la migración de células tumorales se ha promovido, inhibido o ha permanecido inalterada.
7. Método según la reivindicación 6, caracterizado porque el paso (a) incluye proporcionar una célula iniciada de piel, mama o próstata.
8. Método según la reivindicación 6, caracterizado porque el paso (b) tiene lugar in vivo en un animal no humano.
9. Método según la reivindicación 6, caracterizado porque dicho agente biológico o químico es un anticuerpo contra ubiquitina.
1. Método según la reivindicación 9, caracterizado porque dicho anticuerpo es MEL-14.
11. Método según la reivindicación 1, caracterizado porque dicho anticuerpo se selecciona de entre el grupo consistente en los anticuerpos 14372 y 1C2-2.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]