Inmunoensayo de salvinorinas.
Un método para detectar o determinar salvinorina A, salvinorina B y análogos en C-9 de salvinorina A ysalvinorina B en una muestra in vitro,
comprendiendo el método poner en contacto la muestra con un conjugadoy un anticuerpo, detectar el conjugado unido y deducir a partir de una curva de calibración la presencia, o lacantidad, de salvinorina A, salvinorina B y análogos en C-9 de salvinorina A , en donde el anticuerpo se producecontra un inmunógeno de la siguiente estructura **Fórmula**
en donde accm es un material portador que confiere antigenicidad y el agente reticulante une el átomo de O enC-9 del anillo tricíclico fusionado al accm.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09159094.
Solicitante: RANDOX LABORATORIES LTD..
Nacionalidad solicitante: Reino Unido.
Dirección: Ardmore, 55 Diamond Road Crumlin, County Antrim BT29 4QY REINO UNIDO.
Inventor/es: MCCONNELL, ROBERT IVAN, FITZGERALD, STEPHEN PETER, LOWRY,ANDREW PHILIP, BENCHIKH,ELOUARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/16 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales vegetales.
- G01N33/94 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen narcóticos.
PDF original: ES-2415733_T3.pdf
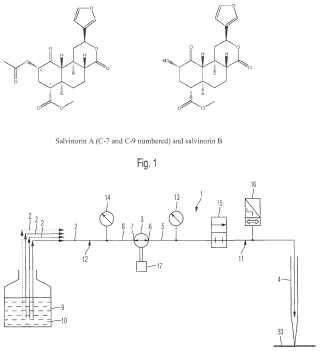
Fragmento de la descripción:
Inmunoensayo de salvinorinas
Antecedentes de la invención El diterpenoide salvinorina A, es un potente componente psicoactivo de la planta mexicana indígena Salvia divinorum utilizada en medicina por los indios mazatecos para el tratamiento de dolores de cabeza, artritis y anemia (Valdes et al., 1983) . La actividad sobre el SNC de esta molécula no nitrogenada se atribuye a su fuerte afinidad por el receptor de opiáceos kappa (abreviadamente en lo sucesivo KOR por la expresión inglesa kappa opioid receptor) (Roth et al., 2002) . Su uso como una droga recreativa está aumentando debido a su fácil disponibilidad y potente actividad. La ingestión de S. divinorum o salvinorina A (de aquí en adelante, la referencia al uso o ingestión de salvinorina A incluye implícitamente S. divinorum se realiza generalmente masticando la hoja, ingeriendo un extracto líquido de las hojas o inhalación su humo. Sus efectos sobre el SNC y propiedades alucinógenas han sido comparados con los del LSD, lo que lleva a su situación ilegal en muchos países. El KOR ha sido implicado en la nocicepción y en una serie de procesos morbosos, y hay gran interés en el ingrediente activo de S. divinorum, salvinorina A (y sus análogos) como un tratamiento potencial para diversos estados, incluyendo diarrea, trastornos del estado de ánimo y en la regulación del dolor (Vortherms and Roth, 2006) . El uso de salvinorina A y análogos como un tratamiento potencial de episodios maníacos se describe en WO 2005/089745; US 2006/0058264 describe salvinorina A y análogos como compuestos útiles para fines de investigación farmacológica y para el tratamiento de enfermedades; US 2006/0083679 propone el uso de salvinorina A y análogos como medicamentos o como sondas químicas en los procedimientos de diagnóstico, tales como tomografía de emisión de positrones (abreviadamente, PET por la expresión inglesa Positron Emission Tomography) , tomografía computarizada por emisión de un solo fotón (abreviadamente SPECT por la expresión inglesa Single-Photon Computarized Tomography) y espectroscopía de resonancia magnética nuclear (abreviadamente NMR, por la expresión inglesa Nuclear Magnetic Resonance) . Este interés ha dado lugar a la síntesis y al estudio farmacológico de diversos análogos de salvinorina. Más recientemente, se ha demostrado que derivados de éter en C-9 de salvinorina A son más activos y tienen una mayor semivida que la salvinorina A. Este desarrollo ha generado interés en la comunidad de investigación científica con respecto a potenciales nuevos fármacos terapéuticos, aunque se desconocen las consecuencias sociales más amplias del abuso de tales moléculas activas potentes sobre el SNC.
La acción de corta duración de la salvinorina A (aproximadamente 10-15 minutos) indica un rápido metabolismo a una forma inactiva. Estudios farmacocinéticos de Hooker et al., (2008) que utilizaron PET apoyaron la rápida absorción y la corta duración de acción de salvinorina A. Se especula que el análogo hidroxilado en C-9, salvinorina B, es el metabolito principal formado por hidrólisis mediada por esterasa (Yan and Roth 2004; Schmidt et al., 2005a) . Los estudios realizados por Schmidt et al., (2005a, 2005b) en el plasma de mono no fueron concluyentes, puesto que el estudio ex vivo identificó salvinorina B como metabolito, mientras que el estudio in vivo no detectó salvinorina B. Pichini et al., (2005) no pudieron detectar salvinorina A en saliva, sudor u orina de pacientes 1, 5 horas después de haber fumado la droga, lo que sugiere o bien la eliminación rápida o un extenso metabolismo. Tsujikawa et al., (2009) , en un estudio metabólico in vitro con plasma de rata, identificaron salvinorina B y ácido 1, 4a-dimetil-1-[2- (3furanil) -2-hidroxietil]-7-hidroxi-5-metoxicarbonil-8-oxodecahidronaftaleno-2-carboxílico como los principales metabolitos. Por lo tanto, aunque hay una cada vez más pruebas de que salvinorina B es el principal metabolito de salvinorina A, además de los metabolitos propuestos por Tsujikawa, es probable que haya todavía metabolitos no identificados. Para facilitar un método de detección robusto que identifique el uso de salvinorina A, son necesarios medios para detectar no sólo los marcadores reconocidos, tales como salvinorina A precursora y el metabolito en C-9, salvinorina B, sino también metabolitos todavía no identificados. Además este método debe ser altamente sensible a la salvinorina A, un marcador inequívoco del uso de salvinorina. Un análisis comparativo de la vía metabólica de otras drogas psicoactivas con estructuras moleculares similares, métodos de ingestión y propiedades farmacológicas permite predicciones de otros metabolitos posibles de la salvinorina A. El metabolismo de la droga por lo general implica la formación de sustancias más polares para facilitar la excreción. Esto ocurre a través de oxidación en una primera fase (en la sangre) mediada por las enzimas citocromo P450 y glucuronidación en una segunda fase de (en el hígado) . Las similitudes estructurales y farmacológicas de salvinorina A y L9-THC, así como sus métodos similares de ingestión, sugieren que los datos metabólicos derivados de la investigación de 9-THC
L podrían ser un indicador útil de los productos probablemente metabólicos de la salvinorina A. Un metabolito de L9-THC es el alcohol primario 11-hidroxi-L9-THC, formado por oxidación del grupo metilo unido al grupo alqueno del sistema heterocíclico.
El alcohol primario se oxida adicionalmente al principal metabolito de L9-THC, ácido 11-nor-L9-THC-9-carboxílico que también experimenta glucuronidación. La cocaína y la heroína, drogas potentes que actúan sobre el SNC, al igual que la salvinorina A, posee cada una dos funcionalidades éster y se podría esperar que las vías metabólicas de los tres fármacos mostraran similitudes. La cocaína y la heroína son metabolizadas por carboxilesterasas humanas (hCE) , enzimas expresadas en diversos órganos, incluyendo hígado, intestinos y pulmones (Imai et al., 2006) . Basándose en evidencia científica comparativa y en las propiedades farmacológicas de la salvinorina A y sus análogos, el ácido salvinorina-A-7-carboxílico y ácido salvinorina-B-7-carboxílico, son potenciales metabolitos de la salvinorina A.
Se han ideado varios métodos de análisis para detectar y cuantificar la salvinorina A y sus análogos en S. divinorum (Grundmann et al., 2007) . Además del estudio en plasma de rata de Tsujikawa, la detección en fluidos animales se ha limitado a la detección de salvinorina A y salvinorina B. Schmidt et al., (2005a) usaron HPLC-MS para detectar salvinorina A y salvinorina B en muestras de plasma de monos ex vivo. Dichos autores describieron que la 5 salvinorina B no podía ser claramente detectada en muestras in vivo. Pichini et al., (2005) usaron cromatografía de gases-espectrometría de masas (GC-MS) para analizar orina, saliva y sudor de dos individuos que habían fumado hojas de S. divinorum. Como se ha descrito anteriormente, la salvinorina A, se detectó en orina en las primeras 1, 5 horas (el límite de detección fue 5 ng/mL) . Después de 1, 5 horas, la técnica no detectó salvinorina A en orina o saliva, probablemente limitada por la sensibilidad del ensayo. McDonough et al., (2008) desarrollaron un método de HPLC-MS para detectar y cuantificar la salvinorina A en fluidos biológicos humanos estableciendo como irreproducibles los métodos descritos anteriormente. El método tenía un límite de detección de 2, 5 ng/mL y un límite de cuantificación de 5, 0 ng/mL. Dichos autores sugirieron también que debido a la rápida desaparición de la salvinorina A, era deseable la identificación de un metabolito de la sustancia activa principal.
Es evidente que los formatos de ensayo existentes para la detección de la salvinorina A son inadecuados, pues usan un equipo costoso que tiene una baja sensibilidad para la salvinorina A y por lo tanto, una ventana limitada de detección después de la ingestión de salvinorina A. Además, estos ensayos no se dirigen a la detección de nuevos y futuros análogos sintéticos de mayor estabilidad y actividad que la salvinorina A.
Bibliografía Grundmann O. et al., (2007) . Planta Med., 73: 1046.
Hooker J.M. et al., (2008) . Neuroimage, 41: 1044-1050.
Imai, T. et al., (2006) . Drug Metab Dispos., 34: 1734-1741.
McDonough et al., P.C. (2008) . J. Anal. Toxicol, 32: 417-421.
Pichini S et al., (2005) . Rap. Commun. Mass Spectr., 19: 1649-1656.
Roth B.L.et al., (2002) . Proc. Natl. Acad. Sci., 99: 11934-11939.
Schmidt M.S. et al., (2005a) . J. Chromatography B, 818: 221-225.
Schmidt, M.D. et al. (2005b) . Synapse, 58: 208-210.
Valdes, L.J. et al., (1983) . J. Ethnopharmacol, 7:... [Seguir leyendo]
Reivindicaciones:
1. Un método para detectar o determinar salvinorina A, salvinorina B y análogos en C-9 de salvinorina A y salvinorina B en una muestra in vitro, comprendiendo el método poner en contacto la muestra con un conjugado y un anticuerpo, detectar el conjugado unido y deducir a partir de una curva de calibración la presencia, o la cantidad, de salvinorina A, salvinorina B y análogos en C-9 de salvinorina A, en donde el anticuerpo se produce contra un inmunógeno de la siguiente estructura
en donde accm es un material portador que confiere antigenicidad y el agente reticulante une el átomo de O en C-9 del anillo tricíclico fusionado al accm.
4. Un método para detectar o determinar salvinorina A y/o salvinorina B y análogos en C-7 de salvinorina A y/o salvinorina B en una muestra in vitro, comprendiendo el método poner en contacto la muestra con un conjugado y con al menos un anticuerpo, detectar el conjugado unido y deducir a partir de una curva de calibración la presencia, o la cantidad, de salvinorina A y/o salvinorina B y análogos en C-7 de salvinorina A y/o salvinorina B, en donde el anticuerpo se produce contra un inmunógeno de la siguiente estructura en donde R = H o acetilo, accm es un material portador que confiere antigenicidad y el agente reticulante une el grupo carbonilo en C-7 del anillo tricíclico fusionado al accm.
5. El método de la reivindicación 4, en donde el anticuerpo se produce contra un inmunógeno en el que R del
inmunógeno es H o acetilo; el agente reticulante es - (X) n-Y-Z-, donde n = 0 o 1, y si X está presente es preferiblemente un heteroátomo seleccionado de O, S y N que se une al grupo carbonilo unido en C-7 del anillo tricíclico condensado; Y es preferiblemente un resto alquileno saturado o de cadena lineal sustituida o no sustituida de C1-10, más preferiblemente de C2-6, o un resto arileno; Z es preferiblemente un grupo carbonilo o un grupo amino.
6. Un método para detectar o determinar ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2hidroxietil]-7-hidroxi-5-metoxicarbonil-8-oxodecahidronaft-2-il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4adimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-5-carboxi-7-hidroxi-8-oxodecahidronaft-2-il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-7-acetoxi-5-carboxi-8-oxodecahidronaft2-il}etanoico o ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-7-acetoxi-5
metoxicarbonil-8-oxodecahidronaft-2-il}etanoico en una muestra in vitro, comprendiendo el método poner en contacto la muestra con un conjugado y con al menos un anticuerpo, en donde el anticuerpo se produce contra un inmunógeno de la siguiente estructura en donde R = H o acetilo y R1 = OH o CH3-O-, accm es un material portador que confiere antigenicidad y el agente reticulante une el grupo carbonilo en C-2 del anillo bicíclico fusionado al accm.
7. El método de la reivindicación 6, donde el anticuerpo se produce contra un inmunógeno en el que R del inmunógeno es H o acetilo y R1 del inmunógeno es OH o CH3-O-; el agente reticulante es - (X) n-Y-Z-, donde n es 0 o 1 y si X está presente es preferiblemente N, O o S; Y es preferiblemente un resto alquileno saturado o de cadena lineal sustituida o no sustituida de C1-10, más preferiblemente de C1-6, o un resto arileno; Z del inmunógeno es preferiblemente un grupo carbonilo o un grupo amino.
8. Un anticuerpo producido contra un inmunógeno como se describe en las reivindicaciones 1 o 2, siendo el anticuerpo capaz de unirse con al menos un epítopo estructural de salvinorina A, salvinorina B y análogos en C-9 de salvinorina A y salvinorina B.
9. Un anticuerpo producido contra un inmunógeno como se describe en la reivindicación 3, siendo el anticuerpo capaz de unirse con al menos un epítopo estructural de salvinorina A, salvinorina B, 9-metoximetiléter-salvinorina B y 9-etoximetiléter-salvinorina B.
10. Un anticuerpo producido contra un inmunógeno como se describe en las reivindicaciones 4 o 5, siendo el anticuerpo capaz de unirse con al menos un epítopo estructural de salvinorina A y análogos en C-7 de salvinorina A.
11. Un anticuerpo producido contra un inmunógeno como se describe en las reivindicaciones 6 o 7, siendo el anticuerpo capaz de unirse con al menos un epítopo estructural de ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil1-[ (S) -2- (3-furanil) -2-hidroxietil]-7-hidroxi-5-metoxicarbonil-8-oxodecahidronaft-2-il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-5-carboxi-7-hidroxi-8-oxodecahidronaft-2il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-7-acetoxi-5-carboxi-8ºxodecahidronaft-2-il}etanoico o ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-7acetoxi-5-metoxicarbonil-8-oxodecahidronaft-2-il}etanoico.
12. Un kit para detectar o determinar salvinorina A, salvinorina B y análogos en C-9 de salvinorina A y salvinorina B, incluyendo el kit al menos un anticuerpo de la reivindicación 8.
13. Un kit para detectar o determinar salvinorina A, salvinorina B, 9-metoximetiléter-salvinorina B y 9-etoximetilétersalvinorina B, incluyendo el kit al menos un anticuerpo de la reivindicación 9.
14. Un kit para detectar o determinar salvinorina A y análogos en C-7 de salvinorina A, incluyendo el kit al menos un anticuerpo de la reivindicación 10.
15. Un kit para detectar o determinar ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4 a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]7-hidroxi-5-metoxicarbonil-8-oxodecahidronaft-2-il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-[ (S) 2- (3-furanil) -2-hidroxietil]-5-carboxi-7-hidroxi-8-oxodecahidronaft-2-il}etanoico, ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) 1, 4a-dimetil-1-[ (S) -2- (3-furanil) -2-hidroxietil]-7-acetoxi-5-carboxi-8-oxodecahidronaft-2-il}etanoico o ácido 2-{ (1R, 2R, 4aR, 5R, 7S, 8aR) -1, 4a-dimetil-1-
Patentes similares o relacionadas:
Anticuerpos para olanzapina y uso de los mismos, del 8 de Julio de 2020, de JANSSEN PHARMACEUTICA NV: Un anticuerpo aislado o un fragmento de unión del mismo, que se une a olanzapina y que se selecciona del grupo que consiste de: i) un anticuerpo aislado o un fragmento […]
Anticuerpos para haptenos de quetiapina y uso de los mismos, del 26 de Febrero de 2020, de JANSSEN PHARMACEUTICA NV: Un anticuerpo aislado o un fragmento de enlace del mismo, que enlaza específicamente con la quetiapina, y se genera en respuesta a un conjugado de un compuesto de Fórmula […]
Kits de detección de lectura directa para contaminación de superficie por fármacos antineoplásicos, del 12 de Febrero de 2020, de Centers for Disease Control and Prevention: Un procedimiento para detectar la contaminación por fármacos antineoplásicos de una superficie, que comprende: proporcionar una solución humectante […]
Método para la medición de anticuerpos anti-fármaco, del 25 de Diciembre de 2019, de JIMRO CO., LTD: Un método para medir anticuerpos anti-fármaco (ADA) en un analito a medir, comprendiendo el método: una etapa de proporcionar una muestra […]
Matriz multisensor y su uso para la detección de analitos o mezclas de los mismos en la fase gaseosa y procedimiento para su preparación, del 27 de Noviembre de 2019, de DANMARKS TEKNISKE UNIVERSITET: Una matriz multisensor para la detección de un analito o mezclas del mismo en la fase gaseosa, que comprende al menos dos compuestos quimioselectivos […]
Procedimiento diagnóstico para detectar una enfermedad autoinmunitaria relacionada con gaba(a) y materia objeto relacionada, del 27 de Noviembre de 2019, de Institut D'Investigaciones Biomèdiques August Pi i Sunyer: Uso in vitro de un GABA(A)R, fragmento de GABA(A)R, u homólogo del mismo o de una célula que expresa el GABA(A)R, fragmento de GABA(A)R, u homólogo del mismo para el pronóstico […]
Composiciones y métodos para la detección de metabolitos de metadona, del 5 de Noviembre de 2019, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Un compuesto que comprende una unidad estructural, seleccionada del grupo que consiste en unidades estructurales de etiqueta de poli(aminoácido), […]
Anticuerpos contra haptenos de olanzapina y uso de los mismos, del 15 de Mayo de 2019, de JANSSEN PHARMACEUTICA NV: Un método para producir un anticuerpo que se une a la olanzapina, el método comprendiendo: (i) seleccionar un huésped no humano para la producción de anticuerpos; […]