Inhibidores de MAP quinasa p38.
Un compuesto de fórmula (I):
en donde:
G es -N≥ o -CH≥
D es un radical fenilo sustituido opcionalmente o piridinilo sustituido opcionalmente;
R6 es hidrógeno o alquilo C1-C3 sustituido opcionalmente;
P representa hidrógeno y U representa un radical de fórmula (IA);
-A-(CH2)z-X1-L1-Y-NH-CR1R2R3 (IA)
en donde
A representa un radical 1,4-fenileno sustituido opcionalmente;
z es 0 o 1;
Y es un enlace, -C(≥O)-, -S(≥O)2-, -C(≥O)NR7-, -C(≥S)-NR7, -C(≥NH)NR7 o -S(≥O)2NR7- en donde R7 eshidrógeno o alquilo C1-C6 sustituido opcionalmente;
L1 es un radical divalente de fórmula -(Alk1)m(Q)n(Alk2)p- en donde
m, n y p son independientemente 0 o 1,
Q es (i) un radical carbocíclico o heterocíclico mono- o bicíclico divalente sustituido opcionalmente que tiene 5 -13 miembros anulares, o (ii), en el caso en el que tanto m como p son 0, un radical divalente de fórmula -X2-Q1-o -Q1-X2- en donde X2 es -O-, S- o NRA- en donde RA es hidrógeno o alquilo C1-C3 sustituido opcionalmente, yQ1 es un radical carbocíclico o heterocíclico mono- o bicíclico divalente sustituido opcionalmente que tiene 5 - 13miembros anulares,
Alk1 y Alk2 representan independientemente radicales cicloalquilo C3-C7 divalentes sustituidos opcionalmente, oradicales alquileno C1-C6, alquenileno C2-C6, o alquinileno C2-C6 lineales o ramificados sustituidosopcionalmente que pueden contener opcionalmente o terminar en una conexión éter (-0-), tioéter (-S-) o amino(-NRA-) en donde RA es hidrógeno o alquilo C1-C3 sustituido opcionalmente; y
X1 representa un enlace; -C(≥O); o -S(≥O)2-; -NR4C(≥O)-, -C(≥O)NR4-, -NR4C(≥O)NR5-, -NR4S(≥O)2-, o-S(≥O)2NR4- en donde R4 y R5 son independientemente hidrógeno o alquilo C1-C6 sustituido opcionalmente;R1 es un grupo éster que es hidrolizable por medio de una o más enzimas esterasas intracelulares a un grupoácido carboxílico en donde el grupo éster tiene la fórmula - (C≥O)OR14 en donde R14 es R8R9R10C- en donde
(i) R8 es hidrógeno o sustituido opcionalmente alquil(C1-C3)-(Z1)a-[alquil(C1-C3)]b- o alquenil(C2-C3)-(Z1)a-[alquil(C1-C3)]b- en donde a y b son independientemente 0 o 1 y Z1 es -O-, -S-, o -NR11- en donde R11 eshidrógeno o alquilo C1-C3; y R9 y R10 son independientemente hidrógeno o alquil(C1-C3)-;
(ii) R8 es hidrógeno o R12R13N-alquil(C1-C3)- sustituido opcionalmente en donde R12 es hidrógeno o alquilo C1-C3y R13 es hidrógeno o alquilo C1-C3; o R12 y R13 junto con el nitrógeno al que están anclados forman un anilloheterocíclico monocíclico sustituido opcionalmente de 5 o 6 átomos anulares o un sistema anular heterocíclicobicíclico de 8 a 10 átomos anulares, y R9 y R10 son independientemente hidrógeno o alquil(C1-C3)-; o
(iii) R8 y R9 tomados junto con el carbono al que están anclados forman un anillo carbocíclico monocíclico de 3 a7 átomos anulares o un sistema anular carbocíclico bicíclico de 8 a 10 átomos anulares sustituidosopcionalmente, o un sistema anular carbocíclico monocíclico puenteado de 7 a 10 átomos anulares, y R10 es hidrógeno.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/000553.
Solicitante: CHROMA THERAPEUTICS LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: 93 Milton Park Abingdon Oxon OX14 4RY REINO UNIDO.
Inventor/es: MOFFAT, DAVID, FESTUS, CHARLES, DAVIES, STEPHEN JOHN, PINTAT,STÉPHANE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/44 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Piridinas no condensadas; Sus derivados hidrogenados.
- A61P1/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- A61P37/00 A61P […] › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
- C07D213/73 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › Radicales insustituidos amino o imino.
PDF original: ES-2427892_T3.pdf
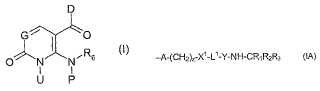
Fragmento de la descripción:
Inhibidores de MAP quinasa p38
Esta invención se refiere a una serie de ésteres de aminoácidos, a las composiciones que los contienen, a los procedimientos para su preparación y a su uso en medicina como inhibidores de MAP quinasa p38 para el tratamiento de enfermedades autoinmunitarias e inflamatorias, incluyendo artritis reumatoide, psoriasis, enfermedad inflamatoria intestinal, enfermedad de Crohn, colitis ulcerosa, enfermedad pulmonar obstructiva crónica, asma, esclerosis múltiple, diabetes, dermatitis atópica, enfermedad de injerto frente a anfitrión, lupus eritematoso generalizado y otras.
Antecedentes de la invención La activación inapropiada de leucocitos incluyendo monocitos, macrófagos y neutrófilos que conduce a la producción de niveles elevados de citoquinas tales como TNF-a, IL1-º e IL-8, es un rasgo de la patogénesis de numerosas enfermedades inflamatorias incluyendo artritis reumatoide, colitis ulcerosa, enfermedad de Crohn, enfermedad pulmonar obstructiva crónica (EPOC) , asma y psoriasis. La producción de citoquinas por las células inflamatorias es el resultado de la respuesta a una variedad de estímulos externos, que conducen a la activación de numerosos mecanismos de señalización intracelular. Entre estos destacan la superfamilia de proteínas quinasa activadas por mitógeno (MAPK) que consiste en quinasas de señalización altamente conservadas que regulan el crecimiento, la diferenciación y las respuestas el estrés de las células. Las células de mamíferos contienen al menos tres familias de MAPK: las MAPK quinasa reguladas por señales extracelulares p42/44 (ERK) , las quinasas NH2 terminales c-Jun (JNK) y la MAPK p38 (también denominada p38a/Mpk2/RK/SAPK2a/CSBP1/2) . La MAPK p38 fue clonada por primera vez después de su identificación como una quinasa que es fosforilada en tirosina después de la estimulación de los monocitos por lipopolisacáridos (LPS) [Han et al, Science 1994, 265, 808]. Se han descrito homólogos adicionales de p38 de mamífero e incluyen p38º [Jiang et al, J. Biol. Chem. 1996, 271, 17920], p38y [Li et ai, Biochem. Biophys. Res. Commun.1996, 228, 334] y p385 [Jiang et ai, J. Bioi. Chem. 1997, 272, 30122]. Si bien p38a y p38º son expresadas ubicuamente, p38y está restringida principalmente al músculo esquelético y p385 es expresada predominantemente en pulmón y riñón.
La liberación de citoquinas por las células de defensa del anfitrión y la respuesta de los leucocitos a las citoquinas y otros estreses pro-inflamatorios están regulados en un grado variable por la MAPK p38 [Cuenda et al, FEBS Lett, 1995, 364, 229-233]. En otros tipos de células, MAPK p38 controla las respuestas al estrés tales como la producción de IL-8 por las células epiteliales bronquiales estimuladas por TNF-a, y la regulación al alza de la molécula de adherencia celular ICAM-1 en células endoteliales estimuladas por LPS. Tras la activación, por medio de la fosforilación dual de un motivo TGY por las quinasas de especificidad dual MKK3 y MKK6, la MAPK p38 ejerce sus efectos a través de la fosforilación de factores de transcripción y otras quinasas. La proteína quinasa-2 activada por quinasa MAP (MAPKAPK-2) ha sido identificada como una diana para la fosforilación de p38. Se ha demostrado que los ratones [Kotlyarov et al, Nat. Cell Biol. 1999, 1, 94-97] que carecen de MAPKAPK-2 liberan niveles reducidos de TNF-a, IL-1º, IL-6, IL-10 e IFN-y en respuesta al choque endotóxico mediado por LPS/galactosamina. La regulación de los niveles de estas citoquinas así como de COX-2 está en el nivel de ARNm. Los niveles de TNF-a están regulados por medio del control traduccional a través de elementos ricos en AU de la UTR-3' del ARNm de TNF-a, incrementando la señalización con MAPKAPK-2 la traducción del ARNm de TNF-a. La señalización con MAPKAPK2 conduce a un incremento de la estabilidad del ARNm para COX-2, IL-6 y proteína inflamatoria de macrófagos. MAPKAPK-2 determina la localización celular de la MAPK p38 así como la transducción de la señalización de MAPK p38, que posee una señal de localización nuclear en su extremo carboxilo y una señal de exportación nuclear como parte de su dominio autoinhibidor [Engel et al, EMBO J. 1998, 17, 3363-3371]. En células con estrés, MAPKAPK-2 y p38 MAPK migran al citoplasma desde el núcleo, esta migración solo se produce cuando la MAPK p38 es catalíticamente activa. Se cree que este evento está dirigido por la exposición de la señal de exportación nuclear MAPKAPK-2, como resultado de la fosforilación por MAPK p38 [Meng et al, J. Biol. Chem. 2002, 277, 37401-37405]. Adicionalmente la MAPK p38 conduce directamente o indirectamente a la fosforilación de diversos factores de transcripción que se cree que median la inflamación, incluyendo ATF1/2 (activando los factores de transcripción 1/2) , CHOP-10/GADD-153 (gen 153 inducible por detención del crecimiento y daño al ADN) , SAP-1 (proteína-1 accesoria del factor de respuesta de suero) y MEF2C (factor-2 potenciador de miocitos) [Foster et al, Drug News Perspect. 2000, 13, 488-497].
Se ha demostrado en varios casos que la inhibición de la actividad de la MAPK p38 por moléculas pequeñas, es útil para el tratamiento de diversos estados de enfermedad mediados por una producción inapropiada de citoquinas incluyendo artritis reumatoide, EPOC, asma e isquemia cerebral. Esta modalidad ha sido sujeto de numerosas revisiones [Salituro et al, Current Medicinal Chemistr y , 1999, 6, 807-823 y Kumar et al, Nature Reviews Drug Discover y 2003, 2, 717-726].
Se ha demostrado que los inhibidores de MAPK p38 son eficaces en modelos animales de artritis reumatoide, tales como artritis inducida por colágeno en ratas [Revesz et al, Biorg. Med. Chem. Lett., 2000, 10, 1261-1364] y artritis inducida por coadyuvante en ratas [Wadsworth et al, J. Pharmacol. Exp. Ther., 1999, 291, 1685-1691]. En modelos murinos de lesión pulmonar inducida por pancreatitis, el pretratamiento con un inhibidor de MAPK p38 redujo la liberación de TNF-a en las vías respiratorias y el edema pulmonar [Denham et al, Crit. Care Med., 2000, 29, 628 y Yang et al, Surger y , 1999, 126, 216]. La inhibición de MAPK p38 antes de la exposición a ovoalbúmina (OVA) en 5 ratones sensibilizados a OVA disminuyó la acumulación de citoquina y células inflamatorias en las vías respiratorias en un modelo de inflamación alérgica de las vías respiratorias, [Underwood et al, J. Pharmacol. Exp. Ther., 2000, 293, 281]. Se ha observado un aumento de actividad de la MAP quinasa p38 MAP en pacientes que padecen enfermedad inflamatoria intestinal [Waetzig et al, J. Immunol, 2002, 168, 5432-5351]. Se ha demostrado que los inhibidores de MAPK p38 son eficaces en modelos de rata de hipertrofia cardíaca [Behr et al, Circulation, 2001, 104,
1292-1298] e isquemia cerebral focal [Barone et al, J. Pharmacol. Exp. Ther., 2001, 296, 312-321].
Los autores de la presente invención han descubierto ahora un grupo de compuestos que son inhibidores potentes y selectivos de MAPK p38 (p38a, º, y y 5) y de las isoformas y variantes de empalme de las mismas, especialmente p38a, p38º y p38 º2. Los compuestos tienen por lo tanto uso en medicina, por ejemplo en el tratamiento y la 15 profilaxis de trastornos inmunitarios e inflamatorios descritos en la presente memoria. Los compuestos se caracterizan por la presencia en la molécula de un motivo de glicina a, a-disustituido o un motivo éster de glicina a, adisustituido que es hidrolizable por cualquier carboxilesterasa intracelular. Los compuestos de la invención que tienen el motivo de éster de glicina a, a-disustituido lipofílico cruzan la membrana celular, y son hidrolizados a ácido por las carboxilesterasas intracelulares. El producto de la hidrólisis polar se acumula en la célula puesto que no cruza fácilmente la membrana celular. Por lo tanto la actividad de la MAP quinasa p38 del compuesto es prolongada intensificada en el interior de la célula. Los compuestos de la invención están relacionados con los inhibidores de MAP quinasa p38 incluidos en las descripciones de la Solicitud de Patente Internacional WO 03076405, pero difieren en que los presentes compuestos tienen el motivo éster de aminoácido referido anteriormente.
Los compuestos de la invención también están relacionados con los descritos en la Solicitud de Patente Internacional copendiente Núm. WO 2007/129040. Los últimos compuestos tienen un motivo éster de glicina amonosustituido que también permite a los compuestos atravesar la membrana celular hacia el interior de la célula donde son hidrolizados al correspondiente ácido por las carboxilesterasas intracelulares. Sin embargo, esa publicación no sugiere que los productos conjugados de éster de glicina a, a-disustituidos puedan ser hidrolizados por las carboxilesterasas... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula (I) :
en donde:
G es -N= o -CH= D es un radical fenilo sustituido opcionalmente o piridinilo sustituido opcionalmente; 10 R6 es hidrógeno o alquilo C1-C3 sustituido opcionalmente; P representa hidrógeno y U representa un radical de fórmula (IA) ;
- A- (CH2) z-X1-L1-Y-NH-CR1R2R3 (IA)
en donde A representa un radical 1, 4-fenileno sustituido opcionalmente; z es 0 o 1; Y es un enlace, -C (=O) -, -S (=O) 2-, -C (=O) NR7-, -C (=S) -NR7, -C (=NH) NR7 o -S (=O) 2NR7- en donde R7 es hidrógeno o alquilo C1-C6 sustituido opcionalmente;
L1 es un radical divalente de fórmula - (Alk1) m (Q) n (Alk2) p- en donde m, n y p son independientemente 0 o 1, Q es (i) un radical carbocíclico o heterocíclico mono- o bicíclico divalente sustituido opcionalmente que tien.
5. 13 miembros anulares, o (ii) , en el caso en el que tanto m como p son 0, un radical divalente de fórmula -X2-Q1-o -Q1-X2- en donde X2 es -O-, S- o NRA- en donde RA es hidrógeno o alquilo C1-C3 sustituido opcionalmente, y
Q1 es un radical carbocíclico o heterocíclico mono- o bicíclico divalente sustituido opcionalmente que tien.
5. 13 miembros anulares, Alk1 y Alk2 representan independientemente radicales cicloalquilo C3-C7 divalentes sustituidos opcionalmente, o radicales alquileno C1-C6, alquenileno C2-C6, o alquinileno C2-C6 lineales o ramificados sustituidos opcionalmente que pueden contener opcionalmente o terminar en una conexión éter (-0-) , tioéter (-S-) o amino
(-NRA-) en donde RA es hidrógeno o alquilo C1-C3 sustituido opcionalmente; y X1 representa un enlace; -C (=O) ; o -S (=O) 2-; -NR4C (=O) -, -C (=O) NR4-, -NR4C (=O) NR5-, -NR4S (=O) 2-, o -S (=O) 2NR4- en donde R4 y R5 son independientemente hidrógeno o alquilo C1-C6 sustituido opcionalmente; R1 es un grupo éster que es hidrolizable por medio de una o más enzimas esterasas intracelulares a un grupo ácido carboxílico en donde el grupo éster tiene la fórmula - (C=O) OR14 en donde R14 es R8R9R10C- en donde (i) R8 es hidrógeno o sustituido opcionalmente alquil (C1-C3) - (Z1) a-[alquil (C1-C3) ]b- o alquenil (C2-C3) - (Z1) a[alquil (C1-C3) ]b- en donde a y b son independientemente 0 o 1 y Z1 es -O-, -S-, o -NR11- en donde R11 es hidrógeno o alquilo C1-C3; y R9 y R10 son independientemente hidrógeno o alquil (C1-C3) -;
(ii) R8 es hidrógeno o R12R13N-alquil (C1-C3) - sustituido opcionalmente en donde R12 es hidrógeno o alquilo C1-C3 y R13 es hidrógeno o alquilo C1-C3; o R12 y R13 junto con el nitrógeno al que están anclados forman un anillo heterocíclico monocíclico sustituido opcionalmente de 5 o 6 átomos anulares o un sistema anular heterocíclico bicíclico de 8 a 10 átomos anulares, y R9 y R10 son independientemente hidrógeno o alquil (C1-C3) -; o (iii) R8 y R9 tomados junto con el carbono al que están anclados forman un anillo carbocíclico monocíclico de 3 a 7 átomos anulares o un sistema anular carbocíclico bicíclico de 8 a 10 átomos anulares sustituidos opcionalmente, o un sistema anular carbocíclico monocíclico puenteado de 7 a 10 átomos anulares, y R10 es 45 hidrógeno; y en donde en los casos (i) , (ii) y (iii) anteriores, el término "alquilo" incluye fluoroalquilo; y uno de R2 y R3 es metilo, y el otro es metilo, etilo, o n- o iso-propilo; o R2 y R3 tomados junto con el carbono al que están anclados forman un anillo de a ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo; y en donde el término "sustituido" aplicado a cualquier fracción significa sustituido con hasta cuatro sustituyentes 50 compatibles, cada uno de los cuales se selecciona independientemente entre alquilo C1-C6, alcoxi C1-C6, hidroxi, hidroxialquilo C1-C6, mercapto, mercaptoalquilo C1-C6, alquil (C1-C6) tio, fenilo, halo, trifluorometilo, trifluorometoxi, nitro, nitrilo (-CN) , oxo, - COOH, -COORA, -CORA, -SO2RA, -CONH2, -SO2NH2, -CONHRA, -SO2NHRA, - CONRARB, -SO2NRARB, -NH2, -NHRA, -NRARB, -OCONH2, -OCONHRA, -OCONRARB, - NHCORA, -NHCOORA, -NRBCOORA, -NHSO2ORA, -NRBSO2OH, -NRBSO2ORA, - NHCONH2, -NRACONH2, -NHCONHRB, -NRACONHRB, -NHCONRARB, y -NRACONRARB en donde RA y RB son independientemente alquilo C1-C6, cicloalquilo C3-C6, fenilo o heteroarilo monocíclico que tiene 5 o 6 átomos anulares, o RA y RB cuando se anclan al mismo átomo de nitrógeno forman un grupo amino cíclico.
3. Un compuesto como se ha reivindicado en la reivindicación 1 o la reivindicación 2 en donde los sustituyentes opcionales en D y/o A se seleccionan entre flúor y cloro.
en donde R15 y R16 son independientemente hidrógeno o fluoro, y en donde z, X1, L1, Y, R1, R2 y R3 se definen como 15 en la reivindicación 1.
5. Un compuesto como se ha reivindicado en una cualquiera de las reivindicaciones anteriores en donde el radical -Y-L1-X1-[CH2]z-, es -CH2-, -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2-, -CH2O-, -CH2CH2O-, -CH2CH2CH2O-, -CH2CH2CH2CH2O-, -C (=O) -CH2-, -C (=O) -CH2O-, - C (=O) -NH-CH2-, o -C (=O) -NH-CH2O-.
6. Un compuesto como se ha reivindicado en una cualquiera de las reivindicaciones anteriores en donde R14 es metilo, trifluorometilo, etilo, n- o iso-propilo, n-, sec- o terc-butilo, ciclohexilo, alilo, biciclo[2, 2, 1]hept-2-ilo, 2, 3-dihidro1H-inden-2-ilo, fenilo, 2-, 3- o 4-piridilmetilo, N-metilpiperidin-4-ilo, tetrahidrofuran-3-ilo o metoxietilo.
7. Un compuesto como se ha reivindicado en una cualquiera de las reivindicaciones 1 a 5 en donde R14 es ciclopentilo.
8. Un compuesto como se ha reivindicado en la reivindicación 1 seleccionado del grupo que consiste en: N- (2-{4-[6-Amino-5- (2, 4-difluorobenzoil) -2-oxopiridin-1 (2H) -il]fenil}etil) -2-metilalaninato de ciclopentilo,
N- (2-{4-[6-Amino-5- (2, 4-difluorobenzoil) -2-oxopiridin-1 (2H) -il]-3, 5-difluorofenil}etil) -2-metilalaninato de ciclopentilo, N- (3-{4-[6-Amino-5- (2, 4-difluorobenzoil) -2-oxopiridin-1 (2H) -il]-3, 5-difluorofenoxi}propil) -2-metilalaninato de ciclopentilo, y sus sales farmacéuticamente aceptables.
9. Una composición farmacéutica que comprende un compuesto como se ha reivindicado en cualquiera de las reivindicaciones anteriores, junto con un portador farmacéuticamente aceptable.
10. Un compuesto como se ha reivindicado en una cualquiera de las reivindicaciones 1 a 8 para su uso en el
tratamiento de una enfermedad autoinmunitaria o inflamatoria. 40
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Procedimiento de compuestos antifúngicos, del 22 de Julio de 2020, de NQP 1598, Ltd: Procedimiento para preparar un compuesto de fórmula 5 ó 5*, o una mezcla de los mismos: **(Ver fórmula)** comprendiendo el método: (a) hacer reaccionar un compuesto […]
Productos terapéuticos basados en la lantionina sintetasa 2 tipo C, del 15 de Julio de 2020, de LANDOS BIOPHARMA, INC: Un compuesto de la fórmula: **(Ver fórmula)** o una sal o éster farmacéuticamente aceptable de este, en donde: Q es piperazina-1,4-diilo; […]
Derivados de piperidina en calidad de inhibidores de HDAC1/2, del 8 de Julio de 2020, de Regenacy Pharmaceuticals, Inc: Un compuesto de Fórmula IIIa: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde R1 se selecciona del grupo que consiste […]
Compuestos orgánicos, del 17 de Junio de 2020, de INTRA-CELLULAR THERAPIES, INC: Un compuesto de Fórmula I: **(Ver fórmula)** en forma libre o de sal, donde: R1 y R2 son independientemente H o alquilo C1-4 (por ejemplo, metilo o […]
Compuestos ahorradores de PPAR para el tratamiento de enfermedades metabólicas, del 3 de Junio de 2020, de Metabolic Solutions Development Company LLC (100.0%): Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: cada uno de R1 y R2 se selecciona independientemente entre […]
Uso de inhibidores de la PDE4 para la profilaxis y/o la terapia de la dislipoproteinemia y trastornos relacionados, del 27 de Mayo de 2020, de Albert-Ludwigs-Universität Freiburg: Inhibidor específico de la fosfodiesterasa 4 (PDE 4) para uso en el tratamiento profiláctico o terapéutico de la dislipoproteinemia, en donde el inhibidor […]
Nuevos usos terapéuticos de derivados de la bencilidenguanidina para el tratamiento de proteopatías, del 20 de Mayo de 2020, de InFlectis BioScience: Compuesto de la fórmula (I), o una sal farmacéuticamente aceptable del mismo, **(Ver fórmula)** o un tautómero de los mismos donde: […]