Conjugados de amatoxinas con ligadores mejorados.
Conjugado que comprende un resto de unión a una diana unido a través de un ligador L a una amatoxina,
en el que el ligador L está conectado a la amatoxina a través de
(i) el átomo de C del aminoácido de amatoxina 1, particularmente a través de un enlace amida;
(ii) un átomo de oxígeno unido al átomo de C del aminoácido de amatoxina 3, particularmente a través de un enlace éster, un enlace éter o un enlace uretano; o
(iii) el átomo de C 6' del aminoácido de amatoxina 4, particularmente a través de un átomo de oxígeno unido al átomo de C 6' del aminoácido de amatoxina 4;
en cada caso en el que el ligador L está conectado al resto de unión a una diana a través de un resto urea.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10012573.
Solicitante: Heidelberg Pharma AG.
Nacionalidad solicitante: Alemania.
Dirección: Schriesheimer Strasse 101 68526 Ladenburg ALEMANIA.
Inventor/es: MULLER, CHRISTOPH, SIMON, WERNER, Anderl,Jan Dr.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K47/48
- A61P35/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
PDF original: ES-2402254_T3.pdf
Fragmento de la descripción:
Conjugados de amatoxinas con ligadores mejorados Campo de la invención La invención se refiere a terapia tumoral. En un aspecto, la presente invención se refiere a conjugados de una amatoxina y un resto de unión a una diana, por ejemplo un anticuerpo, conectado por un ligador que comprende un resto urea, que son útiles en el tratamiento de cáncer. En un aspecto adicional, la invención se refiere a composiciones farmacéuticas que comprenden tales conjugados.
Antecedentes de la invención Las amatoxinas son péptidos cíclicos compuestos por 8 aminoácidos. Pueden aislarse de setas Amanita phalloides o prepararse sintéticamente. Las amatoxinas inhiben específicamente la ARN polimerasa II dependiente de ADN de células de mamíferos, y de ese modo también la transcripción y biosíntesis de proteínas de las células afectadas. La inhibición de la transcripción en una célula provoca la detención del crecimiento y la proliferación. Aunque no está unido covalentemente, el complejo entre amanitina y ARN polimerasa II es muy fuerte (KD = 3 nM) . La disociación de la amanitina de la enzima es un proceso muy lento, haciendo por tanto que la recuperación de una célula afectada sea improbable. Cuando la inhibición de la transcripción dura demasiado, la célula experimentará muerte celular programada (apoptosis) .
El uso de amatoxinas como restos citotóxicos para terapia tumoral ya se había explorado en 1981 acoplando un anticuerpo anti-Thy 1.2 a -amanitina usando un ligador unido al anillo de indol del Trp (aminoácido 4; véase la figura 1) a través de diazotación (Davis & Preston, Science 1981, 213, 1385-1388) . La solicitud de patente EP 1 859 811 A1 (publicada el 28 de noviembre de 2007) describe conjugados, en los que el átomo de C del aminoácido de amatoxina 1 de -amanitina se acopló directamente, es decir, sin una estructura de ligador, a albúmina o a anticuerpo monoclonal HEA125, OKT3 o PA-1. Además, se mostró el efecto inhibidor de estos conjugados sobre la proliferación de células de cáncer de mama (MCF-7) , células de linfoma de Burkitt (Raji) , y células de linfoma T (Jurkat) . Se sugirió el uso de ligadores, incluyendo ligadores que comprenden elementos tales como restos amida, éster, éter, tioéter, disulfuro, urea, tiourea, hidrocarburo y similares, pero no se mostraron realmente tales constructos, y no se proporcionaron más detalles, tales como sitios de unión en las amatoxinas.
El documento WO2007/121326 A2 da a conocer un conjugado que comprende un oligonucleótido formador de triple hélice (TFO) que se une de manera covalente al átomo de C gama de beta-amanitina a través de un enlace que contiene amida.
Se sabe que las amantoxinas son relativamente no tóxicas cuando se acoplan a portadores de biomoléculas grandes, tales como moléculas de anticuerpos, y que ejercen su actividad citotóxica sólo después de que se escinda el portador de biomoléculas. En vista de la toxicidad de las amatoxinas, particularmente para células del hígado, es de máxima importancia que los conjugados de amatoxina para terapia tumoral dirigida permanezcan altamente estables tras la administración en plasma, y que la liberación de la amatoxina se produzca tras la internalización en las células diana. En este contexto, mejoras menores de la estabilidad del conjugado pueden tener consecuencias drásticas para la ventana terapéutica y la seguridad de los conjugados de amatoxina para enfoques terapéuticos.
Objeto de la invención Por tanto, había una gran necesidad en la técnica anterior de conjugados de resto de unión a una diana-amatoxina que fueran estables en plasma, de modo que se minimicen los efectos secundarios perjudiciales en células no diana.
Sumario de la invención En un primer aspecto la presente invención se refiere a un conjugado que comprende un resto de unión a una diana unido a través de un ligador L a una amatoxina, en el que el ligador L está conectado a la amatoxina a través de
(iii) el átomo de C 6’ del aminoácido de amatoxina 4, particularmente a través de un átomo de oxígeno unido al átomo de C 6’ del aminoácido de amatoxina 4;
en cada caso en el que el ligador L está conectado al resto de unión a una diana a través de un resto urea.
En un segundo aspecto, la presente invención se refiere a una composición farmacéutica que comprende el conjugado según la presente invención.
En otro aspecto, la presente invención se refiere a una molécula de conjugación con amatoxina que comprende un ligador L conectado a una amatoxina a través de
(iii) el átomo de C 6’ del aminoácido de amatoxina 4, particularmente a través de un átomo de oxígeno unido al átomo de C 6’ del aminoácido de amatoxina 4;
en cada caso en el que el ligador L comprende un derivado de ácido carbámico -NH-C (O) -X, en el que X es un grupo saliente que puede reemplazarse por una amina primaria de un resto de unión a una diana.
Aún en otro aspecto, la presente invención se refiere a un método para sintetizar un conjugado de la presente invención, que comprende la etapa de hacer reaccionar una molécula de conjugación con amatoxina de la presente invención con un resto de unión a una diana que comprende un grupo amino primario.
Breve descripción de los dibujos La figura 1 muestra las fórmulas estructurales de diferentes amatoxinas. Los números en negrita (1 a 8) designan la numeración convencional de los ocho aminoácidos que forman la amatoxina. También se muestran las designaciones convencionales de los átomos en los aminoácidos 1, 3 y 4 (letras griegas a , letras griegas a y números desde 1’ hasta 7’, respectivamente) . La figura 2 muestra la actividad citotóxica de diferentes conjugados de amanitina-herceptina usando diferentes restos ligadores sobre células SKOV-3 en un ensayo de BrdU tras incubación durante 72 h.
La figura 3 muestra la actividad citotóxica de diferentes conjugados de amanitina-herceptina usando diferentes restos ligadores sobre células SK-BR-3 en un ensayo de BrdU tras incubación durante 72 h.
La figura 4 muestra la actividad citotóxica de diferentes conjugados de amanitina-herceptina usando diferentes restos ligadores sobre células NCI-N87 en un ensayo de BrdU tras incubación durante 72 h.
La figura 5 muestra la actividad citotóxica de diferentes conjugados de amanitina-herceptina usando diferentes restos ligadores sobre células MDA-MB231 en un ensayo de BrdU tras incubación durante 72 h.
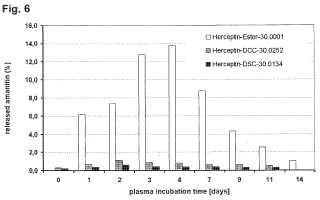
La figura 6 y la figura 7 muestran la cantidad de amanitina liberada de diferentes conjugados de amanitinaherceptina usando diferentes restos ligadores tras incubación en plasma durante hasta 14 días.
La figura 8 muestra una comparación de la actividad citotóxica de diferentes conjugados de amanitina-herceptina usando diferentes restos ligadores sobre células SKOV-3 en un ensayo de BrdU antes y después de la incubación en plasma.
La figura 9 muestra una comparación de la actividad de dos conjugados de amanitina-herceptina diferentes usando diferentes restos ligadores in vivo en un modelo de xenoinjerto de SKOV-3.
Descripción detallada de la invención A menos que se defina lo contrario, todos los términos técnicos y científicos usados en el presente documento tienen los mismos significados que entiende comúnmente un experto habitual en la técnica.
Preferiblemente, los términos usados en el presente documento se definen tal como se describe en “A multilingual glossar y of biotechnological terms: (IUPAC Recommendations) ”, Leuenberger, H.G.W, Nagel, B. y Kölbl, H. eds. (1995) , Helvetica Chimica Acta, CH-4010 Basilea, Suiza) .
Durante toda esta memoria descriptiva y las reivindicaciones que siguen, a menos que el contexto requiera lo contrario, la palabra “comprenden”, y variaciones tales como “comprende” y “que comprende”, se entenderá que implican la inclusión de un número entero o etapa o grupo de números enteros o etapas establecidos pero no la exclusión de cualquier otro número entero o etapa o grupo de números enteros o etapas.
Se... [Seguir leyendo]
Reivindicaciones:
1. Conjugado que comprende un resto de unión a una diana unido a través de un ligador L a una amatoxina, en el que el ligador L está conectado a la amatoxina a través de
(iii) el átomo de C 6’ del aminoácido de amatoxina 4, particularmente a través de un átomo de oxígeno unido al átomo de C 6’ del aminoácido de amatoxina 4;
en cada caso en el que el ligador L está conectado al resto de unión a una diana a través de un resto urea.
2. Conjugado según la reivindicación 1, en el que el conjugado tiene una estructura seleccionada de una de las siguientes estructuras:
(ii) amatoxina-C -O-C (O) -L-NH-C (O) -NH-resto de unión a una diana;
(iii) amatoxina-C -O-L-NH-C (O) -NH-resto de unión a una diana;
(iv) amatoxina-C -O-C (O) -NH-L-NH-C (O) -NH-resto de unión a una diana; y
(v) amatoxina-6’C-O-L-NH-C (O) -NH-resto de unión a una diana.
3. Conjugado según la reivindicación 1 ó 2, en el que el resto de unión a una diana está conectado al ligador L a través de un grupo amino presente en el resto de unión a una diana, en el que dicho grupo amino forma parte de dicho resto urea.
o análogos de los mismos.
5. Conjugado según una cualquiera de las reivindicaciones 1 a 4, en el que el ligador L es un grupo alquileno, heteroalquileno, alquenileno, heteroalquenileno, alquinileno, heteroalquinileno, cicloalquileno, heterocicloalquileno, arileno, heteroarileno, aralquileno o heteroaralquileno, opcionalmente sustituido.
6. Conjugado según una cualquiera de las reivindicaciones 1 a 5, en el que el ligador L comprende un resto seleccionado de uno de los siguientes restos: un resto disulfuro, un resto éter, un resto amina, un resto éster, un resto carboxamida, un resto uretano y un resto urea.
7. Conjugado según una cualquiera de las reivindicaciones 1 a 6, en el que el resto de unión a una diana se une específicamente a un epítopo que está presente en una célula tumoral, particularmente en el que el resto de unión a una diana se une específicamente a un epítopo de molécula de adhesión de células epiteliales (EpCAM) .
8. Conjugado según una cualquiera de las reivindicaciones 1 a 7, en el que el resto de unión a una diana se selecciona del grupo que consiste en:
(i) anticuerpo o fragmento de unión a antígeno del mismo;
(ii) proteína de tipo anticuerpo; y
(iii) aptámero de ácido nucleico.
9. Conjugado según la reivindicación 8, en el que el anticuerpo o el fragmento de unión a antígeno del mismo se selecciona de un diacuerpo, un tetracuerpo, un nanocuerpo, un anticuerpo quimérico, un anticuerpo desinmunizado, un anticuerpo humanizado o un anticuerpo humano.
10. Conjugado de resto de unión a una diana-toxina según la reivindicación 8 ó 9, en el que el fragmento de unión a antígeno se selecciona del grupo que consiste en Fab, F (ab’) 2, Fd, Fv, Fv de cadena sencilla y Fv unidos por disulfuros (dsFv) .
11. Conjugado según una cualquiera de las reivindicaciones 1 a 10, para su uso como medicamento.
12. Conjugado según una cualquiera de las reivindicaciones 1 a 11, para el tratamiento de cáncer en un paciente, en el que el cáncer se selecciona del grupo que consiste en cáncer pancreático, colangiocarcinoma, cáncer de
mama, cáncer colorrectal, cáncer de pulmón, cáncer de próstata, cáncer de ovario, cáncer de estómago, cáncer de riñón, melanoma maligno, leucemia y linfoma maligno.
13. Composición farmacéutica que comprende el conjugado según una cualquiera de las reivindicaciones 1 a 10 y
que comprende además uno o más diluyentes, portadores, excipientes, cargas, aglutinantes, lubricantes, 5 deslizantes, disgregantes, adsorbentes; y/o conservantes farmacéuticamente aceptables.
14. Molécula de conjugación con amatoxina que comprende un ligador L conectado a una amatoxina a través de
(ii) un átomo de oxígeno unido al átomo de C 6 del aminoácido de amatoxina 3, particularmente a través de un enlace éster, un enlace éter o un enlace uretano; o
(iii) el átomo de C 6’ del aminoácido de amatoxina 4, particularmente a través de un átomo de oxígeno unido al átomo de C 6’ del aminoácido de amatoxina 4;
en cada caso en el que el ligador L comprende un derivado de ácido carbámico -NH-C (O) -X, en el que X es un grupo saliente que puede reemplazarse por una amina primaria de un resto de unión a una diana.
15. Molécula de conjugación con amatoxina según la reivindicación 14, en la que X se selecciona de: -tbutiloxilo,
succinimidiloxilo, -1-O-succinimidiloxi-3-sulfonato (-Sulfo-NHS) , -O- (4-nitrofeniloxilo) , -O- (3-nitrofeniloxilo) , -O- (2, 4dinitrofeniloxilo) , -O- (2, 4-dicloro-6-nitrofeniloxilo) , -pentafluorofeniloxilo, -pentaclorofeniloxilo, -O- (2, 4, 5triclorofeniloxilo) , -O- (3, 4-dihidro-3-hidroxi-4-oxo-1, 2, 3-benzotriazin-3-ilo) , -O- (endo-1-hidroxi-5-norbornen-2, 3dicarboximida-1-ilo) , -1-ftalimidoiloxilo, -1-benzotriazoliloxilo, -1- (7-aza-benzotriazolilo) oxilo) y -N-imidazolilo.
16. Método para sintetizar un conjugado según una cualquiera de las reivindicaciones 1 a 12, que comprende la etapa de hacer reaccionar una molécula de conjugación con amatoxina según la reivindicación 14 ó 15 con un resto de unión a una diana que comprende un grupo amino primario.
Patentes similares o relacionadas:
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Aril éteres y usos de los mismos, del 22 de Julio de 2020, de Peloton Therapeutics, Inc: Un compuesto de formula Vd: **(Ver fórmula)** ç o una sal farmaceuticamente aceptable del mismo, en donde: R1 es arilo o heteroarilo; […]