SUSPENSIÓN DE PARTÍCULAS DE HERRUMBRE VERDE NO ESTEQUIOMÉTRICA.
Suspensión de nanopartículas no estequiométricas de herrumbre verde.
Las herrumbres verdes (Green Rusts), son sales de hidróxidos dobles laminares de hierro II y III. En su forma estequiométrica aislable, la relación entre hierro II y hierro III es de 2 en carbonato y sulfato y de 3 en cloruro. Se reivindican las aplicaciones de una suspensión de sales de partículas de herrumbre verde "no estequiométrica", donde la proporción estructural entre Fe(II)/Fe(III) es mayor que la estequiométrica. Tal suspensión, utilizada en exceso de ión ferroso, posee propiedades extraordinarias diversas a las de sus congéneres estequiométricas. Reduce nitratos a nitrógeno suavemente y nitritos a nitrógeno a velocidad cien veces mayor que los compuestos estequiométricos que las reducen a amonio. Reduce el agua a hidrogeno y el nitrógeno gas hasta amoniaco en medio acuoso y temperatura y presión ambientes con rendimiento del orden del 50%. Se reivindica su aplicación en síntesis química general y en remediación medioambiental, en la producción de hidrógeno y la producción de amoniaco.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201100422.
Solicitante: DR CANICIO CONSULTING CHEMIST, S.L.
Nacionalidad solicitante: España.
Inventor/es: CANICIO CHIMENO,JOSE ALFONSO, CANICIO BARDOLET,Ruth, SEMPERE NOMEN,Bernat, ÁLVAREZ GONZÁLEZ,Nancy, ONUKI ESTEBAN,Olga, CAMPAS CASALI,Mª Mercè.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01D53/58 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01D SEPARACION (separación de sólidos por vía húmeda B03B, B03D, mesas o cribas neumáticas B03B, por vía seca B07; separación magnética o electrostática de materiales sólidos a partir de materiales sólidos o de fluidos, separación mediante campos eléctricos de alta tensión B03C; aparatos centrifugadores B04B; aparato de vórtice B04C; prensas en sí para exprimir los líquidos de las sustancias que los contienen B30B 9/02). › B01D 53/00 Separación de gases o de vapores; Recuperación de vapores de disolventes volátiles en los gases; Depuración química o biólogica de gases residuales, p. ej. gases de escape de los motores de combustión, humos, vapores, gases de combustión o aerosoles (recuperación de disolventes volátiles por condensación B01D 5/00; sublimación B01D 7/00; colectores refrigerados, deflectores refrigerados B01D 8/00; separación de gases difícilmente condensables o del aire por licuefacción F25J 3/00). › Amoniaco.
- B82Y30/00 B […] › B82 NANOTECNOLOGIA. › B82Y USOS O APLICACIONES ESPECIFICOS DE NANOESTRUCTURAS; MEDIDA O ANALISIS DE NANOESTRUCTURAS; FABRICACION O TRATAMIENTO DE NANOESTRUCTURAS. › Nano tecnología para materiales o ciencia superficial, p.ej. nano compuestos.
- C01B3/06 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01B ELEMENTOS NO METALICOS; SUS COMPUESTOS (procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01B 3/00 Hidrógeno; Mezclas gaseosas que contienen hidrógeno; Separación del hidrógeno a partir de mezclas que lo contienen; Purificación del hidrógeno (producción de gas de agua o gas de síntesis a partir de materias carbonosas sólidas C10J). › por reacción de compuestos inorgánicos que tienen un hidrógeno enlazado electropositivamente, p. ej. de agua, ácidos, bases, amoniaco, con agentes reductores inorgánicos (por electrólisis del agua C25B 1/04).
- C01G49/02 C01 […] › C01G COMPUESTOS QUE CONTIENEN METALES NO CUBIERTOS POR LAS SUBCLASES C01D O C01F (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base C01B 37/00; compuestos que tienen propiedades de tamices moleculares y de cambiadores de base, p. ej. zeolitas cristalinas, C01B 39/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C21B, C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01G 49/00 Compuestos de hierro. › Oxidos; Hidróxidos.
- C02F1/70 C […] › C02 TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS. › C02F TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS (procedimientos para transformar las sustancias químicas nocivas en inocuas o menos perjudiciales, efectuando un cambio químico en las sustancias A62D 3/00; separación, tanques de sedimentación o dispositivos de filtro B01D; disposiciones relativas a las instalaciones para el tratamiento del agua, agua residual o de alcantarilla en los buques, p. ej. para producir agua dulce, B63J; adición al agua de sustancias para impedir la corrosión C23F; tratamiento de líquidos contaminados por radiactividad G21F 9/04). › C02F 1/00 Tratamiento del agua, agua residual o de alcantarilla (C02F 3/00 - C02F 9/00 tienen prioridad). › por reducción.
PDF original: ES-2390308_A1.pdf
Fragmento de la descripción:
Suspensión de partículas de herrumbre verde no estequiométrica Descripción
Sector de la técnica
La invención se encuadra en los sectores de la síntesis química y la producción industrial de combustibles, Hidrógeno y Amoníaco!, fertilizantes y en general de la obtención industrial, por reducción química, de todo tipo
de compuestos orgánicos e inorgánicos. La invención se encuadra aSimismo, en el sector de la nanotecnología, la remediación medioambiental, el tratamiento y potabilización de aguas y la Ecotecnología en general. La invención contempla como objeto la reducción química desustancias mediante un reactivo formado por micro o nano partículas de herrumbre verde no estequiométrica en suspensión acuosa, en suspensión en disolvente, o absorbidas sobre un soporte sólido en fase sólida. El reactivo es preparado desde materias primas (hierro ferroso y hierro férrico) ubicuas y asequibles y resulta de fabricación fácil, simple y muy económica. Debe entenderse por herrumbre verde una sal de hidróxido doble laminar ferroso férrico (Layered Double Hydroxide) , donde la relación estructural entre hierro (n) y hierro (nI) es superior a la estequiométrica, usual, aunque no exclusivamente, superior a 2, aunque dependiendo de la sal.
Tal suspensión es capaz de reducir de suerte rápida y específica, compuestos que, de ordinario, no son susceptibles de tal reducción rápida, económica y específica, o lo son en condiciones mucho más drásticas y energéticamente mucho más onerosas.
Específicamente, la invención se aplicará a los tratamientos de agua para eliminar nitratos y especialmente nitritos y por ende, a procesos de tratamiento de agua para eliminación de excesos de nitratos y nitritos mediante su conversión en nitrógeno gas. En suma a la potabilización, a la depuración de aguas residuales para vertido a cauce publico, la remediación de acuíferos, lagos y embalses contaminados, la reutilización de las aguas urbanas y de las empleadas en acuicultura y a la destrucción de los residuos de tratamiento de las plantas de desnitrificación por membrana.
Específicamente, la invención se aplicará a la producción de hidrógeno por descomposición de agua mediante luz solar o mediante otros dispositivos en los que la energía global precisa para descomponer el agua sea inferior a la necesaria para hacerlo directamente por electrolisis.
Específicamente, la invención se aplicará a la producción de amoníaco por reducción del nitrógeno molecular del aire en condiciones en extremo mas suaves y menos energéticamente onerosas que en el proceso de Haber
1 La oxidación del amoníaco mediante oxígeno del aire puede conducir a nitrógeno y agua mediante la reacción redox, 4NH3 + 302 = 2N2 + 6 H20. Esta reacción, producida en una célula de combustible, libera energía eléctrica susceptible de ser utilizada para todo tipo de aplicaciones incluso motrices (coche de amoníaco) o para la obtención de energía térmica de suerte idéntica y alternativa al uso de hidrógeno para los mismos fines según la reacción 2H2 + O2 = 2H20.
y Bosch de síntesis del amoníaco. La suspenslon reductora para la que se solicita protección legal en todas sus formas de uso, es capaz de reducir el nitrógeno gas disuelto en el agua, aún a temperatura y presión ambientes, con rendimiento del orden del 50 %. Se producen hoy del orden de cien millones de toneladas anuales de amoníaco mediante el proceso de Haber y Bosch. El procedimiento de Haber y Bosch de producción de amoníaco opera por reacción del nitrógeno gas del aire con hidrógeno, obtenido este de la reacción de vapor de agua antaño con carbón al rojo y hoy por "steam reforming" del metano, pero a presiones de entre 500 y 1000 atmósferas y temperaturas de 500-6000 c., para obtener un rendimiento por paso del 17 %. La dicha síntesis de Haber y Bosch permite alimentar -mediante la fabricación de abonos nitrogenados -al 50 % de la humanidad al coste de consumir del orden del 5% de gas natural (C02 a la atmósfera) y del consumo de del orden del 2 % del consumo mundial de energía.
El procedimiento para el que se solicita protección legal de reducción del nitrógeno del aire con la suspensión de partículas de herrumbre verde no estequiométrica opera a presión y temperatura ambientes con rendimiento del orden del 50 %.
Estado de la técnica
a) eliminación de nitratos y nitritos del agua por conversión en nitrógeno gas.
La legislación europea permite un máximo de 50 ppm de nitrato en agua de uso de boca. Existen al presente, diversos procedimientos conocidos para la eliminación del exceso de nitratos disueltos en agua: destilación, intercambio iónico, ósmosis inversa y numerosos procesos biológicos en los que se eliminan los nitratos mediante microorganismos cultivados en al agua a tratar. Empero, ninguno de los procedimientos es, en realidad, totalmente satisfactorio y eficiente y la eliminación económica de nitratos del agua, a gran escala, constituye aún un problema solo parcialmente resuelto.
Una alternativa es la reducción química del nitrato a nitrógeno elemental
Sin embargo, la reducción química del nitrato no transcurre de forma unívoca; a menudo el producto de reducción no es el nitrógeno gas elemental sino que conjunta o alternativamente, se produce un producto nitrogenado aún mas tóxico que el nitrato: el amoniaco, NH3, según:
El amoniaco es un producto extremadamente tóxico e indeseable en agua, por lo que si la reducción química del nitrato no transcurre de forma unívoca hasta nitrógeno gas, inocuo, la reducción química de los nitratos agrava en realidad el problema de la toxicidad del agua derivada de la presencia de aquellos. La toxicidad del producto de reducción, el amoniaco, es mucho mayor que la del producto a eliminar: el ion nitrato.
Esta es la circunstancia que ha limitado el uso de la reducción química para la eliminación de nitratos: la ausencia de procedimientos de remediación a escala industrial que permitan su reducción directa y unívoca a nitrógeno gas. En tal escenario de la técnica, la aplicación de reducción química cómo medio de eliminación de nitrato, implica y conlleva la eliminación del amoniaco simultáneamente producido, lo que complica el procedimiento de depuración. Así, la reducción química, al estado de la técnica actual, es muy poco utilizada en el tratamiento de aguas en cuanto a la eliminación de nitratos se refiere. La clave pues de la posibilidad de uso de la reducción química para la remediación de aguas con exceso de contenido en nitratos, radica en la invención de un procedimiento selectivo de reducción -un reductor selectivo -de nitratos a nitrógeno gas sin formación de amoniaco.
La suspensión -en todas las formas de actuación reivindicadas-de herrumbre verde no estequiométrica, reduce en cinco minutos cantidades del orden de 2 mM/1 de nitritos a nitrógeno gas.
Los nitratos en exceso en el agua, son susceptibles de ser convertidos cuantitativamente en nitritos mediante arte conocid02, o también -a velocidad menor y con limitaciones en la concentración -mediante la suspensión de herrumbre verde no estequiométrica. La reducción de los nitritos obtenidos por uno u otro procedimiento, o por otro arte público conocido, mediante la suspensión de partículas objeto de solicitud de protección legal, conduce cuantitativamente a nitrógeno gas.
b) . obtención de Hidrógeno.
El Hidrógeno, ha sido reivindicado cómo el combustible ideal para combatir el cambio climático debido a la acumulación atmosférica de CO2, sin renunciar al uso extendido de máquinas de combustión interna. Es la obvia alternativa no contaminante al uso de combustibles fósiles.
Que el agua puede ser reducida produciendo hidrógeno, no es en sí novedad tecnológica ninguna. La electrolisis, por ejemplo, descompone el agua en sus componentes Oxígeno e Hidrógeno. Ello, no obstante, resulta caro y en realidad, en atención al origen fósil de la inmensa mayor parte de la energía eléctrica, para nada resuelve el problema de las emisiones de CO2 si el hidrógeno no se obtiene mediante energía nuclear o renovable. El método principal de obtención de hidrógeno es el steam reforming del gas natural: del metano. Obviamente, el procedimiento,... [Seguir leyendo]
Reivindicaciones:
1. Micro o nanopartículas de una sal de hidróxido doble laminar formada por iones ferrosos y férricos, caracterizadas porque la relación molar entre los iones ferrosos y los iones férricos es superior a 2 cuando el anión de la sal es orgánico o inorgánico excepto el cloruro, y dicha relación molar es superior a 3 cuando el anión es cloruro.
2. Micro o nanopartículas según la reivindicación 1, caracterizadas porque la relación molar entre los iones ferrosos y los iones férricos está comprendida entre 5 y 20.
3. Micro o nanopartículas según la reivindicación 2, caracterizadas porque la relación molar entre los iones ferrosos y los iones férricos está comprendida entre 10 y 15.
4. Micro o nanopartículas según la reivindicación 2, caracterizadas porque la relación molar entre los iones ferrosos y los iones férricos es 11
o 13.
5. Micro o nanopartículas según cualquiera de las reivindicaciones 1 a 4, caracterizadas porque el anión es cloruro, sulfato o carbonato.
6. Micro o nanopartículas según cualquiera de las reivindicaciones 1 a S, caracterizadas porque se encuentran adsorbidas sobre una sustancia hidroxilada.
7. Micro o nanopartículas según la reivindicación 6, caracterizadas la sustancia hidroxilada se selecciona entre el grupo formado por polioles, polímeros hidroxilados, y polímeros oxietilenados.
8. Micro o nanopartículas según la reivindicación 7, caracterizadas porque el poliol es glicerina.
9. Micro o nanopartículas según la reivindicación 7, caracterizadas porque el polímero hidroxilado es celulosa, hemicelulosa o celulosa químicamente modificada.
10. Micro o nanopartículas según cualquiera de las reivindicaciones 1 a 5, caracterizadas porque se encuentran en forma de suspensión acuosa.
11. Micro o nanopartículas según cualquiera de las reivindicaciones 1 a 5, caracterizadas porque se encuentran en forma de suspensión no acuosa.
12. Procedimiento para preparar micro o nanopartículas según cualquiera de las reivindicaciones 1 a 11, caracterizado porque comprende las etapas:
a) preparar una solución de una sal de iones ferrosos en un disolvente acuoso anóxico,
b) añadir a la solución obtenida en la etapa a) una cantidad de una solución de una sal de iones férricos férrica en un disolvente acuoso anóxico, de modo que la relación molar entre los iones ferrosos y los iones férricos es superior a 2 cuando el anión de la sal es orgánico o inorgánico excepto el cloruro, y superior a 3 cuando el anión es cloruro, y
c) ajustar con una base el pH a un valor de pH comprendido entre 7 y 8, 5, d) separar las micro o nanopartículas formadas en la etapa c) y, en caso necesario, e) suspender las micro o nanopartículas formadas en la etapa c) en un disolvente acuoso, o f) suspender las micro o nanopartículas formadas en la etapa c) en un disolvente no acuoso, o g) adsorber las micro o nanopartículas formadas en la etapa c) sobre una sustancia hidroxilada.
13. Procedimiento según la reivindicación 12, caracterizado porque la base se selecciona de entre el grupo formado por carbonatos, bicarbonatos, hidróxidos y óxidos alcalinos o alcalino térreos.
14. Procedimiento según la reivindicación 13, caracterizado porque la relación molar de oxidrilos de la base con respecto a los iones ferrosos está comprendida entre 2 y 3.
15. Procedimiento para preparar micro o nanopartículas según cualquiera de las reivindicaciones 1 a 11, caracterizado porque comprende la electroxidación de un ánodo de hierro en condiciones alcalinas a un pH comprendido entre 8 y 14, en donde los iones ferrosos son oxidados a iones férricos por oxigeno de modo que la relación molar entre los iones ferrosos y los iones férricos es: superior a 2 cuando el anión es orgánico o inorgánico excepto el cloruro, y superior a 3 cuando el anión es cloruro.
16. Uso de las micro o nanopartículas de cualquiera de las reivindicaciones 1 a 11 como reductor.
17. Uso según la reivindicación 16, caracterizado porque el exceso de iones ferrosos es de 2 a 20 veces molar con respecto a la molécula a reducir.
18. Uso de las micro o nanopartículas de cualquiera de las reivindicaciones 1 a 11 para reducir nitratos y nitritos del agua.
19. Uso de las micro o nanopartículas de cualquiera de las reivindicaciones 1 a 11 para reducir agua y producir hidrógeno.
20. Uso de las micro o nanopartículas de cualquiera de las reivindicaciones 1 a 11 para reducir nitrógeno molecular del aire y producir amoníaco.
Patentes similares o relacionadas:
Método para producir borohidruro metálico e hidrógeno molecular, del 11 de Marzo de 2020, de H2Fuel Cascade B.V: Un método para producir un borohidruro metálico, en donde el método comprende: A1. Proporcionar hidróxido metálico, B2O3 y H2 para permitir que un proceso de síntesis […]
Sistema de extracción de oxígeno para un recipiente, del 18 de Diciembre de 2019, de Amcor Rigid Plastics USA, LLC (The Corporation Trust Company): Un recipiente que comprende: un cuerpo que tiene un volumen interior, incluyendo dicho cuerpo una porción superior que tiene una pared lateral cilíndrica […]
Uso de un material a base de magnesio para producir dihidrógeno o electricidad, del 4 de Diciembre de 2019, de Université de Bordeaux: Uso de un material para producir hidrógeno o electricidad, comprendiendo el material , al menos al 50 % en masa, un reactivo destinado a […]
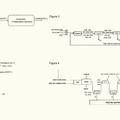 Producción de sintegas mediante un proceso de reducción de CO2, del 28 de Agosto de 2019, de POLITECNICO DI MILANO: Un proceso para producir gas de síntesis que comprende la reacción endotérmica entre CO2 y H2S, de acuerdo con el siguiente esquema de reacción […]
Producción de sintegas mediante un proceso de reducción de CO2, del 28 de Agosto de 2019, de POLITECNICO DI MILANO: Un proceso para producir gas de síntesis que comprende la reacción endotérmica entre CO2 y H2S, de acuerdo con el siguiente esquema de reacción […]
Un sistema y un procedimiento para generar hidrógeno, del 12 de Junio de 2019, de DRAGE & MATE INTERNATIONAL, S.L: Un sistema para generar hidrógeno a partir de agua, que comprende: (a) un material estructural para soportar: un reactivo primario en estado […]
Procedimiento para el suministro de dihidrógeno a partir de silicio hidrogenado, del 10 de Abril de 2019, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Uso de un silicio hidrogenado en forma de un material sólido que tiene al menos una dimensión mayor que 0,5 mm, obteniéndose dicho silicio hidrogenado […]
Procedimiento para la síntesis de hidrógeno, del 20 de Febrero de 2019, de VITO NV: Un procedimiento para la síntesis de gas hidrógeno (H2) en un reactor en condiciones hidrotérmicas, que comprende (a) poner en contacto hierro metálico (Fe0) y/o […]
Material compuesto para la generación hidrolítica de hidrógeno, dispositivo para la generación hidrolítica de hidrógeno, procedimiento para la generación de hidrógeno, dispositivo para la generación de energía eléctrica así como posibilidades de uso, del 30 de Enero de 2019, de FRAUNHOFER-GESELLSCHAFT ZUR FORDERUNG DER ANGEWANDTEN FORSCHUNG E.V.: Material compuesto para la generacion hidrolitica de hidrogeno, que contiene o esta compuesto por a) al menos un hidruro de metal que contiene metal alcalinoterreo, […]