Recipiente de muestras para análisis.
Soporte de biochips que comprende una placa de soporte (3) con por lo menos una cámara de reacción tridimensional (5),
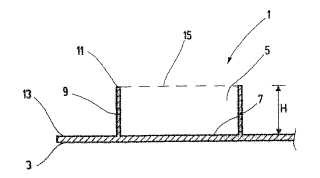
en donde la cámara de reacción (5) está formada por un fondo (7) y el volumen abierto por arriba de la cámara de reacción (5) está abarcado lateralmente por las paredes laterales (9), en donde la relación entre la superficie (F) del fondo (7) y la altura (H) de las paredes laterales (9) es mayor o igual a 30, de preferencia mayor de 50, y en donde el fondo (7) y/o por lo menos una pared lateral (9) de por lo menos una cámara de reacción (5) está ejecutada como matriz de unión con un grupo funcional que permite la unión de una molécula natural o sintética, en particular de una molécula biológicamente activa, y en donde por lo menos una cámara de reacción (5) está asociada reversiblemente a una cámara de aumento de volumen (37), en donde la cámara de aumento de volumen (37) está aplicada sobre el soporte de biochips (1), de manera que se forma una unión estanca a los líquidos entre las paredes laterales (9) de la cámara de reacción (5) y las paredes laterales (39) de la cámara de aumento de volumen (37) .
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/000311.
Solicitante: GREINER BIO-ONE GMBH.
Nacionalidad solicitante: Alemania.
Dirección: MAYBACHSTRASSE 2 72636 FRICKENHAUSEN ALEMANIA.
Inventor/es: JEHLE,Heinrich, KNEBEL,Günther, STAPPERT,Jörg, KESSLER,Joachim.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01J19/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › Procedimientos químicos, físicos o físico-químicos en general; Aparatos apropiados.
- B01L3/00 B01 […] › B01L APARATOS DE LABORATORIO PARA LA QUIMICA O LA FISICA, DE USO GENERAL (aparatos de uso médico o farmacéutico A61; aparatos para aplicaciones industriales o aparatos de laboratorio cuya estructura y funciones son comparables a las de aparatos industriales similares, ver las clases relativas a los aparatos industriales, en particular las subclases B01 y C12; aparatos de separación o de destilación B01D; dispositivos de mezcla o de agitación B01F; atomizadores B05B; tamices, cribas B07B; tapones, capuchones B65D; manipulación de líquidos en general B67; bombas de vacío F04; sifones F04F 10/00; grifos, válvulas F16K; tubos, empalmes para tubos F16L; aparatos especialmente adaptados al estudio y análisis de materiales G01, particularmente G01N; aparatos eléctricos u ópticos, ver las subclases apropiadas en las secciones G y H). › Recipientes o utensilios para laboratorios, p. ej. cristalería de laboratorio (botellas B65D; equipos para enzimología o microbiología C12M 1/00 ); Cuentagotas (recipientes para volumetría G01F).
- C40B40/06 QUIMICA; METALURGIA. › C40 TECNOLOGIA COMBINATORIA. › C40B QUIMICA COMBINATORIA; BIBLIOTECAS, p. ej. QUIMIOTECAS (bibliotecas combinatorias in silico de ácidos nucleicos, proteínas o péptidos G16B 35/00; química combinatoria in silico G16C 20/60). › C40B 40/00 Bibliotecas per se , p. ej. arrays, mezclas. › Bibliotecas que contienen nucleótidos o polinucleótidos, o sus derivados.
- C40B40/10 C40B 40/00 […] › Bibliotecas que contienen péptidos o polipéptidos, o sus derivados.
- C40B60/14 C40B […] › C40B 60/00 Aparatos especialmente adaptados para su empleo en química combinatoria o con bibliotecas. › para la creación de bibliotecas.
PDF original: ES-2377564_T3.pdf
Fragmento de la descripción:
Recipiente de muestras para análisis.
La invención se refiere a un recipiente de muestras para análisis, en particular a un soporte de biochips, el cual comprende una placa de soporte con por lo menos una cámara de reacción, la cual es apropiada para diagnósticos médicos o para la búsqueda de substancias activas.
Son ya conocidas las microplacas para la titulación de materiales biológicos o químicos, o respectivamente, para la realización de mediciones de fluorescencia, de luminiscencia u otras mediciones. Las microplacas, que están formadas por múltiples cubetas, encuentran aplicación particularmente en la investigación, la clínica y la industria, en particular en la determinación de la serología de grupos sanguíneos, series de ensayo de antibióticos, titulaciones complementarias y otros trabajos de laboratorio, en los cuales por ejemplo se requieren series de dilución geométrica. El formato estándar general con las investigaciones bioquímicas y biológicos celulares son placas de microtitulación de 96 pocillos ("potecitos de muestras" o cavidades) con un volumen de reacción de hasta 500 μl por pocillo. Cada vez más se emplean placas de microtitulación con 384 pocillos o incluso con 1536 pocillos. Esta tendencia de una creciente miniaturización está forzada ante todo por la química combinatoria y el screening de alto rendimiento, también llamado HTS ("High Throughput Screening") ("Screening de alto rendimiento") . Ambos campos pertenecen hoy a los pilares fundamentales de la moderna investigación farmacéutica de substancias activas.
Mediante el HTS se investiga por ejemplo si existe en una biblioteca de substancias una substancia activa que puede ser empleada como base para nuevos medicamentos. Los componentes de la biblioteca de substancias deben investigarse a este respecto en un procedimiento de ensayo con respecto a su reactividad con un objetivo (molécula diana) . Las substancias encontradas son posibles candidatos para una substancia activa, la cual puede influir sobre la función de la molécula diana en cuestión. La detección de la substancia activa tiene lugar a este respecto o bien mediante procedimientos ópticos como la absorción, la fluorescencia y la luminiscencia, o bien mediante la detección de la radioactividad por centelleo. La multiplicidad de las interacciones a investigar requiere una gran variación en los sistemas de ensayo y en los tipos de detección vinculados.
La búsqueda de substancias activas exige que en primer lugar se encuentren las dianas que son responsables de la aparición de enfermedades. Gracias a la creciente comprensión de la moderna biología molecular se identifican cada vez más genes causantes de enfermedades o respectivamente influyentes en enfermedades, sobre los cuales puede actuarse con medicamentos apropiados. Un hito en el análisis de moléculas biológicamente activas, en particular, para la identificación de los genes responsables de la aparición de las enfermedades, lo constituyen los soportes miniaturizados, los llamados biochips. En la superficie de estos soportes pueden ser inmovilizadas o sintetizadas moléculas biológicamente activas de composición conocida, en toda la superficie o en una retícula asignada. En el caso de las moléculas biológicamente inmovilizadas puede tratarse por ejemplo de ácidos nucleicos o fragmentos de los mismos o respectivamente de proteínas o fragmentos de las mismas. Mediante la ayuda de los biochips que contienen los ácidos nucleicos inmovilizados, los cuales se llaman también DNA-Arrays ("matrices de ADN") , la determinación por ejemplo de ácidos nucleicos en las muestras que hay que investigar, se facilita, se acelera, se paraleliza, se automatiza y se precisa esencialmente. Los chips de ADN o las matrices de ADN se emplean por ejemplo en el diagnóstico clínico de enfermedades infecciosas, de enfermedades cancerígenas y de enfermedades hereditarias. La eficiencia de dichos chips de ADN en los análisis de muestras reside en particular en que son necesarios únicamente pequeños volúmenes de muestra y en que la evaluación puede lograrse mediante procedimientos de medición altamente sensibles. Mediante el empleo de dichos chips se pueden investigar por lo tanto gran cantidad de muestras con mucha rapidez. También son conocidas las matrices de proteína, en las cuales análogamente a los chips de ADN, se disponen las proteínas o los péptidos sobre por ejemplo membranas de plástico en una ordenada y conocida retícula. Esta clase de matrices de proteína se emplean ante todo para la investigación del enlace mutuo de proteínas, por ejemplo, la interacción receptor-ligando, para la identificación de complejos de proteínas intracelulares, para la investigación de interacciones proteína-ADN e interacciones proteínas-ARN, ó para el análisis de interacciones proteína-anticuerpo. Con la ayuda de la tecnología proteína-chip ya pueden ser identificados numerosos marcadores de proteína para las enfermedades cancerígenas o enfermedades como la demencia de Alzheimer.
La miniaturización del sistema de ensayo con microplacas aporta en verdad considerables ventajas con respecto a los costes, pero sin embargo está unida a grandes problemas en su realización técnica. Debido a la miniaturización de las placas de microtitulación deben también miniaturizarse cada vez más los ensayos a efectuar en los pocillos. Por este motivo son necesarios también dispositivos de detección con volúmenes cada vez más pequeños y exigencias cada vez más grandes. Así, es conocido que en los tipos de detección individuales en volúmenes extremamente pequeños se presentan especiales problemas. En la medición de la luminiscencia, un volumen pequeño de muestra significa por ejemplo también una señal pequeña para la detección óptica lo cual tiene influencia sobre la sensibilidad de la medición. La medición de la absorción se ve entorpecida por el efecto menisco de la superficie del líquido, puesto que el menisco tiene lugar de manera muy variable en espacios extremadamente pequeños de muestras. Única y solamente la medición de la fluorescencia no está sujeta a restricciones de volumen. De todas formas la sensibilidad que puede lograrse está aquí limitada, por la propia fluorescencia del material plástico que se utiliza en las placas de microtitulación en la mayoría de los procedimientos.
Surgen problemas en particular con las microplacas con varios cientos de pocillos. Puesto que la abertura de dichos pocillos es muy pequeña y además frecuentemente está limitada todavía por un abultamiento anular, mientras que el volumen es al mismo tiempo relativamente grande, se pueden emplear en los pocillos sistemas de detección empleados para detectar las reacciones, por ejemplo, dispositivos de scanning, que se emplean colocados no verticalmente en un ángulo óptimo de 90º encima o respectivamente en la abertura de los pocillos, sino que deben colocarse oblicuamente encima o respectivamente dentro de las aberturas, de manera que el ángulo sea parcialmente considerablemente menor de 90º C. Con ello se produce un efecto de sombra, el cual falsea adicionalmente los resultados conseguidos en el análisis mediante el sistema de detección. También los dispositivos Spotter ("marcadores") que sirven para recubrir el fondo de los pocillos por ejemplo con ácidos nucleicos, originan problemas técnicos, puesto que los Spotter deben introducirse en los pocillos a una relativa profundidad.
En la industria farmacéutica basada en la investigación o respectivamente en la investigación básica pueden tolerarse a menudo los problemas que aparecen en la placa de microtitulación en relación con la miniaturización. En primer lugar, se pretende someter muchas muestras al mismo procedimiento de ensayo sobre una placa, en filas paralelas. A menudo, es más que suficiente, determinar la diferencia de intensidad de una señal entre pocillos individuales y con ello obtener una declaración más cualitativa. En el diagnóstico clínico la situación sin embargo es totalmente distinta. Aquí por ejemplo deben someterse muy a menudo muestras, por ejemplo líquidos corporales de un paciente a varios diferentes procedimientos de ensayo con el empleo de diferentes reactantes, en donde cada ensayo puede comprender comparativamente pocas mezclas paralelas. Por el contrario, es a menudo también necesario ensayar muchas muestras de diferentes pacientes respecto a un único parámetro. Por el contrario, en el screening de alto rendimiento los ensayos clínicos individuales deben hacer posible de todas formas, declaraciones cuantitativas para por ejemplo poder detectar el brote o el curso de una enfermedad en un paciente individual. Los problemas... [Seguir leyendo]
Reivindicaciones:
1. Soporte de biochips que comprende una placa de soporte (3) con por lo menos una cámara de reacción tridimensional (5) , en donde la cámara de reacción (5) está formada por un fondo (7) y el volumen abierto por arriba de la cámara de reacción (5) está abarcado lateralmente por las paredes laterales (9) , en donde la relación entre la superficie (F) del fondo (7) y la altura (H) de las paredes laterales (9) es mayor o igual a 30, de preferencia mayor de 50, y en donde el fondo (7) y/o por lo menos una pared lateral (9) de por lo menos una cámara de reacción (5) está ejecutada como matriz de unión con un grupo funcional que permite la unión de una molécula natural o sintética, en particular de una molécula biológicamente activa, y en donde por lo menos una cámara de reacción (5) está asociada reversiblemente a una cámara de aumento de volumen (37) , en donde la cámara de aumento de volumen (37) está aplicada sobre el soporte de biochips (1) , de manera que se forma una unión estanca a los líquidos entre las paredes laterales (9) de la cámara de reacción (5) y las paredes laterales (39) de la cámara de aumento de volumen (37) .
2. Soporte de biochips según la reivindicación 1, en donde el borde superior (11) de por lo menos una cámara de reacción (5) representa la parte más alta del soporte de biochips (1) .
3. Soporte de biochips según la reivindicación 1 ó 2, en donde el borde superior (11) de por lo menos una cámara de reacción (5) , está en un plano por encima del borde superior (13) de la placa de soporte (3) .
4. Soporte de biochips según la reivindicación 3, en donde la placa de soporte (3) forma el fondo (7) de por lo menos una cámara de reacción (5) y las paredes laterales (9) de la cámara de reacción (5) están formadas como elevaciones sobre la placa de soporte (3) .
5. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 4, en donde por lo menos una cámara de reacción (5) está colocada sobre una base (29) .
6. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 5, en donde la base (29) en una vista en planta tiene la misma forma de la vista en planta de la cámara de reacción (5) .
7. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 6, en donde la superficie superior (31) de la base (29) representa el fondo (7) de la cámara de reacción (5) .
8. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 7, en donde las paredes laterales (33) de la base (29) están en un mismo plano con las paredes laterales (9) de la cámara de reacción (5) .
9. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 8, en donde las paredes laterales (9) de la cámara de reacción (5) están formadas como unas elevaciones sobre la base (29) .
10. Soporte de biochips según la reivindicación 1 ó 2, en donde el borde superior (11) de por lo menos una cámara de reacción (5) y el borde superior (13) de la placa de soporte (3) están en el mismo plano.
11. Soporte de biochips según la reivindicación 10, en donde por lo menos una cámara de reacción (5) está colocada dentro de, y/o debajo de, la placa de soporte (3) como un pocillo.
12. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 11, en donde la parte del fondo (7) de por lo menos una cámara de reacción (5) en la vista en planta, tiene la forma de un círculo, un rectángulo, un cuadrado, un hexágono, un polígono, o de una elipse.
13. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 12, en donde la placa de soporte (3) tiene unas dimensiones que permiten la inserción del soporte de biochips (1) en una placa de microtitulación que tiene unas dimensiones según la norma SBS (Society of Biomolecular Screening) ("Sociedad de screening biomolecular") .
14. Soporte de biochips según la reivindicación 13, en donde el soporte de biochips (1) tiene 1, 2, 4, 8, 12 ó en cada caso múltiplos enteros de 8 ó 12 cámaras de reacción (5) .
15. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 13, en donde la placa de soporte (3) está ejecutada como una tira.
16. Soporte de biochips según la reivindicación 15, en donde la placa de soporte (3) tiene las dimensiones de un portaobjetos estándar.
17. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde la placa de soporte (3) está ejecutada como una tira con 4 ó en cada caso múltiples enteros de 4 cámaras de reacción (5) separadas, dispuestas unas detrás de otras.
18. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde por lo menos una de las cámaras de reacción (5) tiene el fondo (7) en forma de círculo con un diámetro de 6 mm y una altura de pared lateral (H) de 0, 5 mm.
19. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde por lo menos una cámara de reacción (5) tiene el fondo de forma cuadrada con una longitud lateral de 6 mm y una altura de la pared (H) de 0, 5 mm.
20. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 19, en donde la placa de soporte (3) y por lo menos una cámara de reacción (5) son de un material plástico.
21. Soporte de biochips según la reivindicación 20, en donde en el caso de un material de plástico se trata del copolímero de estireno-anhídrido maleico (SMA) , copolímero de cicloolefinas (COC) , polímero de cicloolefinas (COP) , acrilobutadienoestireno, poliamida, policarbonato, poliéster, polimetilmetacrilato, polipropileno, poliestireno o estirenoacrilonitrilo.
22. Soporte de biochips según una cualquiera de las reivindicaciones 1 a 21, en donde el fondo (7) de por lo menos una cámara de reacción (5) , se compone de un polímero, de vidrio, de una membrana o de un híbrido de los mismos, el cual tiene en la superficie por lo menos un grupo funcional que puede fijarse a una molécula biológicamente activa.
23. Soporte de biochips según la reivindicación 22, en donde el grupo funcional se aplica sobre la superficie del polímero mediante el empleo de un procedimiento de funcionalización química.
24. Soporte de biochips según la reivindicación 23, en donde el polímero del fondo es un polímero con radicales aromáticos, en cuya superficie están anclados grupos de clorometilo.
25. Soporte de biochips según la reivindicación 24, en donde el polímero es poliestireno.
26. Soporte de biochips según la reivindicación 24 ó 25, en donde el grupo clorometilo del polímero está substituido con N-u O-nucleófilos.
27. Soporte de biochips según la reivindicación 26, en donde el grupo clorometilo está substituido con un grupo aldehído.
28. Soporte de biochips según la reivindicación 26, en donde el grupo clorometilo está substituido con un ácido carboxílico.
29. Soporte de biochips según la reivindicación 23, en donde el polímero del fondo es un polímero saturado, cuya superficie está clorada.
30. Soporte de biochips según la reivindicación 29, en donde el polímero clorado es un copolímero clorado de cicloolefinas, en particular el producto TOPAS clorado.
31. Soporte de biochips según la reivindicación 22, en donde el grupo funcional se aplica mediante el empleo de un procedimiento de funcionalización con plasma sobre la superficie del polímero.
32. Soporte de biochips según la reivindicación 31, en donde la superficie presenta funciones de ácido carboxílico, de aldehído/cetona, de amina, de epoxí y/o de halógeno.
33. Soporte de biochips según la reivindicación 22, en donde el grupo funcional se aplica mediante el empleo de una funcionalización de la superficie fotoinducida sobre la superficie del polímero.
34. Soporte de biochips según la reivindicación 33, en donde el grupo funcional se aplica sobre la superficie del polímero mediante la reacción de la antraquinona con un dador y a continuación se efectúa la fijación fotoquímica.
35. Soporte de biochips según la reivindicación 33, en donde el grupo funcional se aplica mediante injerto fotoquímico sobre la superficie del polímero.
36. Soporte de biochips según la reivindicación 22, en donde el grupo funcional se aplica mediante el empleo de la polimerización por injerto sobre la superficie del polímero.
37. Soporte de biochips según una cualquiera de las reivindicaciones 22 a 36, en donde en el fondo (7) de la cámara de reacción (5) está unida una molécula biológicamente activa.
38. Soporte de biochips según la reivindicación 37, en donde la molécula biológicamente activa es una proteína, un ácido nucleico o una molécula de PNA.
39. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde a cada una de las cámaras de reacción (5) del soporte de biochips (1) está asignada una cámara de aumento de volumen (37) .
40. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde la cámara de aumento de volumen (37) está formada por unas paredes laterales (29) .
41. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde la cámara de aumento de volumen (37) formada por las paredes laterales (29) , es un componente de un dispositivo de aumento de volumen (35) .
42. Soporte de biochips según la reivindicación 41, en donde el dispositivo de aumento de volumen (35) comprende un marco (41) y por lo menos una cámara de aumento de volumen (37) formada por las paredes laterales (29) .
43. Soporte de biochips según una cualquiera de las reivindicaciones 41 ó 42, en donde el dispositivo de aumento de volumen (35) está realizado en forma de una tira o de una matriz.
44. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde la altura (Hv) de las paredes laterales (39) de la cámara de aumento de volumen (37) es mayor que la altura (H) de las paredes laterales (9) de la cámara de reacción (5) .
45. Soporte de biochips según una cualquiera de las reivindicaciones 41 a 43, en donde el dispositivo de aumento de volumen (35) puede aplicarse sobre el soporte de biochips (1) , de manera que se forma una unión hermética a los líquidos entre las paredes laterales (9) de la cámara de reacción (5) y las paredes laterales (39) de la cámara de aumento de volumen (37) .
46. Soporte de biochips según una cualquiera de las reivindicaciones 41 a 43 ó 45, en donde entre el soporte de biochips (1) y el dispositivo de aumento de volumen asignable reversiblemente (35) se aplica una almohadilla impermeable (43) .
47. Soporte de biochips según una cualquiera de las precedentes reivindicaciones, en donde cada cámara de aumento de volumen (37) puede cerrarse, en particular mediante una de las cubiertas (45) asignadas a la cámara de aumento de volumen (37) .
48. Kit que comprende un soporte de biochips (1) según una cualquiera de las reivindicaciones 1 a 38, y una placa de microtitulación (100) .
49. Kit según la reivindicación 48, que comprende además, una almohadilla de estanqueidad (43) .
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
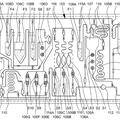 Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
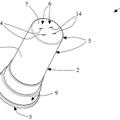 Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
DISPOSITIVO PARA LA SELECCIÓN DE ESPERMATOZOIDES, del 23 de Julio de 2020, de INSTITUTO NACIONAL DE INVESTIGACION Y TECNOLOGIA AGRARIA Y ALIMENTARIA (INIA): Dispositivo para la selección de espermatozoides que comprende una unidad de selección que comprende a su vez un compartimento de carga (1b) […]
Uso de un sistema de banco de células de crioconservación cerrado de alta capacidad y procedimiento para descongelar y dispensar células almacenadas, del 22 de Julio de 2020, de Boehringer Ingelheim Animal Health USA Inc: Uso de un sistema de banco de células de crioconservación de fase cerrada y alta capacidad para almacenar grandes volúmenes de células, en el que el uso comprende las siguientes […]
Dispositivo microfluídico para generar una secuencia de sustancias en un canal microfluídico, del 22 de Julio de 2020, de EUROPEAN MOLECULAR BIOLOGY LABORATORY: Un aparato microfluídico para proporcionar una o más sustancias líquidas a una red de canales microfluídicos , comprendiendo el aparato microfluídico una red de canales […]
Sistema microfluídico, del 22 de Julio de 2020, de Menarini Silicon Biosystems S.p.A: Un sistema microfluídico para el aislamiento de partículas de al menos un tipo dado de una muestra; comprendiendo el sistema microfluídico una entrada , a […]
Un dispositivo y método para calentar o enfriar una muestra, del 22 de Julio de 2020, de Cell Therapy Catapult Limited: Un dispositivo para calentar o enfriar una o más muestras, comprendiendo el dispositivo una pluralidad de miembros que pueden funcionar en uso para calentar […]