Métodos para medir la inhibición de la agregación de plaquetas mediante antagonistas del receptor de trombina.
Un método para medir la inhibición de la agregación de plaquetas por un antagonista del receptor de trombina,
que comprende las etapas de:
a) proporcionar una muestra de sangre que contiene plaquetas de un individuo tratado con un antagonista delreceptor de trombina;
b) poner en contacto dicha muestra de sangre que contiene plaquetas con un activador del receptor detrombina en condiciones adecuadas para activar la agregación de plaquetas en dicha muestra de sangre quecontiene plaquetas; y
c) evaluar la agregación de plaquetas en dicha muestra de sangre que contiene plaquetas para determinar lapresencia, ausencia y/o grado de inhibición de la agregación de plaquetas por dicho antagonista del receptorde trombina en dicho individuo, en donde la ausencia o una reducción de dicha agregación de plaquetas indicaque dicho individuo tiene capacidad reducida para formar agregación de plaquetas en respuesta a dichotratamiento con antagonista del receptor de trombina en el que,
el antagonista del receptor de trombina comprende una sustancia seleccionada del grupo que consiste en unanticuerpo para el dominio de unión a trombina de un receptor de trombina, un derivado peptídico de TRAP-1, underivado peptídico de TRAP-4, un péptido mimético de un derivado de TRAP-1, un peptidomimético de un derivadode TRAP-4, E5555 y SCH 530348.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/062415.
Solicitante: ACCUMETRICS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3985 SORRENTO VALLEY BLVD. SAN DIEGO, CA 92121 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DURBIN,DENNIS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/86 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que interviene el tiempo de coagulación de la sangre.
PDF original: ES-2387700_T3.pdf
Fragmento de la descripción:
Métodos para medir la inhibición de la agregación de plaquetas mediante antagonistas del receptor de trombina
CAMPO DE LA INVENCIÓN
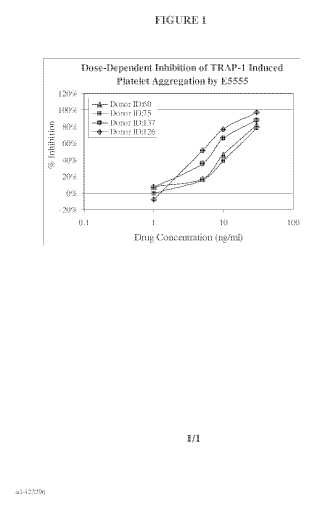
La presente invención está relacionada con el campo de los ensayos de diagnóstico, y en particular con la determinación de la actividad de la función de plaquetas en muestras sanguíneas para estudiar los efectos de composiciones antiplaquetarias, y más particularmente el uso de un activador de plaquetas, tal como péptido activador del receptor de trombina (TRAP) , para la medición de la función en plaquetas de los inhibidores del receptor de trombina, incluyendo E5555 (Eisai) y SCH 530348 (Schering-Plough) , con sensibilidad aumentada.
ANTECEDENTES DE LA INVENCIÓN
El papel de las plaquetas en la fisiología de mamíferos es extraordinariamente diverso, pero su papel primario es en la promoción de la hemostasis. En muchas situaciones, se desea una evaluación de la capacidad de la sangre para coagular, un parámetro que frecuentemente se controla por la capacidad de las plaquetas para adherirse y/o agregarse. Resulta de interés, por lo tanto, la evaluación de las funciones adhesivas de las plaquetas. Por ejemplo, las cuestiones de interés incluyen si administrar fármacos que bloqueen, o promuevan, la formación de coágulos, o si detectar deficiencias en la función de las plaquetas antes de procedimientos quirúrgicos. También resulta de interés evaluar la eficacia de un inhibidor de plaquetas que se ensaya como un nuevo fármaco o que se usa como tratamiento clínico aprobado en un paciente.
Se sabe que las plaquetas se agregan en una diversidad de condiciones y en presencia de varios reactivos diferentes. La agregación de plaquetas es un término usado para describir la unión de plaquetas entre sí. La agregación de plaquetas in vitro depende de la capacidad de las plaquetas para unir fibrinógeno a sus superficies después de activación por un agente inductor de agregación tal como trombina, adenosín difosfato (ADP) o colágeno.
Las plaquetas desempeñan un papel crítico en el mantenimiento de la hemostasis normal. Cuando se exponen a un vaso sanguíneo dañado, las plaquetas se adherirán a matriz sub-endotelial expuesta. Después de la adhesión inicial, diversos factores liberados o producidos en el sitio de la lesión tales como trombina, ADP y colágeno activan las plaquetas. Una vez que las plaquetas se activan, se produce un cambio conformacional en el receptor glucoproteína GPIIb/IIIa de plaquetas, permitiéndole unirse a fibrinógeno y/o factor de von Willebrand. Es esta unión del fibrinógeno multivalente y/o moléculas de factor de von Willebrand por receptores GPIIb/IIIa en plaquetas adyacentes lo que da como resultado el reclutamiento de plaquetas adicionales en el sitio de lesión y su agregación para formar un tapón hemostático o trombo.
La agregometría de plaquetas in vitro es el método de laboratorio usado para evaluar la capacidad in vivo de las plaquetas para formar los agregados que conducen a un tapón hemostático primario. En esta técnica, se añade un agente agregante tal como ADP o colágeno a sangre completa o plasma rico en plaquetas y se controla la agregación de las plaquetas. La agregometría de plaquetas es una herramienta de diagnóstico que puede ayudar en el diagnóstico de pacientes y selección de terapia. Los ensayos actuales para medir la agregación de plaquetas son caros, requieren mucho tiempo, son incómodos y generalmente no son adecuados para un ambiente clínico.
Se ha desarrollado un ensayo de la función de las plaquetas rápido y se describe en la Patente de Estados Unidos Nº 5.763.199 (Coller) . El ensayo determina bloqueo del receptor glucoproteína GPIIb/IIIa en sangre completa. La aglutinación de perlas poliméricas pequeñas recubiertas con un ligando de GPIIb/IIIa tal como fibrinógeno resulta cuando las perlas se ponen en contacto con sangre completa que contiene plaquetas con receptores GPIIb/IIIa activados que no están bloqueados. La no aglutinación indica que los receptores GPIIb/IIIa no se activan y/o bloqueo de los receptores GPIIb/IIIa. En una realización preferida, la adición de un activador de receptor de trombina da como resultado un ensayo que es suficientemente rápido y conveniente para realizarse a la cabecera y que da como resultado aglutinación de las perlas poliméricas pequeñas en un periodo de tiempo conocido conveniente si los receptores GPIIb/IIIa no están bloqueados. El ensayo incluye la capacidad para transferir sangre para ensayar de un recipiente de recogida a un dispositivo de ensayo sin abrir el recipiente de recogida. Este ensayo de agregación de plaquetas puede realizarse a la vez que el tiempo de coagulación activado (ACT) , que se realiza para evaluar la adecuación de la heparinización.
La agregación de plaquetas desempeña un papel clave en la patogénesis de trombosis y enfermedad de arteria coronaria aguda. Un enfoque para tratar trombosis implica inhibir la actividad enzimática de trombina, y los compuestos usados para este fin han incluido heparina, heparina de bajo peso molecular, hirudina, argatrobán, hirulog, etc. Todos los compuestos tales inhiben la actividad enzimática de trombina, y actúan inhibiendo la formación de coágulos sanguíneos de fibrina sin inhibir específicamente el efecto de la trombina en las células. La tendencia a la hemorragia es por lo tanto un efecto secundario habitual encontrado en la clínica. [0008] El papel de la trombina en trombosis no se limita a su actividad de coagulación sanguínea. Además de su papel central en la hemostasis y curación de heridas, la trombina activa las plaquetas humanas uniéndose a dos receptores activados por proteasa acoplados a proteínas G de superficie celular, PAR-1 y PAR-4, que también se conocen como los receptores de trombina. (Véase Kahn, et al., Nature 1998, 394:690-694; Kahn, et al., J. Clin. Invest. 1999, 103:879-887) . La afinidad por la trombina es más alta para PAR-1 que PAR-4, y por lo tanto se cree que la activación de plaquetas por dosis bajas de trombina está predominantemente mediada por PAR-1. Se ha sugerido que PAR-4 mantiene la activación de plaquetas prolongada por altas dosis de trombina. (Véase Covic, et al., Biochemistr y 2000, 39:5458-5467; Covic, et al., Thromb. Haemost. 2002, 87:722-727) . La activación de los receptores PAR-1 y PAR-4 desencadena liberación de calcio intracelular, que activa PKC, modulando de este modo glucoproteína IIb/IIIa y permitiendo que los sitios de unión a ligando de integrina contribuyan a la agregación de plaquetas. La liberación de calcio intracelular inducida por trombina también activa fosfolipasa A2, liberando ácido araquidónico, la primera etapa en la biosíntesis de prostaglandina y tromboxano.
Se han clonado tanto PAR-1 como PAR-4. (Véase Vu, et al., Cell 1991, 64:1057-1068; Xu, et al., Proc. Natl. Acad. Sci. USA 1998, 95:6642-6646; Mar y anoff, et al., Curr. Med. Chem. Cardiovasc. Hematol. Agents 2003, 1 (1) :13-36) , abriendo una puerta importante para el desarrollo de sustancias que se dirigen a receptores de trombina celular. El examen detallado de la secuencia de aminoácidos de estos receptores de trombina ha revelado que tanto PAR-1 como PAR-4 se escinden por trombina en sitios específicos en el dominio extracelular para desenmascarar una nueva secuencia N-terminal que se une al cuerpo del receptor e inicia la señalización transmembrana. (Véase Vu, et al., Nature 1991, 353:674-677; Coughlin, S.R., Proc. Natl. Acad. Sci. U.S.A. 1999, 96:11023-11027) . Los péptidos específicos que reproducen la secuencia del nuevo extremo N-terminal de los receptores de trombina activados (habitualmente denominados “péptidos de activación del receptor de trombina” o “TRAP”) son activadores potentes y selectivos de PAR-1 y PAR-4 no hidrolizados y se ha mostrado que desencadenan todas las respuestas de plaquetas inducidas por trombina. (Véase, Kahn, et al., J. Clin. Invest. 1999, 103:879-887; Hung, et al., J. Biol. Chem 1992, 267:20831-20834) .
El péptido activador del receptor de trombina PAR-1 (TRAP-1) , que activa específicamente PAR-1, es un heptapéptido que tiene la siguiente secuencia de aminoácidos: SFLLRNP (NH2-Ser-Phe-Leu-Leu-Arg-Asn-Pro-COOH) . Por el contrario, el péptido activador del receptor de trombina PAR-4 (TRAP-4) , que activa específicamente PAR-4, es un hexapéptido: GYPGQV (NH2-Gly-Tyr-Pro-Gly-Gln-Val-COOH) . Notablemente, se ha indicado que una variante más potente de TRAP-4, denominada como alternativa en la bibliografía TRAP-4 o TRAP-4A, tiene la secuencia de aminoácidos AYPGKF... [Seguir leyendo]
Reivindicaciones:
1. Un método para medir la inhibición de la agregación de plaquetas por un antagonista del receptor de trombina, que comprende las etapas de:
a) proporcionar una muestra de sangre que contiene plaquetas de un individuo tratado con un antagonista del receptor de trombina; b) poner en contacto dicha muestra de sangre que contiene plaquetas con un activador del receptor de trombina en condiciones adecuadas para activar la agregación de plaquetas en dicha muestra de sangre que contiene plaquetas; y c) evaluar la agregación de plaquetas en dicha muestra de sangre que contiene plaquetas para determinar la presencia, ausencia y/o grado de inhibición de la agregación de plaquetas por dicho antagonista del receptor de trombina en dicho individuo, en donde la ausencia o una reducción de dicha agregación de plaquetas indica que dicho individuo tiene capacidad reducida para formar agregación de plaquetas en respuesta a dicho tratamiento con antagonista del receptor de trombina en el que,
el antagonista del receptor de trombina comprende una sustancia seleccionada del grupo que consiste en un anticuerpo para el dominio de unión a trombina de un receptor de trombina, un derivado peptídico de TRAP-1, un derivado peptídico de TRAP-4, un péptido mimético de un derivado de TRAP-1, un peptidomimético de un derivado de TRAP-4, E5555 y SCH 530348.
2. El método de la reivindicación 1, en el que el receptor de trombina es PAR-1 o PAR-4.
3. El método de la reivindicación 1, en el que el activador del receptor de trombina comprende una sustancia seleccionada del grupo que consiste en una trombina, un péptido activador del receptor de trombina PAR-1 (TRAP1) y un péptido activador del receptor de trombina PAR-4 (TRAP-4) .
4. El método de la reivindicación 3, en el que la trombina tiene una concentración final de 0, 01 U/ml a 0, 5 U/ml.
5. El método de la reivindicación 3, en el que el TRAP-1 tiene una concentración final de 0, 5 !M a 10 !M.
6. El método de la reivindicación 3, en el que el TRAP-4 tiene una concentración final de 50 !M a 1 mM.
7. El método de la reivindicación 1, en el que el activador del receptor de trombina comprende TRAP-1.
8. El método de la reivindicación 1, en el que la muestra de sangre que contiene plaquetas es una muestra de sangre completa.
9. El método de la reivindicación 1, en el que la muestra de sangre que contiene plaquetas es una muestra de plasma.
10. El método de la reivindicación 9, en el que la muestra de plasma es una muestra de plasma rica en plaquetas (PRP) .
11. El método de la reivindicación 1, en el que el antagonista del receptor de trombina comprende E5555.
12. El método de la reivindicación 1, en el que el antagonista del receptor de trombina comprende SCH 530348.
13. El método de la reivindicación 1, en el que el activador del receptor de trombina está contenido en un medio de ensayo que tiene una absorción máxima a aproximadamente 800 nm.
14. El método de la reivindicación 1, que se realiza a una temperatura que varía de 30 ºC a 40 ºC, y el tiempo total de las lecturas desde el tiempo de contacto entre la muestra de sangre que contiene plaquetas y el activador del receptor de trombina oscila en el rango de 10 segundos a 10 minutos.
15. El método de la reivindicación 1, en el que dicha muestra de sangre que contiene plaquetas se pone en contacto con dicho activador del receptor de trombina en un dispositivo de ensayo de uso único.
16. El método de la reivindicación 1, que comprende adicionalmente poner en contacto dicha muestra de sangre que contiene plaquetas con partículas que comprenden un ligando de receptor GPIIb/IIIa inmovilizado en las mismas.
17. El método de la reivindicación 16, en el que el ligando del receptor GPIIb/IIIa comprende una sustancia seleccionada del grupo que consiste en fibrinógeno, anticuerpo monoclonal 10E5, anticuerpo monoclonal c7E3, factor de von Willebrand, fibronectina, vitronectina, un ligando que tiene una secuencia de arginina glicina-ácido aspártico (RGD) y un péptido o un peptidomimético que imita la secuencia de RGD.
18. El método de la reivindicación 16, en el que el ligando del receptor GPIIb/IIIa comprende fibrinógeno.
19. El método de la reivindicación 16, en el que las partículas y el activador del receptor de trombina están contenidos en un medio de ensayo que tiene una absorción máxima a aproximadamente 800 nm.
Patentes similares o relacionadas:
Procedimiento de prueba de plaquetas en sangre, del 15 de Julio de 2020, de FUJIMORI KOGYO CO., LTD: Procedimiento para someter a prueba la agregación plaquetaria, que comprende someter sangre anticoagulada a un tratamiento débil de activación […]
Composición para la determinación de las características de coagulación de un líquido de ensayo, del 6 de Mayo de 2020, de C A CASYSO AG: Una composición de diagnóstico para su uso en el análisis viscoelástico de un líquido de ensayo seleccionado de entre sangre entera o plasma sanguíneo, que comprende: […]
Concentración de células raras, del 23 de Octubre de 2019, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Método para aumentar una razón de células raras con respecto a células no raras en una muestra de sangre que se sospecha que contiene células raras y células no raras, comprendiendo […]
Procedimiento de detección de coagulación intravascular diseminada o coagulación intravascular diseminada infecciosa, del 2 de Octubre de 2019, de LSI Medience Corporation: Un procedimiento in vitro de detección de coagulación intravascular diseminada, que comprende medir sCD14-ST en una muestra.
Interfaz y procedimientos de un interpretador de resultados de un sistema de examen de sangre, del 18 de Septiembre de 2019, de C A Casyso GmbH: Un procedimiento para proporcionar un producto de interpretación de resultados, que comprende: recibir, en una máquina analizadora de sangre […]
 Ensayo para determinar anticoagulantes en sangre o plasma sanguíneo, del 31 de Julio de 2019, de Ravmarker AB: Un ensayo para determinar los anticoagulantes en una muestra de sangre o de plasma sanguíneo, en el que los anticoagulantes determinados en dicho ensayo son inhibidores […]
Ensayo para determinar anticoagulantes en sangre o plasma sanguíneo, del 31 de Julio de 2019, de Ravmarker AB: Un ensayo para determinar los anticoagulantes en una muestra de sangre o de plasma sanguíneo, en el que los anticoagulantes determinados en dicho ensayo son inhibidores […]
Dispositivo que incluye componentes sanguíneos para separar moléculas o partículas diana de muestras, del 24 de Julio de 2019, de Debiopharm International S.A: Dispositivo de recogida de muestras para separar agentes infecciosos, toxinas, ácidos nucleicos y/o proteínas de una muestra que comprende: (i) un código […]
Reactivo de tiempo de protrombina que contiene un quelante de hierro, del 6 de Junio de 2019, de SIEMENS HEALTHCARE DIAGNOSTICS PRODUCTS GMBH: Reactivo de tiempo de protrombina que contiene proteína de factor tisular y fosfolípidos, caracterizado porque el reactivo contiene además al menos un quelante de hierro, […]