Deleción de un grupo de genes y humanización en dos etapas.
Un procedimiento para humanizar un ratón para un gen de interés,
que comprende:
a) incorporar un par de sitios de recombinación específica de sitio en el genoma murino mediante recombinación homóloga, de manera que la secuencia diana de genes murinos que se vaya a reemplazar esté flanqueada a cada lado por un sitio de recombinación; en el que al menos uno de los dos sitios de recombinación se crean para que sean contiguos a una secuencia de genes humanos de reemplazo; y siendo dicha secuencia de genes humanos de reemplazo colocada para que dicho sitio de recombinación se encuentre entre dicha secuencia de genes humanos de reemplazo y dicha secuencia diana de genes murinos;
b) realizar la recombinación entre los sitios de recombinación específica de sitio, de modo que la secuencia humana se introduzca en la posición del genoma murino previamente ocupada por el gen diana murino, flanqueada por el sitio residual de recombinación específica de sitio.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2008/003084.
Solicitante: ITI SCOTLAND LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: Scottish Enterprise Atrium Court 50 Waterloo Street Glasgow G2 6HQ REINO UNIDO.
Inventor/es: SCHEER,Nico.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- C12N15/90 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Introducción estable de ADN extraño en el cromosoma.
- C12N9/02 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Oxidorreductasas (1.), p. ej. luciferasa.
PDF original: ES-2384760_T3.pdf
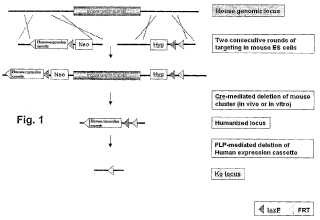
Fragmento de la descripción:
Deleción de un grupo de genes y humanización en dos etapas Campo de la invención La presente invención se refiere, en general, a un procedimiento de humanización de un ratón. En concreto, la invención se refiere a un procedimiento para reemplazar un grupo de genes murinos por un único gen o por múltiples genes del correspondiente grupo de genes humanos mediante el uso de una combinación de recombinación homóloga y recombinación específica de sitio.
Antecedentes de la invención Los modelos murinos son una herramienta inestimable para la investigación de enfermedades humanas, y se usan ampliamente para estudiar la evolución de muchas enfermedades y para probar posibles agentes terapéuticos. Convencionalmente, se han producido ratones transgénicos mediante la inyección pronuclear de ADN exógeno. Más recientemente, se han generado ratones mediante la fusión de una célula madre embrionaria (ES) con una célula que contiene un Cromosoma Artificial Bacteriano (CAB) o un Cromosoma Artificial de Levadura (CAL) que comprende el gen exógeno de interés y un marcador seleccionable para evaluar la integración del segmento de ADN exógeno en el genoma de la célula embrionaria, según lo descrito, por ejemplo, en el documento WO94/02602. Dichos procedimientos se basan en la integración del CAB o del CAL en el genoma de la célula madre embrionaria mediante el procedimiento de recombinación homóloga. Debido a las exigencias técnicas del manejo de los CAB y los CAL, y a las bajas velocidades de transfección de las células ES cuando se usan constructos de ADN de gran tamaño, la realización de la transgénesis de esta manera lleva mucho tiempo, y es ineficaz e imprecisa.
Wallace et al. (Cell 128, 197-209 2007) describió recientemente un procedimiento conocido como reemplazo genómico mediado por recombinasa (RMGR) . Este procedimiento utiliza la recombinación específica de sitio para reemplazar un alelo murino por un alelo humano del gen ortólogo. Se insertan dos sitios de recombinación específica de sitio no interactivos (loxP y lox511) en el cromosoma murino que flanquean el gen diana mediante recombinación homóloga. Se inserta un par idéntico de sitios de recombinación específica de sitio no interactivos en un CAB de manera que flanquean el alelo humano del gen diana. La introducción del CAB en la célula murina y la posterior expresión de la recombinasa específica de sitio produce dos reacciones de recombinación específica de sitio entre los sitios de recombinación específica de sitio compatibles del CAB y del cromosoma murino (loxP/loxP y lox511/lox511) , y el intercambio recíproco de la secuencia de genes humanos por la secuencia murina. Sin embargo, este procedimiento contiene múltiples etapas que se deben realizar en una célula madre embrionaria, lo que lleva a deficiencias, en buena parte, debidas a que a menudo se perturba el cariotipo de la célula. Así pues, sigue existiendo la necesidad de un procedimiento racionalizado para humanizar un ratón que, idealmente, requeriría la realización de menos etapas en una célula madre embrionaria y que, por tanto, subsanaría alguno de estos problemas de falta de eficiencia.
Además, la invención pretende resolver otro problema del campo de la generación de ratones humanizados. Por ejemplo, los procedimientos anteriormente descritos para generar modelos murinos humanizados se han centrado simplemente en el reemplazo de un único gen murino endógeno por el correspondiente gen humano. Esto es un procedimiento aceptable para aquellos locus de genes en los que un gen murino corresponde a un gen humano. Sin embargo, en la evolución, se pueden desarrollar grupos de genes que, a menudo, sufren repetidos cambios, tales como la duplicación y la diversificación, de manera que el grupo puede variar significativamente entre las diferentes especies. Por lo tanto, en un grupo, a veces no es posible identificar verdaderamente los genes ortólogos entre las especies. En los casos extremos, puede que sólo haya un gen funcional (s) en un grupo de una especie, pero muchos más en otro. Uno de dichos ejemplos es el grupo de genes CYP2D de las enzimas metabólicas, que sólo presenta un gen funcional en seres humanos (CYP2D6) , pero nueve genes funcionales en ratones. En dichos casos, el reemplazo de un solo gen murino por el gen humano ortólogo mediante el mecanismo convencional de recombinación homóloga de direccionamiento génico no producirá una humanización funcional debido a la expresión de genes residuales del grupo murino.
Además, en muchos casos, el producto génico de un gen puede constituir la funcionalidad principal de todo el grupo (p.ej., CYP3A4 del grupo CYP3A humano o CYP2C9 del grupo CYP2C humano) y podría ser imposible identificar un homólogo funcional de este gen en otras especies. Esto provoca incertidumbre en cuanto a qué gen ha de ser reemplazado y por cuál. A esto, se añade el problema de que, en realidad, puede no ser posible realizar la deleción de un fragmento de ADN de gran tamaño del cromosoma murino, que constituya un grupo de genes entero, en una sola etapa, debido a la falta de eficacia de la recombinación homóloga si los brazos dirigidos están demasiado separados en el cromosoma murino.
Un procedimiento de generación de modelos murinos humanizados en el que el locus humanizado refleje correctamente los locus de genes humanos equivalentes de interés permitiría investigar de manera más realista las funciones de los genes codificados en dichos locus y facilitar la investigación en la intervención terapéutica de afecciones que están asociadas con genes que forman parte de los grupos de genes de funcionalidad similar.
En la técnica, se sabe que es posible utilizar recombinasas específicas de sitio para dirigir la recombinación homóloga a ubicaciones cromosómicas específicas (véase Jessen et al., 1997) . El uso de dichas recombinasas específicas de sitio permite iniciar la recombinación previa solicitud mediante la adición de la recombinasa específica de sitio.
El documento US2007/0061900 describe un procedimiento para humanizar locus de genes de la región variable de cadena pesada y cadena ligera de inmunoglobulinas. Este procedimiento implica la inserción en cada uno de dos vectores, denominados LTVEC, de un sitio de recombinación específica de sitio en una posición contigua a una parte de la región variable de la inmunoglobulina humana. Luego se alinean estos LTVEC y se introducen en el genoma de una célula murina mediante recombinación homóloga, de manera que los sitios de recombinación específica de sitio flanqueen las secuencias de la región variable de la inmunoglobulina murina, y las secuencias parciales de la región variable de inmunoglobulina humana flanqueen los sitios de recombinación específica de sitio. La realización de la recombinación específica de sitio escinde la secuencia de la región variable de la inmunoglobulina murina y une las dos secuencias parciales de región variable de inmunoglobulina humana, estando el sitio de recombinación específica de sitio residual contenido en ella. Los ratones resultantes producen anticuerpos híbridos que contienen la región variable humana y la región constante murina, siendo necesarias posteriores etapas de transformación para permitir la producción de anticuerpos humanos puros. La naturaleza segmentada de la región variable de la inmunoglobulina permite que el sitio de recombinación específica de sitio residual permanezca en la secuencias de ácidos nucleicos con una escasa probabilidad de sufrir un efecto perjudicial. Sin embargo, no hay indicios de que esta tecnología se pueda utilizar para la humanización de genes no segmentados, en los que la presencia de una secuencia de ácidos nucleicos que codifique un sitio de recombinación específica de sitio residual en el gen eliminaría su capacidad de ser transcrito. La solicitud WO2006064197 revela un procedimiento para humanizar un ratón para un grupo de genes de interés que comprende las etapas de dos series dirigidas consecutivas en células ES para incorporar un par de sitios de recombinación específica de sitio en el genoma murino, de modo que la secuencia diana murina que se vaya a reemplazar esté flanqueada a cada lado por un sitio de recombinación con dos tipos de vectores dirigidos. La deleción mediada por Cre in vivo da como resultado una desactivación del grupo de genes murinos flanqueado por loxP. Se hizo necesaria una etapa más de recombinación mediada por Cre con ADN de CAB que comprendía el gen de reemplazo humano para introducir las secuencias humanas mediante inserción mediada por Cre en células ES rederivadas. Los casetes de selección que flanquean los grupos de genes humanizados... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para humanizar un ratón para un gen de interés, que comprende:
a) incorporar un par de sitios de recombinación específica de sitio en el genoma murino mediante recombinación homóloga, de manera que la secuencia diana de genes murinos que se vaya a reemplazar esté flanqueada a cada lado por un sitio de recombinación; en el que al menos uno de los dos sitios de recombinación se crean para que sean contiguos a una secuencia de genes humanos de reemplazo; y siendo dicha secuencia de genes humanos de reemplazo colocada para que dicho sitio de recombinación se encuentre entre dicha secuencia de genes humanos de reemplazo y dicha secuencia diana de genes murinos; b) realizar la recombinación entre los sitios de recombinación específica de sitio, de modo que la secuencia humana se introduzca en la posición del genoma murino previamente ocupada por el gen diana murino, flanqueada por el sitio residual de recombinación específica de sitio.
2. El procedimiento de la reivindicación 1, en el que la secuencia de genes humanos de reemplazo se inserta en el punto del cromosoma murino en el que el gen diana murino equivalente endógeno se encuentra de manera natural.
3. El procedimiento de la reivindicación 1 ó 2, en el que la secuencia de genes humanos de reemplazo contiene un grupo de genes, opcionalmente, un grupo de genes que codifican proteínas implicadas en el metabolismo farmacológico, tal como un grupo de genes que forma parte de un grupo de genes del citocromo P450 (CYP) .
4. El procedimiento de una cualquiera de las reivindicaciones anteriores, en el que la transcripción de dicha secuencia de genes humanos de reemplazo está bajo el control de una o más secuencias reguladoras murinas endógenas o la/s secuencia/s reguladora/s humana/s endógena/s.
5. El procedimiento de una cualquiera de las reivindicaciones anteriores, en el que cada sitio de recombinación específica de sitio se crea para que sea contiguo a un marcador seleccionable.
6. El procedimiento de la reivindicación 5, en el que cada marcador seleccionable se sitúa de modo que dicho marcador seleccionable se encuentra entre dicha secuencia diana murina y dicho sitio de recombinación.
7. El procedimiento de la reivindicación 5 o la reivindicación 6, en el que cada uno de dichos marcadores seleccionables son diferentes entre sí.
8. El procedimiento de la reivindicación 1, en el que se incorpora un segundo par de sitios de recombinación específica de sitio en el genoma murino; en el que cada sitio del segundo par de sitios de recombinación flanquea el primer par de sitios de recombinación, de modo que la secuencia humana de reemplazo se puede escindir realizando una recombinación específica de sitio entre este segundo par de sitios.
9. El procedimiento de la reivindicación 8, en el que la secuencia de genes humanos de reemplazo está situada entre la mitad del primer par de sitios de recombinación específica de sitio y la mitad del segundo par de sitios de recombinación específica de sitio.
10. El procedimiento de la reivindicación 8 o la reivindicación 9, que comprende además realizar una segunda serie de recombinación entre el segundo par de sitios de recombinación específica de sitio, de modo que se escinda la secuencia de genes humanos de reemplazo y se desactive el gen de interés.
11. El procedimiento de una cualquiera de las reivindicaciones anteriores, en el que la recombinación específica de sitio tiene lugar en una célula madre embrionaria murina.
12. El procedimiento de la reivindicación 11, en el que la célula madre embrionaria se inserta posteriormente en un blastocisto y, opcionalmente, en el que después se transplanta el blastocisto en un ratón pseudo-preñado.
13. El procedimiento de una cualquiera de las reivindicaciones anteriores, en el que la recombinación específica de sitio se realiza in vivo y la recombinación específica de sitio se realiza cruzando un ratón transgénico generado según una cualquiera de las reivindicaciones anteriores con un ratón que expresa una recombinasa específica de sitio que reconoce los sitios de recombinación específica de sitio usados al incorporar la secuencia de genes humanos de reemplazo en el genoma del ratón transgénico.
14. El procedimiento de la reivindicación 13, en el que la expresión de la recombinasa específica de sitio se limita a un determinado tejido.
15. El procedimiento de la reivindicación 14, en el que la recombinasa es albúmina-Cre.
FRT
FRT
FRT loxP
Patentes similares o relacionadas:
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Ratones con un sistema inmunitario humanizado con células dendríticas reforzadas, del 22 de Julio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un ratón Rag-/-, γc-/-, Flk2-/- deficiente para el gen activador de recombinación 2 (Rag2) y/o el gen activador de recombinación 1 (Rag1), cadena gamma […]
Procedimientos de tratamiento del cáncer usando antagonistas de unión al eje de PD-1 e inhibidores de TIGIT, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo antagonista anti-PD-L1 o fragmento de unión a antígeno del mismo y un anticuerpo antagonista anti-TIGIT o fragmento de unión a antígeno del mismo para su uso […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Roedores con alelos mutantes de Acvr1 condicionales, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una construcción de ácido nucleico que comprende: (i) un exón 5 de Acvr1 que codifica una secuencia de tipo silvestre a nivel de proteína, […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]
Polinucleótidos que codifican anticuerpos de roedores con idiotipos humanos y animales que los contienen, del 29 de Abril de 2020, de Open Monoclonal Technology, Inc: Un polinucleótido quimérico que comprende, en orden 5' a 3', un gen de región variable (V) de inmunoglobulina (Ig) humana, un gen de región de diversidad (D) de […]
Ratones ADAM6, del 22 de Abril de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón que ha experimentado reordenación de secuencia génica de inmunoglobulina de modo que exprese un linfocito B que comprende una secuencia de inmunoglobulina reordenada […]