Composición farmacéutica sinérgica, útil para inhibir la neovascularización (angiogénesis) corneal y retinal, y de otros órganos, en un humano o animal.
Una composición farmacéutica sinérgica, útil para inhibir Ia neovascularización (angiogénesis) corneal y retinal,
y de otros órganos, en un humano o animal, caracterizada porque comprende, en unvehículo o portador farmacéuticamente aceptable: 60 a 90 % en peso de Suramina, o el equivalente de una de sus sales farmacéuticamente aceptables; y 40 a 10 % en peso de Bevacizumab; en donde dichos porcentajes son con respecto a Ia suma de los pesos de ambosprincipios activos. Dicha composición farmacéutica sinérgica se presenta bajo Ia forma de una composición inyectable por vía endovenosa, intravítrea o subconjuntival, o bajo Ia forma para Ia administración tópica.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/MX2008/000104.
Solicitante: Asociación Civil De Estudios Superiores.
Nacionalidad solicitante: Argentina.
Dirección: Av. Juan de Garay No. 125 Ciudad de Buenos Aires C1063ABB ARGENTINA.
Inventor/es: GALLO BARRACO,Juan Eduardo María.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K45/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
- A61P27/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 27/00 Medicamentos para tratar los trastornos de los sentidos. › Agentes oftálmicos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
PDF original: ES-2385121_T3.pdf
Fragmento de la descripción:
Composición farmacéutica sinérgica, útil para inhibir la neovascularización (angiogénesis) corneal y retinal, y de otros órganos, en un humano o animal
CAMPO DE LA INVENCIÓN
La Suramina (suramin, suramine) es una droga conocida desde hace muchos años para el tratamiento de enfermedades causadas por nematodos y protozoos. También se han descrito sus propiedades como agente antineoplásico a través de varios mecanismos: inhibición de la angiogénesis de tumores, incremento de la sensibilidad celular a sustancias citotóxicas (quimioterapia) y acción citotóxica por sí misma.
Químicamente, la Suramina puede ser denominada como ácido 8-[[4-metil-3-[[3-[[3-[[2-metil-5-[ (4, 6, 8trisulfonaftalen-1-il) carbamoil]fenil]carbamoil]fenil]carbamoil]amino]benzoil]amino]-naftalen-1, 3, 5-trisulfónico, de fórmula empírica es C51H40N6O23S6 y número CAS 145-63-1.
El Bevacizumab, una sustancia biológicamente activa conocida por su efecto anti-VEGF (factor de crecimiento endotelial vascular) , inhibe la angiogénesis. Se utiliza en el cáncer de colón por su efecto antiangiogénico disminuyendo el crecimiento tumoral y en el tratamiento de enfermedades oftalmológicas que desarrollan neovascularización, como la retinopatía diabética, la degeneración macular relacionada con la edad tipo exudativa y otras.
Recientemente, el Bevacizumab se ha utilizado en oftalmología como un agente intravítreo en el tratamiento de las enfermedades proliferativas (neovascularización) de los ojos. Además, se ha aprobado como nueva indicación para el tratamiento de cáncer de mama en varios países.
De manera inesperada y sorprendente, se ha encontrado que una nueva composición farmacéutica que comprende Suramina y Bevacizumab (denominada en adelante suramab) administrada en una dosis relativamente baja posee gran efecto antiangiogénico, de carácter sinérgico, con mayor intensidad y duración que el efecto producido por una monodosis de Bevacizumab o de Suramina.
BREVE DESCRIPCIÓN DE LA INVENCIÓN ASPECTOS MEDICOS A) Angiogénesis corneal
El objetivo de la presente invención es proporcionar una composición farmacéutica que comprenda Suramina, un antagonista purinérgico no específico, y Bevacizumab, una sustancia anti-VEGF, en el desarrollo de la angiogénesis corneal.
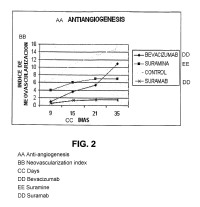
Para tales propósitos, se utilizó un método bien conocido para inducir neovascularización en la córnea. La aparición de vasos de neoformación en la córnea fue documentada a través de una cámara digital a lo largo de un período de 35 días. El efecto de suramab (Suramina + Bevacizumab) en animales fue comparado con el de otros tres grupos de animales tratados con Bevacizumab, tratados con Suramina y sin ningún tipo de tratamiento (grupo de control) .
El suramab administrado por vía endovenosa disminuyó marcadamente el desarrollo de neovasos en la córnea y tuvo un efecto significativamente mayor y duradero que el de los otros grupos animales durante los 35 días de seguimiento. Los resultados han revelado que el suramab tiene un marcado efecto antiangiogénico, capaz de detener la neovascularización corneal y en otros lugares del organismo, constituyéndose en un nuevo agente farmacológico para el tratamiento antiangiogénico.
B) Angiogénesis tumoral
Otro objetivo de la presente invención es proporcionar una composición farmacéutica que comprenda Suramina, un antagonista purinérgico no específico, y Bevacizumab, una sustancia anti-VEGF, en el desarrollo de la angiogénesis tumoral y en la supervivencia del animal de experimentación.
Para tal fin, se utilizó un modelo animal bien conocido. Brevemente, se inocularon células CT26 (adenocarcinoma de colon) , en forma subcutánea, en la región dorso-lateral de las ratas. Al 7.º día de inoculación, se formaron 4 grupos de animales que recibieron por vía intravenosa distintos tratamientos: suramab, Bevacizumab, Suramina, solución fisiológica (control) . Se midieron los tumores tres veces por semana, se calculó el volumen tumoral siguiendo una fórmula conocida y se evaluó la supervivencia de los animales. Los grupos tratados fueron comparados con el grupo de control.
Sólo el grupo tratado con suramab presenta una disminución estadísticamente significativa del volumen tumoral a los 31 días respecto al grupo de control. Además, es el grupo que posee el mayor porcentaje de supervivencia a los 35 días.
DESCRIPCIÓN DETALLADA DE LAS FIGURAS
La Figura 1 ilustra el desarrollo de neovasos corneales 21 días después de la lesión: A) control; B) Bevacizumab; C) Suramina; D) suramab. La Figura 2 muestra la evolución de los neovasos (índice de neovascularización) en función del transcurso del tiempo (días) del ensayo para los cuatro grupos de animales. La Figura 3 ilustra el porcentaje de supervivencia en el transcurso del tiempo (días) del ensayo del modelo de angiogénesis oncológica para los cuatro grupos de animales hasta los 35 días. La Figura 4 muestra el volumen tumoral (promedio) en el transcurso del tiempo (días) del ensayo del modelo de angiogénesis oncológica para los cuatro grupos de animales hasta los 31 días. La Figura 5 ilustra el volumen tumoral (promedio) a los 31 días del ensayo del modelo de angiogénesis oncológica para los cuatro grupos de animales.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN I.ANGIOGENESIS I.1. Introducción
La córnea, ubicada en la parte anterior del ojo, es un tejido transparente y avascular. Algunas patologías oculares pueden causar pérdida de su avascularidad y transparencia, produciendo disminución o pérdida de la visión. Se estima que en los Estados Unidos un millón y medio de pacientes desarrollan neovascularización corneal, algunos de ellos con pérdida de visión, llamados pacientes ciegos por córnea (Brodovsky SC, McCarty CA, Snibson G, Loughnan M, Sullivan L, Daniell M, Taylor HR. Management of alkali burns: an 11-year retrospective review. Ophthalmology. 2000; 107: 182935) . Las causas más frecuentes de la invasión de vasos en la córnea (neovascularización corneal) son: infecciones oculares, como el virus herpes simple, secuelas de enfermedades, como el Pénfigo y el Síndrome de Steven Johnson, Pterigion gigante y, especialmente, las quemaduras con álcali. Las patologías mencionadas suelen cursar con daño severo o destrucción de las células troncales del limbo corneal (stem cells o células madre) , las cuales tendrían la función de no permitir el ingreso de vasos sanguíneos a través de la periferia corneal (Dua HS, Joseph A, Shanmuganathan VA, Jones RE. Stem cell differentiation and the effects of deficiency. Eye 2003;17:877-85) .
El manejo de la neovascularización corneal continúa siendo complejo, aunque se han logrado avances en el tratamiento de esta patología. Casos que se podrían beneficiar de un transplante de córnea convencional tienen mal pronóstico debido a la frecuente recurrencia de la neovascularización. La experiencia demuestra que es necesario disminuir significativamente la neovascularización antes de realizar el transplante de córnea convencional (Garg P, Krishna PV, Stratis AK, Gopinathan U. The value of corneal transplantation in reducing blindness. Eye. 2005;19:110614) .
Nuevos tratamientos, como por ejemplo el transplante de células madre del limbo corneal se encuentran en una etapa inicial de desarrollo. Sin embargo, en los pocos casos reportados no es raro encontrar recurrencia de la neovascularización corneal.
Los receptores de la superficie celular para nucleótidos extracelulares se denominan receptores P2. Estos son activados por nucleótidos como las purinas y/o pirimidinas. Los receptores P2 se dividen en dos grandes grupos: P2X y P2Y. Los receptores P2X están involucrados en el control del flujo de iones en la célula en respuesta al ATP (adenosin trifosfato) . Los receptores P2X participan en la neurotransmisión rápida y se encuentran en gran cantidad en los tejidos con función excitatoria. Los subtipos P2X1, P2X2, P2X3, etc., se encuentran descriptos en la bibliografía. Los receptores P2Y pertenecen a la familia de receptores acoplados a la Proteína G, y también se han encontrado varios tipos como P2Y1, P2Y2, etc. (Abbracchio MP, Burnstock G. Purinoceptors: are there families of P2X and P2Y purinoceptors? Pharmacol Ther 1994;64:445-75) .
Los receptores P2 se encuentran presentes en las células gliales, en la retina y también en la córnea (Lazarowski E, Boucher R, Harden T. Mechanisms of release of nucleotides and integration of their action as P2X-and... [Seguir leyendo]
Reivindicaciones:
1. Composición farmacéutica sinérgica, útil para inhibir la neovascularización (angiogénesis) corneal y retinal, en un humano o animal, caracterizada porque comprende, en un vehículo o portador farmacéuticamente aceptable: 60 a 90 % en peso de Suramina, o el equivalente de una de sus sales farmacéuticamente aceptables; y 40 a 10 % en peso de Bevacizumab; en donde dichos porcentajes son con respecto a la suma de los pesos de ambos principios activos.
2. Composición farmacéutica de acuerdo con la reivindicación 1, caracterizada porque comprende, en un vehículo o portador farmacéuticamente aceptable: aproximadamente 75 % en peso de Suramina, o el equivalente de una de sus sales farmacéuticamente aceptables; y aproximadamente 25 % en peso de Bevacizumab; en donde dichos porcentajes son con respecto a la suma de los pesos de ambos principios activos.
3. Composición farmacéutica de acuerdo con la reivindicación 1, caracterizada porque comprende: aproximadamente 0, 18 % en peso de Suramina, o el equivalente de una de sus sales farmcacéuticamente aceptables; y aproximadamente 0, 06 % en peso de Bevacizumab; siendo el resto un vehículo o portador farmacéuticamente aceptable, en donde los porcentajes están dados con respecto al peso total de la composición farmacéutica.
4. Composición farmacéutica de acuerdo con la reivindicación 1, caracterizada porque comprende: aproximadamente 0, 18 % en peso de Suramina bajo la forma de su sal hexa-sódica; y aproximadamente 0, 06 % en peso de Bevacizumab; siendo el resto un vehículo o portador farmacéuticamente aceptable, en donde los porcentajes están dados con respecto al peso total de la composición farmacéutica.
5. Composición farmacéutica de acuerdo con la reivindicación 1, caracterizada porque es una composición inyectable por vía endovenosa, intravítrea o subconjuntival, o es para la administración tópica.
Patentes similares o relacionadas:
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Terapias de combinación para el cáncer, del 22 de Julio de 2020, de MERCK SHARP & DOHME CORP: Una combinación que comprende un anticuerpo anti-PD-1 humano y un Compuesto A y un Compuesto B, en donde: el anticuerpo anti-PD-1 humano comprende […]