FORMULACIÓN DE FÁRMACO SÓLIDA Y DISPOSITIVO PARA EL ALMACENAMIENTO Y LA ADMINISTRACIÓN CONTROLADA DE LA MISMA.
Dispositivo para el almacenamiento y la liberación controlada de una forma sólida de un fármaco que comprende:
una parte de cuerpo; una pluralidad de depósitos ubicados en y definidos por la parte de cuerpo; un fármaco en una forma de matriz monolítica sólida porosa contenida en cada uno de los depósitos; y uno o más materiales excipientes dispersados por la totalidad de los poros de la matriz de fármaco y que llenan sustancialmente el espacio no ocupado de otra manera por la matriz de fármaco dentro de cada uno de los depósitos, en el que el material excipiente potencia la liberación del fármaco desde cada depósito
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/012757.
Solicitante: BOSTON SCIENTIFIC SCIMED, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE SCIMED PLACE MAPLE GROVE, MN 55311-1566 ESTADOS UNIDOS DE AMERICA.
Inventor/es: STAPLES, MARK, A., SANTINI, JOHN, T., JR., PRESCOTT,James,H, UHLAND,Scott,A.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Abril de 2004.
Clasificación Internacional de Patentes:
- A61K38/09 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormona que libera a la hormona luteinizante [LHRH]; Péptidos relacionados.
- A61K9/00L8
- A61K9/00Z8
Clasificación PCT:
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
PDF original: ES-2359243_T3.pdf


Fragmento de la descripción:
Esta invención está en general en el campo de los métodos y las composiciones para su uso en la administración de un fármaco a pacientes, y más específicamente a formulaciones de fármaco estabilizadas que comprenden formas sólidas de proteínas u otros tipos de principios activos. Esta invención también se refiere a métodos para la manipulación 5 controlada y el almacenamiento de proteínas inestables u otras moléculas y la mejora de la producción, el llenado y almacenamiento de formas secas de tales moléculas.
Muchas proteínas útiles y otras moléculas que son inestables en disoluciones acuosas se manipulan y almacenan como sólidos secos (“seco” se define en este documento como sustancialmente libre de humedad residual, normalmente con un contenido en agua que no supera el 10% p/p).El secado en masa y la liofilización (secado por congelación) son 10 formas útiles conocidas para estabilizar la estructura y la actividad de las proteínas. Los métodos tradicionales de secado por congelación implican la congelación de una disolución acuosa que contiene varios agentes estabilizantes, seguida por la aplicación de vacío para eliminar el agua por sublimación, produciendo un sólido poroso seco que es relativamente estable y adecuado para su almacenamiento a largo plazo.
Los sólidos secos (particularmente polvos) son frecuentemente sensibles a fuerzas de empaquetado, carga estática, 15 humedad y otras variables que pueden afectar a la manipulación de los polvos, haciendo difícil reproducir o administrar cantidades precisas, particularmente microcantidades, de los polvos. Por ejemplo, puede ser difícil controlar la predictibilidad o la repetibilidad de las características de liberación del polvo desde un dispositivo de administración de fármacos. Por consiguiente sería ventajoso minimizar o eliminar tales dificultades. Por consiguiente sería deseable proporcionar métodos mejorados para el almacenamiento y la liberación de formas sólidas secas estables de proteínas 20 y otros principios activos, particularmente desde depósitos de microescala que contienen una formulación farmacéutica.
Además y de manera más general, sería deseable proporcionar composiciones y métodos para manipular y procesar de manera precisa, almacenar de manera estable y administrar de manera exacta formulaciones de fármaco, particularmente proteínas y péptidos a altas concentraciones.
Sumario de la invención 25
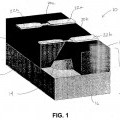
En un aspecto, se proporciona un dispositivo para el almacenamiento y la liberación controlada de una forma sólida de un fármaco. En una realización, este dispositivo comprende una parte de cuerpo; uno o más depósitos ubicados en y definidos por la parte de cuerpo; una matriz monolítica sólida porosa que comprende un fármaco y que está contenida en cada uno del uno o más depósitos; y uno o más materiales excipientes dispersados por la totalidad de los poros dentro de la matriz sólida y que llenan sustancialmente cualquier espacio no ocupado de otra manera por la matriz 30 sólida en cada uno del uno o más depósitos, en el que el material excipiente potencia la estabilidad del fármaco mientras está almacenado en el uno o más depósitos o potencia la liberación del fármaco desde cada depósito.
En varias realizaciones, al menos uno del uno o más materiales excipientes está en un estado sólido, líquido, semisólido o de gel a condiciones ambiente.
En una realización, el uno o más materiales excipientes son no acuosos. Por ejemplo, el material excipiente puede 35 comprender un polímero, tal como un polietilenglicol. En una realización, el polietilenglicol tiene un peso molecular de entre aproximadamente 100 y 10.000 Da. En otra realización, al menos uno del uno o más materiales excipientes comprende un perhalohidrocarburo o un hidrocarburo saturado no sustituido. Aún en otra realización, al menos uno del uno o más materiales excipientes comprende dimetilsulfóxido o etanol. En una realización adicional, al menos uno del uno o más materiales excipientes comprende un aceite farmacéuticamente aceptable. Todavía en una realización 40 adicional, el material excipiente comprende una disolución saturada del fármaco.
En una realización, el fármaco comprende un aminoácido, un péptido o una proteína. En diversas realizaciones, el fármaco se selecciona de glicoproteínas, enzimas, hormonas, interferones, interleucinas y anticuerpos. Por ejemplo, el fármaco puede comprender una hormona paratiroidea humana, una hormona liberadora de hormona leuteinizante, una hormona liberadora de gonadotropina o un análogo de las mismas. Aún en otra realización, el fármaco comprende un 45 péptido natriurético.
En una realización, el uno o más depósitos son microdepósitos. Por ejemplo, el volumen de cada depósito es de entre 10 nl y 500 nl en una realización particular. En otra realización, cada uno del uno o más depósitos tiene un volumen de entre 10 l y 500 l.
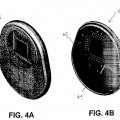
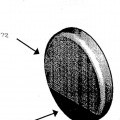
La parte de cuerpo puede adoptar una variedad de formas. En diversas realizaciones, la parte de cuerpo está en forma 50 de un chip, un disco, un tubo, una esfera o una endoprótesis. La parte de cuerpo puede comprender, por ejemplo, silicio, un metal, una cerámica, un polímero o una combinación de los mismos.
En una realización preferida, el dispositivo comprende una pluralidad de depósitos ubicados en posiciones diferenciadas a lo largo de al menos una superficie de la parte de cuerpo. En una realización, cada depósito tiene una abertura
cubierta por una tapa de depósito impermeable que puede romperse selectivamente para iniciar la liberación del fármaco desde el depósito.
En una realización, un primer material excipiente se dispersa por la totalidad de los poros o intersticios dentro de la matriz sólida y un segundo material excipiente llena sustancialmente el espacio del depósito no ocupado por el primer material excipiente en cada uno del uno o más depósitos. 5
En una realización preferida, el uno o más materiales excipientes, tras la exposición a un disolvente ambiental (por ejemplo, un fluido fisiológico) para el fármaco, fomenta la disolución del fármaco para potenciar la liberación del fármaco desde el depósito. En una realización, el uno o más materiales excipientes evitan la agregación o la precipitación del fármaco tras la exposición a un fluido ambiental para potenciar la liberación del fármaco desde el depósito.
En una realización, el dispositivo está adaptado para la implantación en un paciente, y el material excipiente comprende 10 un disolvente orgánico. Preferiblemente, el dispositivo libera in vivo una cantidad del disolvente orgánico que es inferior a la exposición diaria máxima predeterminada para el disolvente orgánico.
En otro aspecto, se proporciona un método para preparar un dispositivo para el almacenamiento y la liberación controlada de una forma sólida de un fármaco. En una realización, el método comprende: proporcionar un fármaco en forma de matriz porosa, seca; y combinar con la matriz de fármaco al menos un material excipiente que llena 15 sustancialmente los poros e intersticios dentro de la matriz para formar un material compuesto fármaco/excipiente, en el que el material compuesto fármaco/excipiente, solo o en combinación con otro material excipiente, llena sustancialmente cada uno del uno o más depósitos ubicados en una parte de cuerpo de un dispositivo para el almacenamiento y la liberación controlada del fármaco.
En una realización, la forma de matriz porosa, seca del fármaco se proporciona en primer lugar en el uno o más 20 depósitos y después se añade el material excipiente fluidificado al uno o más depósitos. En una realización, el método comprende además solidificar el material excipiente fluidificado.
En una realización, la forma de matriz porosa, seca del fármaco se forma mediante un método que comprende: disolver o dispersar un fármaco en un medio líquido volátil para formar un primer fluido; depositar una cantidad del primer fluido en cada uno del uno o más depósitos; y secar la cantidad volatilizando el medio líquido volátil para producir la matriz 25 porosa, seca del fármaco en el uno o más depósitos.
En otra realización, el al menos un material excipiente está en estado fundido cuando se combina con la matriz de fármaco.
Aún en otra realización, la forma de matriz porosa seca de fármaco y el al menos un material excipiente se combinan juntos en primer... [Seguir leyendo]
Reivindicaciones:
1. Dispositivo para el almacenamiento y la liberación controlada de una forma sólida de un fármaco que comprende:
una parte de cuerpo;
una pluralidad de depósitos ubicados en y definidos por la parte de cuerpo;
un fármaco en una forma de matriz monolítica sólida porosa contenida en cada uno de los depósitos; y 5
uno o más materiales excipientes dispersados por la totalidad de los poros de la matriz de fármaco y que llenan sustancialmente el espacio no ocupado de otra manera por la matriz de fármaco dentro de cada uno de los depósitos,
en el que el material excipiente potencia la liberación del fármaco desde cada depósito.
2. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes es sólido en condiciones ambiente. 10
3. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes es líquido en condiciones ambiente.
4. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes es un semisólido o un gel en condiciones ambiente.
5. Dispositivo según la reivindicación 1, en el que uno o más materiales excipientes son no acuosos. 15
6. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes comprende un polímero.
7. Dispositivo según la reivindicación 6, en el que el polímero comprende polietilenglicol.
8. Dispositivo según la reivindicación 7, en el que el polietilenglicol tiene un peso molecular de entre aproximadamente 100 y 10.000 Da. 20
9. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes comprende un perhalohidrocarburo o hidrocarburo saturado no sustituido.
10. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes comprende dimetilsulfóxido o etanol.
11. Dispositivo según la reivindicación 1, en el que al menos uno del uno o más materiales excipientes comprende un 25 aceite farmacéuticamente aceptable.
12. Dispositivo según una cualquiera de las reivindicaciones 1 a 11, en el que el fármaco comprende un aminoácido, un péptido o una proteína.
13. Dispositivo según una cualquiera de las reivindicaciones 1 a 11, en el que el fármaco se selecciona del grupo que consiste en glicoproteínas, enzimas, hormonas, interferones, interleucinas y anticuerpos. 30
14. Dispositivo según una cualquiera de las reivindicaciones 1 a 11, en el que el fármaco comprende una hormona paratiroidea humana, hormona liberadora de hormona leuteinizante, una hormona liberadora de gonadotropina o un análogo de las mismas.
15. Dispositivo según una cualquiera de las reivindicaciones 1 a 11, en el que el fármaco comprende un péptido natriurético. 35
16. Dispositivo según una cualquiera de las reivindicaciones 1 a 15, en el que los depósitos son microdepósitos.
17. Dispositivo según la reivindicación 16, en el que el volumen de cada depósito es de entre 10 nl y 500 nl.
18. Dispositivo según la reivindicación 1, en el que los depósitos tienen individualmente un volumen de entre 10 l y 500 l.
19. Dispositivo según una cualquiera de las reivindicaciones 1 a 18, en el que la parte de cuerpo está en forma de un 40 chip, un disco, un tubo, una endoprótesis o una esfera.
20. Dispositivo según una cualquiera de las reivindicaciones 1 a 19, en el que la parte de cuerpo comprende silicio, un metal, un polímero, una cerámica o una combinación de los mismos.
21. Dispositivo según una cualquiera de las reivindicaciones 1 a 20, en el que cada depósito tiene una abertura cubierta por una tapa de depósito impermeable que se rompe selectivamente para iniciar la liberación del fármaco desde el depósito.
22. Dispositivo según la reivindicación 21, en el que la tapa del depósito comprende una película metálica que se disgrega mediante ablación electrotérmica. 5
23. Dispositivo según la reivindicación 1, en el que un primer material excipiente se dispersa por la totalidad de los poros o intersticios dentro de la matriz sólida y un segundo material excipiente ocupa espacio del depósito no ocupado por el primer material excipiente o la matriz sólida, dentro de cada uno de los depósitos.
24. Dispositivo según la reivindicación 1, en el que el uno o más materiales excipientes, tras la exposición a un disolvente ambiental para el fármaco, fomenta la disolución del fármaco para potenciar la liberación del fármaco desde 10 el depósito.
25. Dispositivo según la reivindicación 1, en el que el uno o más materiales excipientes evitan la agregación o la precipitación del fármaco tras la exposición a un fluido ambiental para potenciar la liberación del fármaco desde el depósito.
26. Dispositivo según una cualquiera de las reivindicaciones 1 a 25, adaptado para su implantación en un paciente. 15
27. Dispositivo según la reivindicación 26, en el que el dispositivo libera in vivo un excipiente de disolvente orgánico en una cantidad que es inferior a la exposición diaria máxima predeterminada para el disolvente orgánico.
28. Método para preparar un dispositivo para el almacenamiento y la liberación controlada de una forma sólida de un fármaco que comprende:
proporcionar una parte de cuerpo del dispositivo que tiene una pluralidad de depósitos ubicados en la misma, estando 20 adaptado el dispositivo para el almacenamiento y la liberación controlada de un fármaco;
proporcionar en los depósitos un fármaco en forma de matriz monolítica sólida porosa; y
combinar con la matriz de fármaco al menos un material excipiente que llena sustancialmente los poros de la matriz de fármaco para formar un material compuesto fármaco/excipiente,
en el que el material compuesto fármaco/excipiente, solo o en combinación con otro material excipiente, llena 25 sustancialmente cada uno de los depósitos.
29. Método según la reivindicación 28, en el que la matriz de fármaco se proporciona en primer lugar en el uno o más depósitos y después se añade el material excipiente fluidificado a los depósitos.
30. Método según la reivindicación 28, en el que la matriz de fármaco se forma mediante un método que comprende:
disolver o dispersar un fármaco en un medio líquido volátil para formar un primer fluido; 30
depositar una cantidad del primer fluido en cada uno de los depósitos; y
secar la cantidad mediante volatilización del medio líquido volátil para producir la matriz monolítica sólida del fármaco en los depósitos.
31. Método según la reivindicación 28, en el que al menos un material excipiente está en estado fundido cuando se combina con la matriz de fármaco. 35
32. Método según la reivindicación 28, en el que la matriz de fármaco y el al menos un material excipiente se combinan juntos en primer lugar fuera de los depósitos para formar un material compuesto fármaco/excipiente y después se carga el material compuesto fármaco/excipiente en los depósitos.
33. Método según la reivindicación 32, en el que el material compuesto fármaco/excipiente se solidifica para dar una preforma antes de cargarse en los depósitos, conformándose cada preforma para ajustarse en y llenar sustancialmente 40 uno de los depósitos.
34. Método según la reivindicación 32, en el que el material compuesto fármaco/excipiente se extruye en estado fundido en los depósitos.
35. Método según la reivindicación 29, que comprende además solidificar el material excipiente fluidificado.
36. Método según la reivindicación 28, en el que el material excipiente comprende una disolución saturada del fármaco. 45
37. Método según cualquiera de las reivindicaciones 28 a 36, en el que los depósitos son microdepósitos.
Patentes similares o relacionadas:
Método para sincronizar el tiempo de inseminación en cerdas primerizas, del 29 de Abril de 2020, de United-AH II, LLC: Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de: […]
Modulador de receptor de andrógeno en combinación con acetato de abiraterona y prednisona para tratar el cáncer de próstata, del 15 de Abril de 2020, de Aragon Pharmaceuticals, Inc: Un compuesto de fórmula (I), o una sal farmacéuticamente aceptable del mismo, para uso en un método de tratamiento de cáncer de próstata resistente a la castración […]
Composición farmacéutica de microesferas de liberación sostenida de goserelina, del 12 de Junio de 2019, de SHANDONG LUYE PHARMACEUTICAL CO., LTD: Una composición farmacéutica de microesferas de goserelina de liberación sostenida, que comprende goserelina o una sal de la misma, poli(lactida-co-glicólido) […]
Composiciones de liberación controlada, del 5 de Junio de 2019, de Evonik Corporation: Una composición que comprende un agente bioactivo y un polímero en una fase orgánica que contiene uno o más disolventes; y un ion orgánico en una fase acuosa, en […]
Composición farmacéutica de liberación lenta hecha de micropartículas, del 20 de Diciembre de 2018, de Debiopharm International SA: Composición farmacéutica hecha de micropartículas para la liberación lenta de una triptorelina agonista de LHRH, caracterizada por que dicha […]
Microcápsulas de liberación sostenida basadas en poli(lactida-co-glicólido) que comprenden un polipéptido y un azúcar, del 15 de Noviembre de 2018, de Amylin Pharmaceuticals, LLC: Un proceso para preparar una composición farmacéuticamente aceptable en forma de micropartículas para la liberación sostenida de exendina-4, que comprende: […]
COMPOSICIÓN VETERINARIA PARA LA FABRICACIÓN DE UN ADITIVO SEMINAL ÚTIL PARA INSEMINACIÓN ARTIFICIAL EN ANIMALES, del 7 de Junio de 2018, de UNIVERSIDAD DE LEON: Composición veterinaria para la fabricación de un estimulante seminal útil para inseminación artificial en animales. La presente invención se refiere a una composición para la […]
Sistema terapéutico transdérmico para la administración de péptidos, del 16 de Mayo de 2018, de LTS LOHMANN THERAPIE-SYSTEME AG: Sistema terapéutico transdérmico (TTS) para la administración de un péptido sobre la piel tratada de forma ablativa de un paciente que comprende una capa […]