USO DE CELULAS MADRE PARA INDUCIR LA DIFERENCIACION NEURAL.
a) un factor neurotrófico que comprende un factor neurotrófico derivado de líneas celulares gliales (GDNF) o
b) un factor neurotrófico que comprende un polipéptido activador de la adenilato ciclasa de la pituitaria (PACAP)
para su uso en el tratamiento de enfermedades neurológicas
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05253870.
Solicitante: CHENG, HENRICH.
Nacionalidad solicitante: Taiwan, Provincia de China.
Dirección: NO. 322 SHIH-PAI ROAD, SEC. 2,PEI-TOU DISTRICT T'AI PEI.
Inventor/es: CHENG,HENRICH, TZENG,SHUN-FEN.
Fecha de Publicación: .
Fecha Solicitud PCT: 22 de Junio de 2005.
Fecha Concesión Europea: 9 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K38/18F
Clasificación PCT:
- A61K31/7076 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo purinas, p. ej. adenosina, ácido adenílico.
- A61K38/18 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento; Reguladores de crecimiento.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- C12N5/074 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre adultas.
Clasificación antigua:
- A61K31/7076 A61K 31/00 […] › conteniendo purinas, p. ej. adenosina, ácido adenílico.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61P25/00 A61P […] › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- C12N5/06
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Uso de células madre para inducir la diferenciación neural.
Antecedentes de la invención
La invención se refiere principalmente al tratamiento de trastornos neurológicos.
La pérdida de células neurales después del daño del sistema nervioso central (SNC) hace difícil la reparación del SNC. Muchos estudios muestran que las células madre neurales (CMN) aisladas de varias áreas del SNC de roedores y humanos son capaces de diferenciarse en células neurales en el SNC adulto de roedor bajo la influencia de factores de crecimiento ambientales y/o exógenos (F.H. Gage, Mammalian neural stem cells. Science. 287 (2000) 1433-1438; J. Price, B.P. Williams, Neural stem cells, Curr. Opin. Neurobiol. 11(2001) 564-567). Por tanto, se cree que el reabastecimiento de CMN es una estrategia potencial para el tratamiento del SNC humano (D.A. Peterson, Stem cells in brain plasticity and repair, Curr. Opin. Pharmacol. 2(2002) 34-42).
Las células madre derivadas de la médula ósea humana (CMMO) son heterogéneas en morfología. Ellas se diferencian de manera multipotencial en adipocitos de osteoblastos, condrocitos y músculo y pueden también generar neuronas (E. Mezey, K.J. Chandross, G. Harta, R.A. Maki, S.R. McKercher, Turning Blood into Brain: Cells Bearing Neuronal Antigens Generated in vivo from Bone Marrow. Science, 290(2000) 1779-1782; E. Mezey, S. Key, G. Vogelsang, I. Szalayova, G.D. Lange, B. Crain, Transplanted bone marrow generates new neurons in human brains, Proc. Natl. Acad. Sci. Estados Unidos 100(2003) 1364-1369; Sánchez-Ramos et al. (2000); D. Woodbury, E.J. Schwarz, D.J. Prockop, I.B. Black, Adult rat and human bone marrow stromal cells differentiate into neurons, J. Neurosci. Res. 61(2000) 364-370). Recientemente, se ha indicado que las CMMO de hombre y ratón expresan el marcador progenitor neuronal (nestina), la proteína nuclear específica neuronal (NeuN) y la proteína ácida fibrilar glial (GFAP) después de la estimulación con ácido retinoico y factor de crecimiento epidérmico (EGF) o factor neurotrófico derivado del cerebro (BDNF) (Sánchez-Ramos et al. (2000)). También se ha demostrado que las CMMO que se trasplantan son capaces de diferenciar entre linajes neuronales y gliales en el SNC dañado (J.R. Sánchez-Ramos. Neural cells derived from adult bone marrow and umbilical cord blood. J. Neurosci Res. 69(2002) 880-893). Además, se ha descubierto en Chopp et al. que el trasplante de CMMO puede mejorar la recuperación funcional en ratas con isquemia cerebral focal (J. Chen, Y. Li, M. Chopp. Intracerebral transplantation of bone marrow with BDNF after MCAo in rat. Neuropharmacology. 39(2000) 711-716) y en ratas con daño cerebral traumático (D. Lu, Y. Li, L. Wang, J. Chen, A. Mahmood, M. Chopp). La administración intraarterial de células estromales de la médula en un modelo de un daño cerebral traumático de rata. J Neurotrauma. 18(2001) 813-819)) y en ratones con la enfermedad de Parkinson (Y. Li, J. Chen, L. Wang, L. Zhang, M. Lu, M. Chopp). El trasplante intracerebral de células estromales de la médula ósea en un modelo 1-metil-4-fenil-1,2,3,6-tetrahidropiridina de la enfermedad de Parkinson de ratón. Neurosci Lett. 316 (2001) 67-70). Estos hallazgos indican la función potencial como una fuente de células útiles de la terapia celular para el SNC en humanos.
Sin embargo, el aislamiento de CMMO mediante la adherencia a una placa petri de cultivo genera sobre todo poblaciones heterogéneas (AJ Friedenstein, J.E. Gorskaja, N.N. Kulagina. Fibroblast precursors in normal and irradiated mouse hematopoietic organs. Exp Hematol. 4 (1976) 267-274). Por lo tanto, se han desarrollado varios métodos basándose en sus diferentes tamaños y marcadores de superficie específicos para generar poblaciones homogéneas usando la clasificación celular (SC Hung, NJ Chen, S.L. Hsieh, H. Li, H.L. Ma, W. H. Lo, Isolation and characterization of size-sieved stem cells from human bone marrow, Stem Cells. 20 (2002) 249-258; R. Zohar, J. Sodek, CA McCulloch, Characterizaction of stromal progenitor cells enriched by flow cytometry, Blood. 90 (1997) 3471-3481). Por consiguiente, Hung et al. (2002) han desarrollado recientemente un aislamiento eficaz de poblaciones homogéneas de médula ósea humana sobre la base del tamaño celular y la capacidad de adherencia mediante el uso de una separación en gradiente de Percoll y un tamiz poroso de 3 µm para disponer de las células más pequeñas. La población de CMMO que se generó se ha denominado como células seleccionadas por tamaño (SSC) y tienen una capacidad de renovación mejor que las poblaciones heterogéneas de CMMO (Hung et al. (2002)). Las SSC carecen de marcadores de superficie de las células madre hematopoyéticas tempranas, CD34 y AC 133, en el paso 2 a 3 y no expresan marcadores para las CMM osteogénicas y los precursores osteogénicos maduros (Hung et al. (2002)). Sin embargo, estas células expresan Thy-1, receptores de matriz (CD44 y CD105) e integrinas (CD29 y CD51). Las SSC son multipotenciales y pueden aumentar los linajes osteogénicos, adipogénicos y condrogénicos bajo la influencia de señalización ambiental (Hung et al. (2002)). También se ha descubierto que las SSC generan células neurales eléctricamente con la estimulación de agentes antioxidantes tales como el ß-mercaptoetanol y el ácido retinoico, que se usan a menudo in vitro para inducir la diferenciación neural de células madre (S.C Hung, H. Cheng, C.Y. Pan, M.J. Tsai, L.S. Kao, H.L. Ma, In vitro differenciation of size-sieved stem cells into electrically active neural cells, Stem Cells. 20 (2002) 522-529). Aunque el ß-mercaptoetanol y el ácido retinoico tienen un efecto potente en la diferenciación de las SSC en neuronas funcionales, queda por definir la función de los dos factores en la reparación del tejido del SNC.
Sin embargo, la estimulación de las SSC para generar células neurales con agentes antioxidantes tales como ß-mercaptoetanol y el ácido retinoico sólo se pueden aplicar in vitro. El ß-mercaptoetanol es un reactivo tóxico. Además, el ácido retinoico es un cancerígeno. Ambos agentes antioxidantes causan daño a un animal y el trasplante de las células neurales estimuladas conduce a la muerte del receptor.
Sumario de la invención
La invención proporciona células madre seleccionadas por tamaño que derivan de la médula ósea humana que se han tratado con a) un factor neurotrófico que comprende un factor neurotrófico derivado de líneas celulares gliales (GDNF) o b) un factor neurotrófico que comprende un polipéptido activador de adenilato ciclasa de la pituitaria (PACAP) para su uso en el tratamiento de enfermedades neurológicas. La invención también proporciona el uso de células como se define anteriormente en la preparación de un medicamento para el tratamiento de trastornos neurológicos. También se describe en este documento un método nuevo para la transformación morfológica de las SSC desde formas de tipo fibroblástico a formas que tienen prolongaciones con factores neurotróficos lo que es seguro y eficaz en la estimulación de cambios de la morfología celular neural. Además, las células neuronales que se obtienen de acuerdo con el método son adecuadas para la reparación de defectos neurales en animales.
También se describe en este documento un método para inducir la diferenciación neural que comprende el tratamiento de una célula madre de médula ósea con un factor neurotrófico y/o dibutiril AMPc (AMPcdb), en el que el factor neurotrófico comprende un factor neurotrófico derivado de líneas celulares gliales (GDNF) o un polipéptido activador de la adenilato ciclasa de la pituitaria (PACAP).
Breve descripción de los dibujos
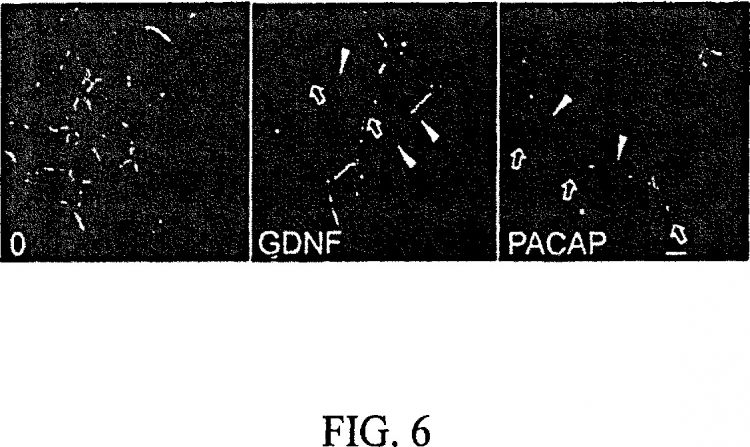
La Fig. 1 ilustra imágenes de contraste de fase de transformación de tipo neuronal de las SSC. Esto indica que las SSC se vuelven células portadoras de proceso en medio ITS solo (0) y en medio ITS con 50 ng/ml de GDNF o 20 ng/ml de PACAP (ampliación = 200 X).
La Fig. 2 ilustra imágenes de contraste de fases de transformación de tipo neuronal de las SSC mediante GDNF, PACAP y AMPcdb. Esto indica que la morfología de las SSC en medio que contiene suero es de tipo fibroblástico y se convierten en unas formas que tienen prolongaciones en medio de retirada de suero (medio ITS solo; 0). Además, las prolongaciones de las SSC tratadas durante 7 días en medio ITS con GDNF (50 ng/ml), PACAP (20 ng/ml), AMPcdb (0,1 mM), GDNF (50 ng/ml) + PACAP (20 ng/ml) o GDNF (50 ng/ml) + AMPcdb (0,1 mM) son alargadas y altamente...
Reivindicaciones:
1. Las células madre seleccionadas por tamaño derivadas de la médula ósea humana que han sido tratadas con
para su uso en el tratamiento de enfermedades neurológicas.
2. Células para su uso de acuerdo con la reivindicación 1, en la que las células madre seleccionadas por tamaño derivadas de médula ósea humana se seleccionan con un tamiz poroso de 3 µm.
3. Células para uso de acuerdo con la reivindicación 1 ó 2, en las que el factor neurotrófico comprende un factor neurotrófico derivado de líneas celulares gliales.
4. Células para su uso de acuerdo con la reivindicación 3, en las que la dosis del factor neurotrófico derivado de líneas celulares gliales es de 20 ng/ml a 50 ng/ml.
5. Células para su uso de acuerdo con la reivindicación 1 ó 2, en las que el factor neurotrófico comprende un polipéptido activador de la adenilato ciclasa de la pituitaria.
6. Células para su uso de acuerdo con la reivindicación 5, en las que la dosis de polipéptido activador de la adenilato ciclasa de la pituitaria es de 10 ng/ml a 20 ng/ml.
7. Células para su uso de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en las que el factor neurotrófico induce la diferenciación neural de las células madre seleccionadas por tamaño derivadas de la médula ósea humana.
8. Células para su uso de acuerdo con la reivindicación 7, en las que la diferenciación neural comprende el aumento de la proteína de neurofilamentos ligeros (NF-L), el aumento de la a-tubulina, la producción de la proteína de la vesícula sinapsina 1, la producción del marcador progenitor neuronal internexina, la elongación de prolongaciones celulares y el aumento de la ramificación de las prolongaciones.
9. Uso de células como se define en una cualquiera de las reivindicaciones 1 a 8 en la preparación de un medicamento para tratar trastornos neurológicos.
Patentes similares o relacionadas:
COMPOSICIÓN QUE COMPRENDE GDNF Y TGF-BETA1 Y SU USO PARA EL TRATAMIENTO DE UNA ENFERMEDAD NEUROLÓGICA, del 22 de Febrero de 2012, de UNIVERSIDAD DE SEVILLA: Composición que comprende GDNG y TGF-{be}1 y su uso para el tratamiento de enfermedad neurológica.Composición farmacéutica que comprende el factor neurotrófico […]
COMPOSICION DE IMPLANTE PARA REGENERACION DE TEJIDO NEURAL, METODO DEOBTENCION Y USOS DE LA MISMA, del 10 de Febrero de 2012, de FINA BIOTECH, S.L.U: Composición de implante para la regeneración de tejido neural, procedimiento de preparación y usos de la misma.En la presente invención se contempla una composición de implante […]
VECTOR VIRICO PARA SU USO EN TERAPIA GENICA IN VIVO DE LA ENFERMEDAD DE PARKINSON, del 6 de Julio de 2010, de NSGENE A/S: Un vector vírico de expresión que comprende una secuencia de polinucleótido que comprende una secuencia promotora capaz de dirigir la expresión […]
 METODO PARA PREVENIR Y TRATAR LA DIABETES CON NEURTURINA, del 27 de Noviembre de 2009, de DEVELOGEN AKTIENGESELLSCHAFT: Uso de un producto de neurturina para estimular y/o inducir la diferenciación entre células productoras de insulina y células progenitoras, […]
METODO PARA PREVENIR Y TRATAR LA DIABETES CON NEURTURINA, del 27 de Noviembre de 2009, de DEVELOGEN AKTIENGESELLSCHAFT: Uso de un producto de neurturina para estimular y/o inducir la diferenciación entre células productoras de insulina y células progenitoras, […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones que comprenden cócteles de fagos antibacterianos y usos de las mismas para el tratamiento de infecciones bacterianas, del 24 de Junio de 2020, de Tecnifar-Indústria Técnica Farmacêutica, S.A: Una composicion que comprende: una primera y una segunda cepa purificada de bacteriofago, cada una de dichas cepas que tiene un genoma que comprende […]
Trampas de GDF, del 3 de Junio de 2020, de ACCELERON PHARMA, INC: Un polipéptido aislado que comprende la secuencia de aminoácidos de SEQ ID NO: 28.