SOLVATOS DE FLUVASTATINA SODICA Y SU UTILIZACION COMO INTERMEDIOS EN LA OBTENCION DE FLUVASTATINA SODICA AMORFA.
Solvatos de fluvastatina sódica y su utilización como intermedios en la obtención de fluvastatina sódica amorfa.
La presente invención proporciona solvatos de fluvastatina sódica estables y de fácil manipulación y procesos para su obtención. En otro aspecto, también se describen procedimientos sencillos para la eliminación de los disolventes de solvatación. La invención se refiere además a un proceso para obtener y preparar fluvastatina sódica amorfa a partir de un solvato de fluvastatina sódica. Estos solvatos son de fácil manipulación y permiten la purificación de la fluvastatina sódica por cristalización e incluso se pueden recristalizar para mejorar la calidad del producto final, además permiten la eliminación del disolvente de solvatación de manera sencilla, constituyendo unos perfectos intermedios para la obtención de fluvastatina sódica amorfa u otra forma de fluvastatina sódica
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702002.
Solicitante: ERCROS INDUSTRIAL, S.A..
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: ASENSIO DOMINGUEZ,RAMON, CRUZADO RODRIGUEZ,M. CARMEN, MAS,GEMMA, LLOVERAS,MAIA, BORRELL,JOSE I, TEIXIDO I CLOSA,JORDI.
Fecha de Solicitud: 18 de Julio de 2007.
Fecha de Publicación: .
Fecha de Concesión: 24 de Febrero de 2010.
Clasificación Internacional de Patentes:
- A61K31/4045 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Indol-alquilaminas; Sus amidas, p. ej. serotonina, melatonina.
- C07D209/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 209/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros, condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › con un radical alquilo o cicloalquilo unido al átomo de nitrógeno del ciclo.
Clasificación PCT:
- A61K31/4045 A61K 31/00 […] › Indol-alquilaminas; Sus amidas, p. ej. serotonina, melatonina.
- A61P3/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Antihiperlipidémicos.
- C07D209/24 C07D 209/00 […] › con un radical alquilo o cicloalquilo unido al átomo de nitrógeno del ciclo.
Fragmento de la descripción:
Solvatos de fluvastatina sódica y su utilización como intermedios en la obtención de fluvastatina sódica amorfa.
Campo de la invención
La presente invención proporciona solvatos de fluvastatina sódica estables y de fácil manipulación y procesos para su obtención. En otro aspecto, también se describen procedimientos sencillos para la eliminación de los disolventes de solvatación.
La invención se refiere además a un proceso para obtener y preparar fluvastatina sódica amorfa a partir de un solvato de fluvastatina sódica.
Antecedentes de la invención
La fluvastatina pertenece al grupo de las estatinas. La fluvastatina, cuyo nombre químico completo es ácido R*,S*-(E)-(±)-7-[3-(4-fluorofenil)-1-(1-metiletil)-1H-indol-2-il]-3,5-dihidroxi-6-heptenoico, así como su sal sódica, se describen en la EP-A-0114 027. La fluvastatina es un inhibidor de la 3-hidroxi-3-metilglutaril-coenzima A (HMG-CoA) reductasa, que es un enzima clave en la regulación de la biosíntesis del colesterol. La fluvastatina puede usarse farmacéuticamente, en particular como un agente hipercolesterolémico, hiperlipoproteinémico y antiaterosclerótico.
La estructura de la fluvastatina sódica se presenta a continuación:
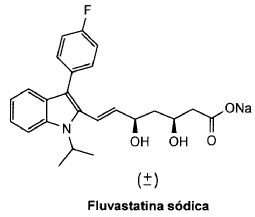
La patente EP0114027 y su equivalente US5354772 describen la obtención de fluvastatina sódica por liofilización de un crudo de reacción. Sin embargo, no se lleva a cabo ninguna cristalización del producto final ni ningún otro tipo de purificación. La patente posterior EP0907639B1 describe que el producto obtenido por liofilización es una mezcla de fluvastatina sódica amorfa y de Forma A, siendo esta última altamente higroscópica.
Hasta este momento se han descrito numerosas formas polimórficas de la fluvastatina sódica, sin embargo muchas de estas formas son hidratos o presentan una alta higroscopicidad, hecho que dificulta su manipulación. Sólo la Forma B descrita en la patente EP0907639B1 podría representar una alternativa.
El estricto control y las especificaciones que deben cumplir hoy en día los fármacos en el mercado ponen de manifiesto la necesidad de disponer de métodos de purificación que aseguren la calidad del producto final. Sin embargo, la fluvastatina sódica amorfa no resulta ni fácil de manipular ni de purificar debido a su difícil precipitación y posterior filtración, por lo que sigue existiendo la necesidad de disponer de unos intermedios manipulables que permitan la purificación de la fluvastatina y su transformación a la forma amorfa.
Como resultado de la presente invención, hemos encontrado que ciertos solvatos de fluvastatina sódica son estables, no higroscópicos y de fácil manipulación y filtración. Dichos solvatos permiten la purificación por cristalización. En otro aspecto de la invención, estos solvatos de fluvastatina sódica permiten la fácil eliminación del disolvente de solvatación, por lo que a partir de ellos se puede obtener, de una forma sencilla, fluvastatina sódica amorfa u otra forma de fluvastatina sódica.
Descripción de las figuras
Fig. 1: Difractograma RX del solvato de diisopropil éter de fluvastatina sódica
Fig. 2: Espectro IR del solvato de diisopropil éter de fluvastatina sódica.
Fig. 3: DSC del solvato de diisopropil éter de fluvastatina sódica.
Fig. 4: TGA del solvato de diisopropil éter de fluvastatina sódica.
Fig. 5: Difractograma RX del solvato de EtOH/ACN de fluvastatina sódica.
Fig. 6: Espectro IR del solvato de EtOH/ACN de fluvastatina sódica.
Fig. 7: DSC del solvato de EtOH/ACN de fluvastatina sódica.
Fig. 8. TGA del solvato de EtOH/ACN de fluvastatina sódica.
Fig. 9: Difractograma RX del solvato de EtOH/ACN/tBuOH de fluvastatina sódica.
Fig. 10: Espectro IR del solvato de EtOH/ACN/tBuOH de fluvastatina sódica.
Fig. 11: DSC del solvato de EtOH/ACN/tBuOH de fluvastatina sódica.
Fig. 12: TGA del solvato de EtOH/ACN/tBuOH de fluvastatina sódica.
Fig. 13. Difractograma de RX del solvato de ACN de fluvastatina sódica.
Fig. 14: Espectro IR del solvato de ACN de fluvastatina sódica.
Fig. 15: DSC del solvato de ACN de fluvastatina sódica.
Fig. 16: TGA del solvato de ACN de fluvastatina sódica.
Fig. 17: Difractograma RX del solvato de 1,4-dioxano de fluvastatina sódica.
Fig. 18: Espectro IR del solvato de 1,4-dioxano de fluvastatina sódica.
Fig. 19: DSC del solvato de 1,4-dioxano de fluvastatina sódica.
Fig. 20: TGA del solvato de 1,4-dioxano de fluvastatina sódica.
Fig. 21: Difractograma RX del solvato de IPA de fluvastatina sódica.
Fig. 22: Espectro IR del solvato de IPA de fluvastatina sódica.
Fig. 23: DSC del solvato de IPA de fluvastatina sódica.
Fig. 24: TGA del solvato de IPA de fluvastatina sódica.
Fig. 25: Difractograma RX del solvato de acetona de fluvastatina sódica.
Fig. 26: Espectro IR del solvato de acetona de fluvastatina sódica.
Fig. 27: DSC del solvato de acetona de fluvastatina sódica.
Fig. 28: TGA del solvato de acetona de fluvastatina sódica.
Fig. 29: Difractograma RX de fluvastatina sódica amorfa.
Fig. 30: Espectro de IR de fluvastatina sódica amorfa.
Fig. 31: DSC de fluvastatina sódica amorfa.
Fig. 32: TGA de fluvastatina sódica amorfa.
Descripción detallada de la invención
La presente invención tiene como objetivo presentar solvatos de fluvastatina sódica y los métodos para su obtención. Estos solvatos son de fácil manipulación y permiten la purificación de la fluvastatina sódica por cristalización e incluso se pueden recristalizar para mejorar la calidad del producto final. Además estos solvatos permiten la eliminación del disolvente de solvatación de una manera sencilla, por lo que constituyen unos perfectos intermedios para la obtención de fluvastatina sódica amorfa u otra forma de fluvastatina sódica. Concretamente, la eliminación del disolvente de solvatación se puede llevar a cabo por secado a presión reducida o mediante liofilización o atomización de una disolución del solvato de fluvastatina sódica, o bien, sorprendentemente, mediante lavado con una mezcla de ACN/H2O del solvato en forma sólida.
Un aspecto de la presente invención consiste en proporcionar métodos para la obtención de estos solvatos. Concretamente, el solvato puede obtenerse por cristalización a partir de una disolución de fluvastatina sódica, a partir de un éster de fluvastatina de cadena corta por reacción con NaOH y posterior cristalización o bien por lavado con una mezcla de disolvente orgánico/H2O de un solvato en forma sólida.
La cristalización de un solvato de fluvastatina sódica puede llevarse a cabo a partir de una disolución de fluvastatina sódica en un disolvente de tipo éter o alcohol, preferentemente THF, MeOH o EtOH. La cristalización del solvato se puede inducir por adición de uno o más insolubilizantes (preferentemente ACN y/o diisopropil éter).
Otro procedimiento para obtener solvatos implica la reacción de un éster de fluvastatina de cadena corta con NaOH en uno o más disolventes de tipo éter o alcohol, preferentemente EtOH, MeOH o THF. Una vez finalizada la reacción se induce la cristalización del solvato por adición de uno o más insolubilizantes (preferentemente ACN y/o diisopropil éter).
Por último también se obtienen solvatos de fluvastatina sódica, preferentemente de 1,4-dioxano, isopropanol o acetona, a partir de otro solvato de fluvastatina sódica (preferentemente un solvato de EtOH/ACN, EtOH/ACN/tBuOH o ACN) por lavado con una mezcla de disolvente orgánico/H2O, concretamente 1,4-dioxano, isopropanol o acetona/H2O respectivamente. De manera preferente, la proporción de la mezcla de lavado disolvente orgánico/H2O está entre 90:10 y 100:0.
La presente invención también describe siete nuevos solvatos de fluvastatina sódica.
Solvato de diisopropil éter de fluvastatina sódica
El solvato de diisopropil éter de fluvastatina sódica presenta...
Reivindicaciones:
1. Solvatos de fluvastatina sódica caracterizados porque incluyen disolventes de tipo éter, alcohol, acetonitrilo, acetona o mezclas de ellos.
2. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de diisopropil éter de fluvastatina sódica.
3. Solvato de diisopropil éter de fluvastatina sódica según la reivindicación 2, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
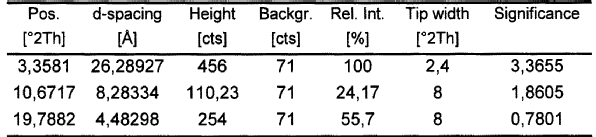
4. Solvato de diisopropil éter de fluvastatina sódica según la reivindicación 2, caracterizado porque su espectro de IR presenta las siguientes bandas:
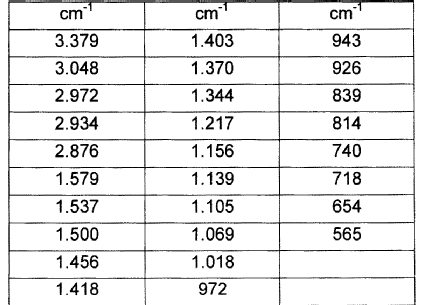
5. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de una mezcla de EtOH y acetonitrilo de fluvastatina sódica.
6. Solvato de EtOH y acetonitrilo de fluvastatina sódica según la reivindicación 5, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
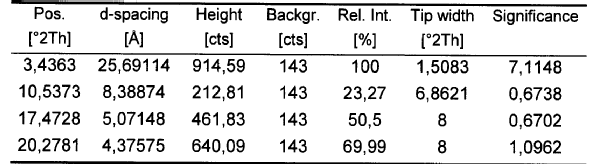
7. Solvato de EtOH y acetonitrilo de fluvastatina sódica según la reivindicación 5, caracterizado porque su espectro de IR presenta las siguientes bandas:
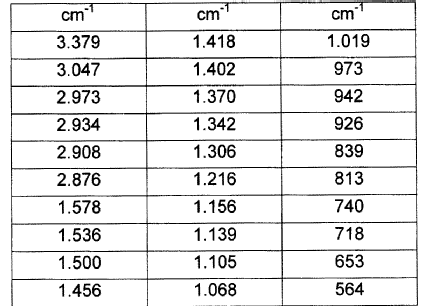
8. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de EtOH, acetonitrilo y tBuOH de fluvastatina sódica.
9. Solvato de EtOH, acetonitrilo y tBuOH de fluvastatina sódica según la reivindicación 8, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
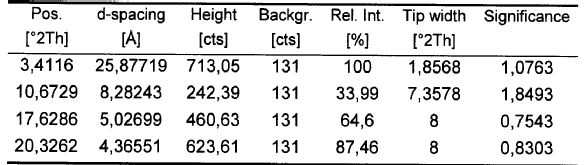
10. Solvato de EtOH, acetonitrilo y tBuOH de fluvastatina sódica según la reivindicación 8, caracterizado porque su espectro de IR presenta las siguientes bandas:
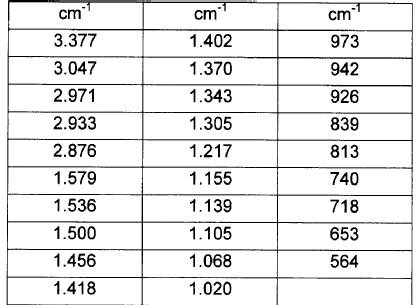
11. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de acetonitrilo de fluvastatina sódica.
12. Solvato de acetonitrilo de fluvastatina sódica según la reivindicación 11, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
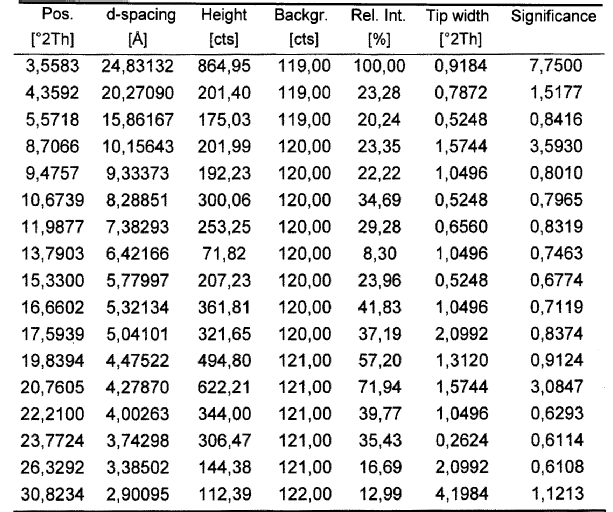
13. Solvato de acetonitrilo de fluvastatina sódica según la reivindicación 11, caracterizado porque su espectro de IR presenta las siguientes bandas:
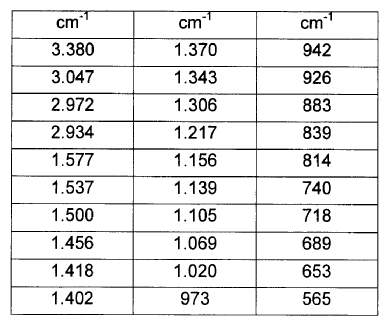
14. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de 1,4-dioxano de fluvastatina sódica.
15. Solvato de 1,4-dioxano de fluvastatina sódica según la reivindicación 14, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
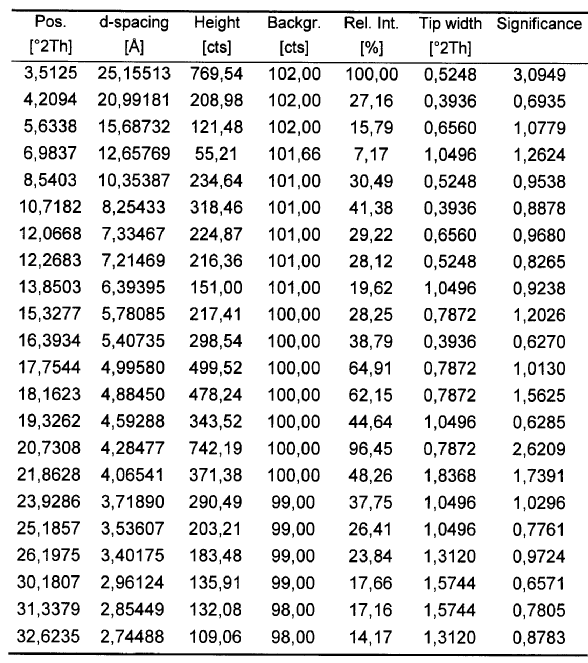
16. Solvato de 1,4-dioxano de fluvastatina sódica según la reivindicación 14, caracterizado porque su espectro de IR presenta las siguientes bandas:
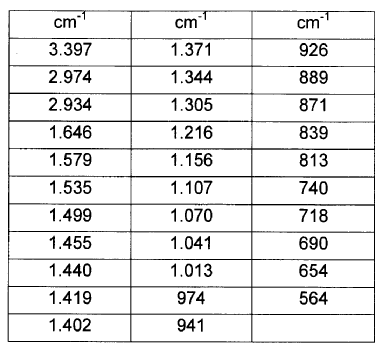
17. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de isopropanol de fluvastatina sódica.
18. Solvato de isopropanol de fluvastatina sódica según la reivindicación 17 caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
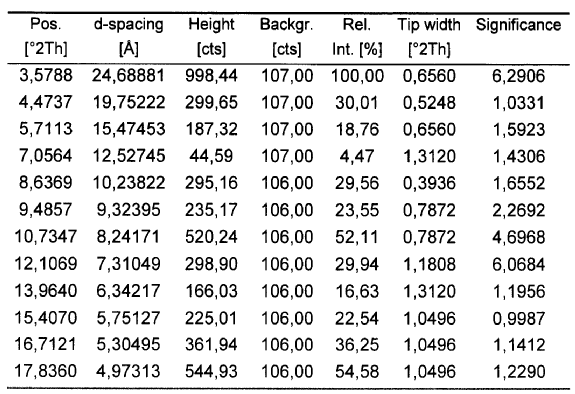
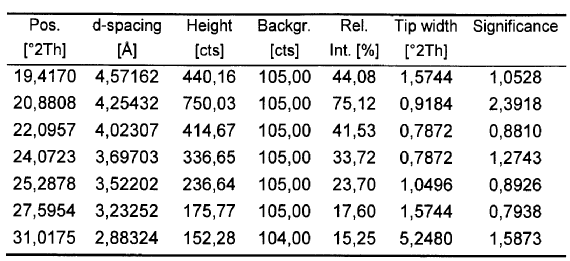
19. Solvato de isopropanol de fluvastatina sódica según la reivindicación 17, caracterizado porque su espectro de IR presenta las siguientes bandas:
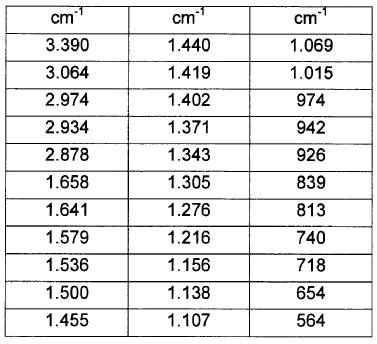
20. Solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque es solvato de acetona de fluvastatina sódica.
21. Solvato de acetona de fluvastatina sódica según la reivindicación 20, caracterizado porque su difractograma de polvo presenta los siguientes picos significativos:
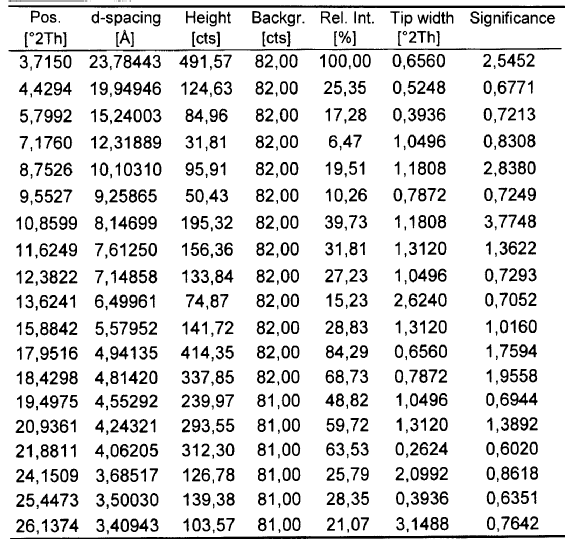
22. Solvato de acetona de fluvastatina sódica según la reivindicación 20, caracterizado porque su espectro de IR presenta las siguientes bandas:
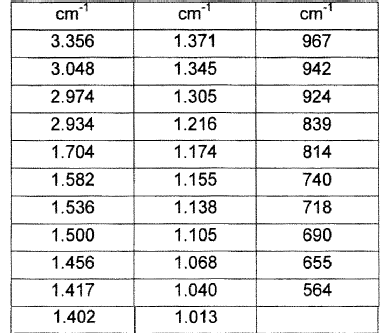
23. Procedimiento para la obtención de un solvato de fluvastatina sódica según la reivindicación 1 caracterizado porque se lleva a cabo a partir de una disolución de fluvastatina sódica y su posterior cristalización.
24. Procedimiento según la reivindicación 23 caracterizado porque la cristalización se lleva a cabo por adición de un insolubilizante.
25. Procedimiento de obtención de un solvato de diisopropil éter de fluvastatina sódica según reivindicación 24, caracterizado porque se realiza a partir de una disolución de fluvastatina sódica en THF por adición de diisopropil éter.
26. Procedimiento de obtención de un solvato de EtOH y acetonitrilo de fluvastatina sódica según reivindicación 24 caracterizado porque se lleva a cabo a partir de una disolución de fluvastatina sódica en EtOH por adición de diisopropil éter y acetonitrilo.
27. Procedimiento de obtención de un solvato de acetonitrilo de fluvastatina sódica según reivindicación 24, caracterizado porque se lleva a cabo a partir de una disolución de fluvastatina sódica en EtOH ó MeOH por adición de diisopropil éter y acetonitrilo.
28. Procedimiento de obtención de un solvato de fluvastatina sódica según la reivindicación 1 caracterizado porque se lleva a cabo a partir de un éster de cadena corta de fluvastatina, por reacción con NaOH y posterior cristalización.
29. Procedimiento según la reivindicación 28 caracterizado porque la cristalización se lleva a cabo por adición de un insolubilizante.
30. Procedimiento de obtención de un solvato de diisopropil éter de fluvastatina sódica según reivindicación 29, caracterizado porque se lleva a cabo a partir de un éster de cadena corta de fluvastatina, por reacción con NaOH en una mezcla de THF/MeOH y posterior cristalización por adición de diisopropil éter.
31. Procedimiento de obtención de un solvato de EtOH, acetonitrilo y tBuOH de fluvastatina sódica según reivindicación 29, caracterizado porque se lleva a cabo a partir de un éster tertbutílico de fluvastatina, por reacción con NaOH en EtOH y posterior cristalización por adición de diisopropil éter y acetonitrilo.
32. Procedimiento de obtención de un solvato de acetonitrilo de fluvastatina sódica según reivindicación 29, caracterizado porque se lleva a cabo a partir de un éster de cadena corta de fluvastatina, por reacción con NaOH en EtOH ó MeOH y posterior cristalización por adición de diisopropil éter y acetonitrilo.
33. Procedimiento de obtención de un solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque se lleva a cabo a partir de otro solvato de fluvastatina sódica por lavado en una mezcla disolvente orgánico/agua.
34. Procedimiento de obtención de un solvato de 1,4-dioxano de fluvastatina sódica según reivindicación 33, caracterizado porque se lleva a cabo por lavado de un solvato de fluvastatina sódica, preferentemente en EtOH/ACN, EtOH/ACN/tBuOH o ACN, con una mezcla 1,4-dioxano/H2O.
35. Procedimiento de obtención de un solvato de isopropanol de fluvastatina sódica según reivindicación 33, caracterizado porque se lleva a cabo por lavado de un solvato de fluvastatina sódica, preferentemente en EtOH/ACN, EtOH/ACN/tBuOH o ACN, con una mezcla isopropanol/H2O.
36. Procedimiento de obtención de un solvato de acetona de fluvastatina sódica según reivindicación 33, caracterizado porque se lleva a cabo por lavado de un solvato de fluvastatina sódica, preferentemente en EtOH/ACN, EtOH/ACN/tBuOH o ACN, con una mezcla acetona/H2O.
37. Procedimiento de obtención de fluvastatina sódica a partir de un solvato de fluvastatina sódica según la reivindicación 1, caracterizado porque se lleva a cabo por eliminación del disolvente de solvatación.
38. Procedimiento según la reivindicación 37 caracterizado porque la eliminación del disolvente de solvatación se lleva a cabo mediante un proceso de secado o bien mediante un proceso de lavado.
39. Procedimiento de obtención de fluvastatina sódica amorfa a partir de un solvato de fluvastatina sódica según reivindicaciones 37 o 38.
40. Procedimiento según la reivindicación 39 caracterizado porque se obtiene fluvastatina sódica amorfa a partir de un solvato de diisopropil éter, EtOH/ACN, EtOH/ACN/tBuOH, acetonitrilo, 1,4-dioxano, isopropanol o acetona.
41. Procedimiento según la reivindicación 39 caracterizado porque la transformación del solvato a fluvastatina sódica amorfa se lleva a cabo mediante cualquier proceso de secado.
42. Procedimiento según reivindicaciones 39 y 41 caracterizado porque la transformación del solvato de fluvastatina sódica a fluvastatina sódica amorfa se lleva a cabo mediante "spray drying" de una disolución del solvato.
43. Procedimiento según reivindicaciones 39 y 41 caracterizado porque la transformación del solvato de fluvastatina sódica a fluvastatina sódica amorfa se lleva a cabo mediante atomización de una disolución del solvato.
44. Procedimiento según reivindicación 38, caracterizado porque el proceso de lavado se lleva a cabo con una mezcla acetonitrilo/H2O.
45. Procedimiento según la reivindicación 44, caracterizado porque se realiza a partir de un solvato de EtOH/ACN, EtOH/ACN/tBuOH ó ACN.
46. Utilización de un solvato de fluvastatina sódica según la reivindicación 1 para la obtención de fluvastatina sódica en cualquiera de sus formas, especialmente en la forma amorfa.
Patentes similares o relacionadas:
Tratamiento de disfunción eréctil y otras indicaciones, del 1 de Julio de 2020, de STRATEGIC SCIENCE & TECHNOLOGIES, LLC: Una composición para su uso en un método de tratamiento de la disfunción sexual en un sujeto, preferiblemente un sujeto humano, comprendiendo la composición: […]
Derivados de amida de aminoácidos N-urea sustituidos como moduladores del receptor análogo al receptor 1 de péptido formilado (FPRL-1), del 1 de Julio de 2020, de ALLERGAN, INC.: Compuesto para usar en el tratamiento de un trastorno asociado con la modulación del receptor análogo al receptor 1 de péptido N-formilado representado por la fórmula […]
Composiciones y métodos no hormonales para la anticoncepción masculina que comprenden (R)-Silodosina, del 1 de Julio de 2020, de Laboratoires Major: Composición para su uso en un método anticonceptivo no hormonal para un sujeto masculino, en la que dicha composición es una formulación de liberación prolongada […]
Compuestos de indol carboxamida útiles como inhibidores de cinasas, del 13 de Mayo de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la fórmula (I): **(Ver fórmula)** o una sal del mismo, en la que: X es CR4; A es: **(Ver fórmula)** o **(Ver fórmula)** Q2 es […]
PARCHES TRANSDÉRMICOS PARA USO EN AURICULOTERAPIA, del 30 de Abril de 2020, de QM HEALTH CARE & NUTRITION, S.L: Parche transdérmico para uso en auriculoterapia que comprende al menos un principio activo seleccionado entre cafeína, chocolate y glutamina para la modulación de neurotransmisores.
Heteroarilamidas como inhibidores de la agregación de proteínas, del 29 de Abril de 2020, de UCB Biopharma SRL: Un compuesto de una Fórmula (I): **(Ver fórmula)** donde: R1 es H, halo, C1-4alquilo, o CF3; R2 es -CF3, o C1-4alquilo no sustituido o […]
Compuestos de 1-tetrahidropiranilcarbonil-2,3-dihidro-1h-indol para el tratamiento del cáncer, del 29 de Abril de 2020, de ELI LILLY AND COMPANY: Un compuesto de fórmula: **(Ver fórmula)** en la que R1a es hidrógeno, metilo, etenilo, ciano, fluoro, cloro, fluorometilo, o difluorometilo; […]
Formas de dosificación de liberación sostenida para un inhibidor de JAK1, del 8 de Abril de 2020, de INCYTE CORPORATION: {1-{1-[3-fluoro-2-(trifluorometil)isonicotinoil]piperidin-4-il}-3-[4-(7H-pirrolo[2,3-d]pirimidin-4-il)-1H-pirazol-1- il]azetidin-3-il}acetonitrilo, o una…