PROCEDIMIENTOS Y COMPOSICIONES PARA EL TRATAMIENTO DE LA DIABETES.
Composición para la terapia de neogénesis de islotes que comprende un ligando de receptor gastrina/colecitoquinina (CCK) en ausencia de un ligando de receptor EGF para utilizar combinadamente de forma simultánea,
separada o secuencial con un agente para la supresión de la respuesta inmunitaria en el tratamiento de un sujeto diabético
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07010865.
Solicitante: WARATAH PHARMACEUTICALS INC.
Nacionalidad solicitante: Canadá.
Dirección: 415, YONGE STREET SUITE 1103,TORONTO, ONTARIO M5B 2E7.
Inventor/es: BRAND, STEPHEN, J., CRUZ,ANTONIO.
Fecha de Publicación: .
Fecha Solicitud PCT: 9 de Junio de 2003.
Fecha Concesión Europea: 14 de Octubre de 2009.
Clasificación Internacional de Patentes:
- A61K31/436 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo el sistema heterocíclico un ciclo de seis eslabones teniendo el oxígeno como heteroátomo del ciclo, p. ej. rapamicina.
- A61K31/522 A61K 31/00 […] › teniendo grupos oxo unidos directamente al heterociclo, p. ej. hipoxantina, guanina, aciclovir.
- A61K31/525 A61K 31/00 […] › Iso-aloxazinas, p. ej. riboflavinas, vitamina B 2.
- A61K31/535 A61K 31/00 […] › que tienen ciclos con seis eslabones con al menos un nitrógeno y al menos un oxígeno como heteroátomos de un ciclo, p. ej. 1,2-oxazinas.
- A61K31/5377 A61K 31/00 […] › no condensadas y conteniendo otros heterociclos, p. ej. timolol.
- A61K31/573 A61K 31/00 […] › sustituidos en posición 21, p. ej. cortisona, dexametasona, prednisona o aldosterona.
- A61K31/663 A61K 31/00 […] › Compuestos que tienen varios grupos deácido del fósforo o sus esteres, p. ej. ácido clodrónico, ácido pamidrónico.
- A61K38/18A
- A61K38/21 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Interferones.
- A61K38/22A
- A61K45/06 A61K […] › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
Clasificación PCT:
- A61K31/436 A61K 31/00 […] › conteniendo el sistema heterocíclico un ciclo de seis eslabones teniendo el oxígeno como heteroátomo del ciclo, p. ej. rapamicina.
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61K38/19 A61K 38/00 […] › Citoquinas; Linfoquinas; Interferones.
- A61K38/22 A61K 38/00 […] › Hormonas (derivados de pro-opiomelanocortina, pro-encefalina o pro-dinorfina A61K 38/33, p. ej. corticotropina A61K 38/35).
- A61K45/06 A61K 45/00 […] › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
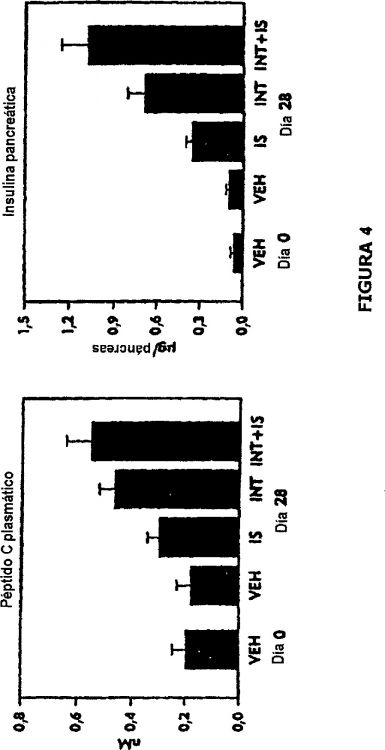
Fragmento de la descripción:
Procedimientos y composiciones para el tratamiento de la diabetes.
Campo de la invención
La presente invención se refiere a procedimientos y composiciones para el tratamiento de sujetos diabéticos con terapia de neogénesis de islotes (I.N.T.TM) y un agente para la inmunosupresión, y con un ligando de receptor gastrina/CCK y un agente para inmunosupresión.
Antecedentes de la invención
Aproximadamente 800.000 personas de la población de los Estados Unidos padecen diabetes por deficiencia de insulina (también conocida como diabetes juvenil o diabetes de tipo I), y cada año surgen aproximadamente 30.000 nuevos casos. Además, en esta población se produce un aumento extremadamente rápido e importante, a un nivel de proporciones epidémicas, del número de pacientes que presentan formas de diabetes de tipo II (también denominada diabetes insulinorresistente o diabetes de aparición adulta) que causan agotamiento pancreático e insuficiencia insulínica.
El nivel anormalmente alto de glucosa en la sangre (hiperglucemia) que caracteriza a la diabetes, si no se trata, da como resultado una variedad de condiciones patológicas, por ejemplo úlceras vasculares periféricas de difícil curación, daños en la retina que conducen a la ceguera y fallo renal. Tanto la diabetes de tipo I como la de tipo II se tratan con la inyección de insulina como respuesta a los niveles de glucosa en la sangre determinados mediante el autocontrol de glucosa efectuado por el propio paciente, aunque no todas las clases de progreso de la diabetes de tipo II requieren terapia insulínica. Normalmente, se suministran al paciente diversas dosis de insulina al día. Las consecuencias patológicas graves de la diabetes están relacionadas con el control poco riguroso del nivel de glucosa en la sangre.
Sumario de las formas de realización
En un aspecto, una forma de realización de la invención consiste en un procedimiento para fabricar un medicamento para su utilización en el tratamiento del sujeto diabético, que comprende la administración al sujeto de una composición para terapia de neogénesis de islotes y un agente para la supresión de una respuesta inmunitaria. El procedimiento utiliza, además, una composición para la terapia de neogénesis de islotes que comprende un ligando de receptor EGF. El procedimiento además utiliza una composición para la terapia de neogénesis de islotes que comprende por lo menos dos agentes para la supresión de una respuesta inmunitaria. La composición del procedimiento para la terapia de neogénesis de islotes comprende un ligando de receptor gastrina/colecistoquinina (CCK). El ligando de receptor EGF es un EGF humano recombinante, por ejemplo, el ligando de receptor EGF es EGF51N. El ligando de receptor gastrina/CCK es gastrina17 humana. En formas de realización relacionadas, el agente para la supresión de la respuesta inmunitaria es un fármaco, por ejemplo, el agente para la supresión de la respuesta inmunitaria es por lo menos uno seleccionado del grupo formado por una rapamicina, un corticosteroide, una azatioprina, mofetil micofenolato; una ciclosporina; una ciclofosfamida; un metotrexato; una 6-mercaptopurina; FK506 (Tacrolimus); 15-deoxispergualina; un FTY 720; una mitoxantrona; un 2-amino-1,3-propanodiol; un hidrocloruro de 2-amino-2[2-(4-octilfenil)etil]propano-1,3-diol; una 6-(3-dimetil-aminopropionil)forscolina; y una demetinmunomicina. La rapamicina es Everolimus o Sirolimus. El corticosteroide es dexametasona. El agente para la supresión de la respuesta inmunitaria es una proteína, por ejemplo una proteína que comprende una secuencia de aminoácido de un anticuerpo. Pueden ser ejemplos de anticuerpos para la supresión de la respuesta inmunitaria por lo menos uno seleccionado de entre el grupo constituido por: hul 124; BTI-322; allotrap-HLA-B270; OKT4A; Enlimomab; ABX-CBL; OKT3; ATGAM; basiliximab; daclizumab; inmunoglobulina antitimocito; ISAtx247; Medi-500; Medi-507; Alefacept; efalizumab; infliximab; en una forma de realización alternativa, la proteína es una citoquina o factor de crecimiento tal como GFAP, S100ß o un interferón.
Según estos procedimientos, la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria se formulan para administración secuencial. Un ejemplo comprende la formulación de la composición para la terapia de neogénesis de islotes y del agente para la supresión de la respuesta inmunitaria para administración secuencial para permitir un período de tiempo de por lo menos un día entre la administración del agente y la administración de la composición. Alternativamente, el período es de por lo menos una semana, o por lo menos de seis semanas entre la administración del agente y la administración de la composición.
En las formas de realización anteriormente descritas, por lo menos uno de los dos productos, la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria, se formula para administración sistémica. Alternativamente, por lo menos uno de los dos productos, la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria, se formula para administración en bolo. Por ejemplo, por lo menos uno de los dos productos, la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria, se formula para administración por una vía del grupo formado por las vías intravenosa, subcutánea, intraperitoneal e intramuscular. En determinadas formas de realización, el agente para la supresión de la respuesta inmunitaria se formula para administración oral. En algunas formas de realización, el agente para la supresión de la respuesta inmunitaria es por lo menos uno seleccionado de entre el grupo de Sirolimus, Tacrolimus, Everolimus, ISAtx247 y daclizumab.
En la mayoría de los casos, el sujeto para el cual se formula la utilización es un diabético mamífero, por ejemplo el sujeto es un humano. Alternativamente, el sujeto puede ser un animal experimental, por ejemplo un ratón NOD.
En otro aspecto, una forma de realización de la invención consiste en un procedimiento para fabricar un medicamento para su utilización en el tratamiento de sujetos diabéticos, que comprende la formulación para el sujeto de una composición para la terapia de neogénesis de islotes formada por lo menos por un ligando de receptor EGF y un ligando de receptor gastrina/CCK, y la administración de por lo menos un agente inmunosupresor. En una forma de realización relacionada, el procedimiento implica otra formulación del ligando de receptor gastrina/CCK y el por lo menos un agente inmunosupresor en ausencia del ligando de receptor EGF. En una forma de realización del procedimiento, antes de la administración posterior del ligando de receptor gastrina/CCK y del por lo menos un agente inmunosupresor en ausencia de ligando de receptor EGF, el procedimiento además comprende un período sin ninguna administración del agente o la composición. Por ejemplo, el sujeto diabético presenta una diabetes de aparición reciente. Además, a continuación del período de no administración, la composición y el agente se formulan para administración secuencial. En determinadas formas de realización, tanto el ligando de receptor EGF como el ligando de receptor gastrina/CCK y el agente inmunosupresor se formulan en dosis efectivas. Además, en algunas formas de realización, la composición o el agente se formulan con un tampón farmacéuticamente aceptable.
Otra forma más de realización de la invención consiste en un procedimiento para fabricar un medicamento para su utilización en el tratamiento de sujetos diabéticos, que comprende la administración al sujeto de una composición para la terapia de neogénesis de islotes formada por lo menos por un EGF51N y gastrina17, y la administración de por lo menos un agente inmunosupresor. El por lo menos un agente inmunosupresor se formula para contener una dosis efectiva tanto de Tacrolimus como de Sirolimus. Alternativamente, el procedimiento además implica la formulación de por lo menos uno de los dos productos EGF51N y gastrina17, y la formulación de una dosis efectiva de por lo menos uno de los productos Tacrolimus, Everolimus, daclizumab, ISAtx247 y Sirolimus. Alternativamente, el procedimiento comprende la formulación para utilización con el sujeto de un ligando de receptor gastrina/CCK y un agente para la supresión de la respuesta inmunitaria. Por ejemplo, el ligando del receptor gastrina/CCK es la gastrina17. El agente para la supresión de la respuesta inmunitaria es un fármaco, por ejemplo, el agente...
Reivindicaciones:
1. Composición para la terapia de neogénesis de islotes que comprende un ligando de receptor gastrina/colecitoqui- nina (CCK) en ausencia de un ligando de receptor EGF para utilizar combinadamente de forma simultánea, separada o secuencial con un agente para la supresión de la respuesta inmunitaria en el tratamiento de un sujeto diabético.
2. Composición según la reivindicación 1, en la que la composición se utiliza con por lo menos dos agentes para la supresión de la respuesta inmunitaria.
3. Composición según la reivindicación 1 ó 2, en la que el ligando de receptor gastrina/CCK es gastrina17 humana.
4. Composición según cualquiera de las reivindicaciones anteriores, en la que el agente para la supresión de una respuesta inmunitaria es por lo menos un agente seleccionado de entre el grupo constituido por una rapamicina; un corticosteroide; una azatioprina; mofetil micofenolato; una ciclosporina; una ciclofosfamida; un metotrexato; una 6-mercaptopurina; FK506 (Tacrolimus); 15-deoxispergualina; un FTY 720; una mitoxantrona; un 2-amino-1,3-propanodiol; un hidrocloruro de 2-amino-2[2-(4-octilfenil)etil]propano-1,3-diol; una 6-(3-dimetil-aminopropionil)forscolina; y una demetinmunomicina.
5. Composición según la reivindicación 1, en la que el agente para la supresión de la respuesta inmunitaria es por lo menos un agente seleccionado de entre el grupo constituido por hul 124; BTI-322; allotrap-HLA-B270; OKT4A; Enlimomab; ABX-CBL; OKT3; ATGAM; basiliximab; daclizumab; inmunoglobulina antitimocito; ISAtx247; Medi-500; Medi-507; Alefacept; efalizumab; infliximab; y un interferón.
6. Composición según cualquiera de las reivindicaciones anteriores, en la que la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria se formulan para administración secuencial.
7. Composición según cualquiera de las reivindicaciones anteriores, en la que la composición y el agente para la supresión de la respuesta inmunitaria se formulan para administración sistémica.
8. Composición según cualquiera de las reivindicaciones 1 a 7, en la que por lo menos la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria se formulan para ser administrados por una vía seleccionada de entre el grupo constituido por las vías intravenosa, subcutánea, intraperitoneal e intramuscular.
9. Composición según cualquiera de las reivindicaciones 1 a 7, en la que por lo menos la composición para la terapia de neogénesis de islotes y el agente para la supresión de la respuesta inmunitaria se formulan para administración oral.
10. Composición según la reivindicación 1, en la que el agente para la supresión de la respuesta inmunitaria se formula para contener por lo menos un agente seleccionado de entre el grupo constituido por Sirolimus, Tacrolimus, Everolimus, ISAtx247 y daclizumab.
11. Composición según cualquiera de las reivindicaciones 1 a 10, en la que la composición o el agente se formulan, además, para comprender un tampón farmacéuticamente aceptable.
12. Composición según cualquiera de las reivindicaciones 1 a 11, en la que la diabetes es una diabetes de aparición reciente.
13. Composición farmacéutica que comprende un agente para la supresión de la respuesta inmunitaria y un ligando de receptor gastrina/CCK en ausencia del ligando de receptor EGF.
14. Composición según la reivindicación 13, en la que el ligando de receptor gastrina/CCK es una gastrina.
15. Composición según la reivindicación 13 ó 14, en la que el ligando de receptor gastrina/CCK es una gastrina17.
16. Composición según la reivindicación 15, en la que la gastrina17 es gastrina17Met15 ó gastrina17Leu15.
17. Composición según cualquiera de las reivindicaciones 13 a 16, en la que el agente para la supresión de la respuesta inmunitaria es por lo menos un agente seleccionado de entre el grupo constituido por una rapamicina; un corticosteroide; una azatioprina; mofetil micofenolato; una ciclosporina; una ciclofosfamida; un metotrexato; una 6-mercaptopurina; FK506 (Tacrolimus); 15-deoxispergualina; un FTY 720; una mitoxantrona; un 2-amino-1,3-propanodiol; un hidrocloruro de 2-amino-2[2-(4-octilfenil)etil]propano-1,3-diol; una 6-(3-dimetil-aminopropionil)forscolina; y una demetinmunomicina.
18. Composición según cualquiera de las reivindicaciones 13 a 16, en la que el agente para la supresión de la respuesta inmunitaria es por lo menos un agente seleccionado de entre el grupo constituido por hul 124; BTI-322; allotrap-HLA-B270; OKT4A; Enlimomab; ABX-CBL; OKT3; ATGAM; basiliximab; daclizumab; inmunoglobulina antitimocito; ISAtx247; Medi-500; Medi-507; Alefacept; efalizumab; infliximab; y un interferón.
19. Utilización de una composición para la terapia de neogénesis de islotes que comprende un ligando de receptor gastrina/colecitoquinina (CCK) en ausencia de un ligando de receptor EGF para la fabricación de un medicamento destinado a su utilización de forma simultánea, separada o secuencial en combinación con un agente para la supresión de la respuesta inmunitaria en el tratamiento de un paciente diabético.
Patentes similares o relacionadas:
COMPOSICIÓN FARMACÉUTICA SINÉRGICA DE ACECLOFENACO Y BETAMETASONA PARA EL TRATAMIENTO DEL DOLOR DE AFECCIONES REUMÁTICAS O DOLOR POSTQUIRÚRGICO, del 16 de Julio de 2020, de AMEZCUA AMEZCUA, Federico: La presente invención está relacionada con una composición farmacéutica compuesta por la combinación sinérgica de un analgésico antiinflamatorio no esteroideo como […]
Composiciones tópicas que comprenden un corticosteroide y un retinoide para tratar la psoriasis, del 1 de Julio de 2020, de Bausch Health Ireland Limited: Una composición farmacéutica tópica para usar en el tratamiento de la psoriasis, la composición que comprende: (a) propionato de halobetasol […]
Emulsión de aceite en agua de monetasona y propilenglicol, del 24 de Junio de 2020, de Galenica AB: Un método para preparar una emulsión de aceite en agua que comprende furoato de mometasona, comprendiendo el método a) preparar una fase oleosa mezclando […]
Métodos de tratamiento de afecciones oculares con un implante de administración sostenida de medicamento, del 17 de Junio de 2020, de ALLERGAN, INC.: Implante bioerosionable para su uso en un método para tratar edema macular diabético (EMD), comprendiendo el método inyectar dicho implante bioerosionable en el vítreo de un […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
17alfa-benzoato de cortexolona para su uso en el tratamiento de tumores, del 3 de Junio de 2020, de COSMO TECHNOLOGIES LTD: Un compuesto que tiene la fórmula: **(Ver fórmula)** para su uso como medicamento.
COMPOSICIÓN TÓPICA ESTABLE, del 22 de Mayo de 2020, de PRODUCTOS MAVER, S.A. DE C.V: La presente invención corresponde a una composición farmacéutica tópica estable que comprende betametasona o sus sales farmacéuticamente aceptables, indometacina […]
Composición farmacéutica tópica a base de alcanos semifluorados, del 13 de Mayo de 2020, de NOVALIQ GMBH: Una composición farmacéutica tópica para usar en la prevención o el tratamiento de una enfermedad o afección que afecta la piel o un apéndice de la piel, que comprende […]