PEPTIDOS INHIBIDORES DE LA EXOCITOSIS NEURONAL.
Péptidos inhibidores de la exocitosis neuronal.
Péptidos de fórmula general (I):
R{sub,1} AA R{sub,2}
(I)
capaces de regular la exocitosis neuronal, sus estereoisómeros y mezclas de los mismos, racémicas o no, y las sales cosméticamente o farmacéuticamente aceptables de los mismos, en donde AA es una secuencia de 3 a 40 aminoácidos adyacentes contenida en la secuencia de aminoácidos de la proteína SNAP 25, R{sub,1} se selecciona del grupo formado por H o grupo alquilo, arilo, aralquilo o acilo; y R{sub,2} se selecciona del grupo formado por amino, hidroxilo o tiol, sustituidos o no con grupos alifáticos o cíclicos, con la condición de que cuando R{sub,1} es H o acetilo, R{sub,2} no es amino, hidroxilo ni tiol no sustituidos. Un método de obtención, composiciones cosméticas o farmacéuticas que los contienen y su uso para tratar aquellas condiciones que requieran la regulación de la exocitosis neuronal, preferentemente para tratar la piel
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200602720.
Solicitante: LIPOTEC, S.A..
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: FERRER MONTIEL, ANTONIO, PONSATI OBIOLS, BERTA, ALMIANA DOMENECH,NURIA, CARREO SERRAIMA,CRISTINA, CEBRIAN PUCHE,JOAN, FERNANDEZ CARNEADO,JIMENA, VAN DEN NEST,WIM.
Fecha de Solicitud: 25 de Octubre de 2006.
Fecha de Publicación: .
Fecha de Concesión: 8 de Abril de 2010.
Clasificación Internacional de Patentes:
- C07K14/705 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
Clasificación PCT:
- A61K8/64 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 8/00 Cosméticos o preparaciones similares para el aseo. › Proteínas; Péptidos; Sus derivados o sus productos de degradación.
- A61Q19/08 A61 […] › A61Q USO ESPECIFICO DE COSMETICOS O DE PREPARACIONES SIMILARES PARA EL ASEO. › A61Q 19/00 Preparaciones para el cuidado de la piel. › Preparaciones antienvejecimiento.
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
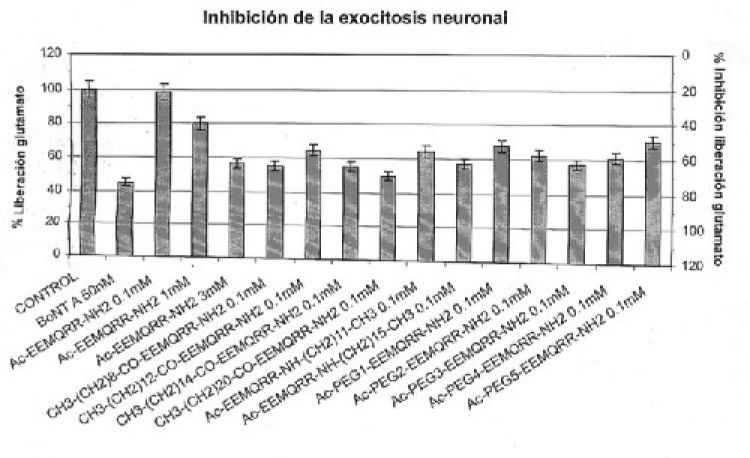
Fragmento de la descripción:
Péptidos inhibidores de la exocitosis neuronal.
Campo de la invención
La presente invención se refiere a péptidos capaces de regular la exocitosis neuronal y a composiciones cosméticas o farmacéuticas que contienen dichos péptidos de utilidad en el tratamiento de aquellas condiciones que requieran una regulación de la exocitosis neuronal, como por ejemplo la espasticidad de los músculos, la asimetría facial y/o las arrugas faciales, preferentemente las arrugas de expresión.
Antecedentes de la invención
Uno de los signos más visibles del envejecimiento del ser humano son los cambios que experimenta la piel: sequedad, aparición de manchas, flaccidez y arrugas. Estos efectos pueden ser causados por agentes externos como la exposición constante al sol, la contaminación atmosférica o el contacto con agentes químicos presentes en, por ejemplo, productos de limpieza, pero también son consecuencia de cambios fisiológicos, bioquímicos e histológicos intrínsecos del organismo humano, debidos a la disminución de la síntesis de proteínas como el colágeno o la elastina, a un aumento de la proteólisis, y a una rotura general de la barrera de la piel, del tejido conectivo y de la cohesión.
Se han descrito distintos principios activos para la prevención o disminución de los síntomas del envejecimiento, como por ejemplo retinoides, hidroxiácidos, flavonoides o derivados de vitamina C y E. Dichos compuestos actúan normalmente mejorando la hidratación de la piel, aumentando la renovación celular o previniendo la degeneración de los tejidos que forman la piel; sin embargo, su eficacia en la prevención o tratamiento de las arrugas faciales motivadas por la contracción de los músculos es limitada. La base o mecanismo de formación de las arrugas faciales de expresión es una tensión de los músculos de la epidermis que arrastran la piel hacia el interior. Esta tensión muscular es el resultado de una hiperactividad de los nervios que enervan los músculos faciales. La hiperactividad nerviosa se caracteriza por una liberación incontrolada y excesiva de neurotransmisores que excitan las fibras musculares. Por ello, las moléculas que regulen la exocitosis neuronal contribuyen a relajar la tensión muscular y, consecuentemente, a eliminar las arrugas faciales.
Existe, pues, la necesidad de desarrollar nuevos principios activos con eficacia probada para la preparación de una composición cosmética o farmacéutica para regular la exocitosis neuronal y, por tanto, para tratar la espasticidad de los músculos y reducir y/o eliminar la asimetría facial y/o las arrugas faciales, especialmente las arrugas de expresión.
Se entiende por arrugas de expresión aquellas que son consecuencia del estrés que ejercen las contracciones de los músculos faciales responsables de producir las expresiones del rostro sobre la piel del rostro. Las arrugas de expresión se suelen localizar en la frente, en el espacio entre las cejas, alrededor de la boca y/o alrededor de los ojos. Dependiendo de la forma del rostro, la frecuencia de las expresiones y la existencia de tics (movimientos convulsivos, que se repiten con frecuencia, producidos por la contracción involuntaria de uno o varios músculos, en este caso del rostro) las arrugas de expresión pueden aparecer incluso en la adolescencia. Los factores externos como la exposición al sol acentúan su profundidad y su visibilidad.
Con el objetivo de reducir y/o eliminar las arrugas de expresión se han empleado ampliamente las toxinas botulínicas, en especial el serotipo A (BOTOX® Cosmetic, Allergan Inc.) [Carruthers J.D. y Carruthers J.A. (1992) "Treatment of glabellar frown lines with C. botulinum -A exotoxin" J. Dermatol. Surg. Oncol. 18, 17-21; Mendez-Eastman S.K. (2003) "Botox: a review" Plast. Surg. Nurs. 23, 64-69]. El tratamiento terapéutico y cosmético con BOTOX® consiste en la inyección localizada de preparados farmacéuticos (complejo botulina A-hematoglutinina, 500 kDa) diluidos en las zonas donde se localiza la tensión muscular. Los efectos paralíticos de la toxina son reversibles con una duración media de 6 meses [Jankovic J. y Brin F.M. (1991) "Therapeutic uses of botulinum toxin" New Engl. J. Med. 324, 1186-1194; Jankovic J. (1994) "Botulinum toxin in movement disorders" Curr. Opin. Neurol. 6, 358-366]. El tratamiento, por tanto, requiere la inyección repetida de toxina botulínica. El problema principal de este tratamiento es la posibilidad de que se desencadene una reacción inmune contra el preparado farmacéutico debido a que por su tamaño molecular puede ser objeto de reconocimiento por el sistema inmunitario del paciente. La aparición de anticuerpos contra la toxina botulínica constituye un grave problema ya que contribuye a una clara pérdida de eficacia del tratamiento [Jankovic J. y Brin F.M. (1991) "Therapeutic uses of botulinum toxin" New Engl. J. Med. 324, 1186-1194; Jankovic J. (1994) "Botulinum toxin in movement disorders" Curr. Opin. Neurol. 6, 358-366; Jankovic J. y Brin M.F. (1997) "Botulinum toxin: historical perspective and potential new indications" Muscle Nerve Suppl. 6, S129-S145; Davis L.E. (1993) "Botulinum toxin-from poison to medicine" West J. Med. 128, 25-28; Hughes A.J. (1994) "Botulinum toxin in clinical practise" Drugs 48, 888-893; Hambleton P. (1992) "Clostridium botulinum toxins a general review of involvement in disease, structure, mode of action and preparation for clinical use" J. Neurol. 239, 16-20; Borodic G.E. y Pearces L.B. (1994) "New concepts in botulinum toxin therapy" Drug Safety 11, 145-152; Brin M.F., Blitzer A., Stewart C., Pine Z., Borg-Stein J., Miller J., Nagalapura N.S. y Rosenfeld D.B. (1993) "Disorders with excesive muscle contraction: Candidates for treatment with intramuscular botulinum toxin (BoTox®)" Botulinum and Tetanus Neurotoxins (Ed. B.R. DasGupata), 559-576]. Esta pérdida de eficacia del tratamiento con BOTOX® conlleva la necesidad de aumentar la concentración del preparado en tratamientos posteriores, lo que a su vez produce una potenciación de la respuesta inmune. Como alternativa al tratamiento con toxina botulínica del serotipo A se ha barajado el uso de serotipos distintos de las toxinas botulínicas, tales como BoTox B, BoTox F y BoTox E. No obstante, la aplicación de preparados farmacéuticos con serotipos distintos no puede considerarse una solución al problema puesto que, tarde o temprano, la reacción inmune se puede volver a producir. Además, el tratamiento con toxinas botulínicas es caro debido, principalmente, a la labilidad e inestabilidad de las preparaciones farmacéuticas que las contienen.
Existe, por tanto, una necesidad imperiosa de desarrollar moléculas que imiten los efectos paralíticos de las toxinas botulínicas pero que estén dotadas de estructuras moleculares mucho más sencillas y estables, que no induzcan reacciones inmunes, y cuyo coste de producción sea económico. Las moléculas de naturaleza peptídica cumplen estas propiedades.
A nivel molecular, las toxinas botulínicas son proteasas que degradan proteínas neuronales que están involucradas en el mecanismo de exocitosis activada por el ión calcio [Schiavo G., Rossetto O. y Montecucco C. (1996) "Bases Moleculares del tétanos y del botulismo" Investigación y Ciencia 234, 46-55; Montecucco C. y Schiavo G. (1994) "Mechanism of action of tetanus and botulinum neurotoxins" Mol. Microbiol. 13, 1-8; Schiavo G., Rosetto O., Benfenati F., Poulain B. y Montecucco, C. (1994) "Tetanus and botulinum neurotoxins are zinc proteases specific for components of the neuroexocytosis apparatus" Ann. NY Acad. Sci. 710, 65-75]. Por ejemplo, la toxina botulínica A, la más comúnmente utilizada en clínica y cosmética por sus aplicaciones en la eliminación de las arrugas faciales y de la asimetría facial, y para suavizar la sintomatología de enfermedades espasmódicas, trunca la proteína neuronal SNAP-25. Esta proteína SNAP-25 juega un papel clave en la neurosecreción puesto que está involucrada en la formación de un complejo proteico (conocido con el nombre de complejo SNARE o de fusión) que dirige y controla la liberación de la acetilcolina acumulada en vesículas. El núcleo de dicho complejo de fusión lo constituyen las proteínas SNAP-25 y sintaxina, localizadas en la membrana plasmática presináptica, y la proteína sinaptobrevina o VAMP, localizada en la membrana plasmática vesicular [Calakos N. y Scheller R.H. (1996) "Synaptic vesicle biogenesis, docking and fusion: a molecular description" PhysioL Rev. 76, 1-29; Sutton R.B., Fasshauer D., Jahn R. y Brunger A.T. (1998) "Crystal structure of a SNARE complex involved in synaptic exocytosis at 2.4Å resolution" Nature 395, 347-353]. La función principal...
Reivindicaciones:
1. Un péptido de fórmula general (I)
sus estereoisómeros, mezclas de los mismos, y sus sales cosméticamente y farmacéuticamente aceptables, caracterizado porque
con la condición de que cuando R1 es H o acetilo, R2 no es amino, hidroxilo o tiol no sustituidos.
2. Péptido según la reivindicación 1 caracterizado porque R1 es acilo de C3 a C24, lineal, ramificado o cíclico, saturado o insaturado.
3. Péptido según la reivindicación 2 caracterizado porque R1 es acilo de fórmula CH3-(CH2)m-CO-, donde m puede variar entre 1 y 22.
4. Péptido según la reivindicación 1 caracterizado porque R1 es un polímero de polietilenglicol.
5. Péptido según la reivindicación 4 caracterizado porque dicho polímero de polietilenglicol tiene un peso molecular comprendido entre 200 y 35.000 daltons.
6. Péptido según la reivindicación 5 caracterizado porque dicho polímero de polietilenglicol es
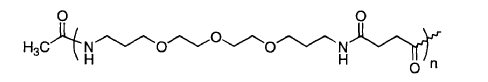
donde n puede variar entre 1 y 100.
7. Péptido según la reivindicación 6 caracterizado porque n varía entre 1 y 5.
8. Péptido según la reivindicación 1 caracterizado porque R2 es amino o hidroxilo, sustituidos o no con grupos alifáticos de C1 a C24 lineales, ramificados o cíclicos, saturados o insaturados.
9. Péptido según la reivindicación 1 caracterizado porque AA es una secuencia de aminoácidos adyacentes contenida en una secuencia seleccionada del grupo formado por MAEDADMRNELEEMQRRADQL, ADESLES TRRMLQLVEESKDAGI, ELEEMQRRADQLA, ELEEMQRRADQL, ELEEMQRRADQ, ELEEMQRRAD, ELEEMQRRA, ELEEMQRR, LEEMQRRADQL, LEEMQRRADQ, LEEMQRRAD, LEEMQRRA, LEEMQRR, EEMQRRADQL, EEMQRRADQ, EEMQRRAD, EEMQRRA, EEMQRR, LESTRRMLQLVEE, NKDMKEAEKN LT, KNLTDL, IMEKADSNKTRIDEANQRATKMLGSG, SNKTRIDEANQRATKMLGSG, TRIDEANQRATKMLG SG, DEANQRATKMLGSG, NQRATKMLGSG y QRATKMLGSG.
10. Procedimiento de obtención de un péptido de fórmula general (I), según cualquiera de las reivindicaciones 1 a 9, caracterizado porque se realiza en fase sólida.
11. Procedimiento de obtención de un péptido de fórmula general (I), según la reivindicación 10, caracterizado porque emplea grupos protectores seleccionados del grupo formado por Fmoc/tButilo, Fmoc/tritilo y Fmoc/alilo.
12. Composición cosmética o farmacéutica que comprende una cantidad cosmética o farmacéuticamente eficaz de al menos un péptido de fórmula general (I) según cualquiera de las reivindicaciones 1 a 9 caracterizada porque comprende al menos un excipiente o adyuvante cosmética o farmacéuticamente aceptable.
13. Composición cosmética o farmacéutica según la reivindicación 12, caracterizada porque el péptido de fórmula general (I) se encuentra incorporado a un vehículo o a un sistema de liberación sostenida cosmética o farmacéuticamente aceptable seleccionado del grupo formado por liposomas, milicápsulas, microcápsulas, nanocápsulas, esponjas, vesículas, micelas, miliesf eras, microesferas, nanoesferas, lipoesferas, microemulsiones, nanoemulsiones, milipartículas, micropartículas y nanopartículas.
14. Composición cosmética o farmacéutica según la reivindicación 12, caracterizada porque el péptido de fórmula general (I) se encuentra adsorbido sobre un polímero orgánico o soporte sólido mineral cosméticamente o farmacéuticamente aceptable seleccionado del grupo formado por talco, bentonita, sílice, almidón o maltodextrina.
15. Composición cosmética o farmacéutica según cualquiera de las reivindicaciones 12 a 14, caracterizada porque presenta una formulación seleccionada del grupo formado por cremas, emulsiones de aceite y/o silicona en agua, emulsiones de agua en aceite y/o silicona, aceites, leches, bálsamos, espumas, lociones, geles, linimentos, sueros, jabones, ungüentos, mousses, pomadas, barras, lápices y vaporizadores.
16. Composición cosmética o farmacéutica, según cualquiera de las reivindicaciones 12 a 14, caracterizada porque el péptido de fórmula general (I) se encuentra incorporado en soportes sólidos seleccionados del grupo formado por toallitas, hidrogeles, parches adhesivos, parches no adhesivos y mascarillas faciales.
17. Composición cosmética o farmacéutica, según cualquiera de las reivindicaciones 12 a 14, caracterizada porque el péptido de fórmula general (I) se encuentra incorporado en productos de línea de maquillaje seleccionados del grupo formado por correctores de ojeras, fondos de maquillaje, lociones desmaquillantes, leches desmaquillantes, sombras de ojos y barras de labios.
18. Composición cosmética o farmacéutica, según cualquiera de las reivindicaciones 12 a 14, caracterizada porque el péptido de fórmula general (I) se encuentra incorporado en tejidos.
19. Composición cosmética o farmacéutica, según la reivindicación 18, caracterizada porque el péptido de fórmula general (I) se encuentra incorporado en vendas.
20. Composición cosmética o farmacéutica que comprende una cantidad cosmética o farmacéuticamente eficaz de al menos un péptido de fórmula general (I), según cualquiera de las reivindicaciones 1 a 9, caracterizada porque el péptido de fórmula general (I) se encuentra a una concentración entre el 0.00000001% y el 20% en peso.
21. Composición cosmética o farmacéutica, según la reivindicación 20, caracterizada porque el péptido de fórmula general (I) se encuentra a una concentración entre el 0.0001% y el 5% en peso.
22. Composición cosmética o farmacéutica que comprende una cantidad cosmética o farmacéuticamente eficaz de al menos un péptido de fórmula general (I), según cualquiera de las reivindicaciones 1 a 9, caracterizada porque comprende una cantidad adicional cosmética o farmacéuticamente eficaz de un agente activo seleccionado del grupo formado por un agente exfoliante, un agente hidratante, un agente despigmentante o blanqueante, un agente propigmentante, un agente anti-estrías, un agente antiarrugas, un agente antioxidante, un agente antiglicación, un inhibidor de la NO-sintasa, un agente anti-envejecimiento, un agente capaz de reducir o eliminar las bolsas bajo los ojos, un agente estimulador de la síntesis de moléculas dérmicas o epidérmicas y/o para prevenir su degradación, un agente estimulador de la proliferación de fibroblastos y/o queratinocitos o para estimular la diferenciación de queratinocitos, agente destinados a mejorar la unión dermis-epidermis, un agente dermorelajante, un agente reafirmante, un agente anti-contaminación atmosférica y/o anti-radicales libres, un agente que actúe sobre la circulación capilar y/o la microcirculación, un agente calmante, un agente antiinflamatorio, un agente antimicrobiano, un agente antifúngico, un agente que actúe sobre el metabolismo de las células, un agente que actúe sobre la circulación capilar y/o la microcirculación, vitaminas, un agente quelante, un agente fotoprotector, de naturaleza orgánica o mineral, activo contra los rayos ultravioleta A y/o B, o mezclas de ellos.
23. Composición cosmética o farmacéutica, según la reivindicación 22, caracterizada porque el agente activo es de origen sintético o un extracto vegetal o proviene de biofermentación.
24. Composición cosmética o farmacéutica, según la reivindicación 22, caracterizada porque el agente antiarrugas y/o antienvejecimiento se selecciona del grupo formado por Argireline®, Leuphasyl®, Decorinyl®, Decorinol®, Lipochroman® y Aldenine®.
25. Uso de un péptido de fórmula general (I), según cualquiera de las reivindicaciones 1 a 9, en la elaboración de una composición cosmética o farmacéutica para el tratamiento de aquellas condiciones de los mamíferos que requieran la regulación de la exocitosis neuronal.
26. Uso de un péptido de fórmula general (I), según cualquiera de las reivindicaciones 1 a 9, en la elaboración de una composición cosmética o farmacéutica para el tratamiento, limpieza o cuidado de la piel.
27. Uso del péptido de fórmula general (I) según cualquiera de las reivindicaciones 1 a 9 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina las arrugas faciales y/o la asimetría facial.
28. Uso del péptido de fórmula general (I) según la reivindicación 27 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina las arrugas faciales de expresión.
29. Uso del péptido de fórmula general (I) según reivindicación 28 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina las arrugas faciales de expresión mediante aplicación en la frente, en el espacio entre las cejas y/o en las arrugas y líneas finas alrededor de la boca y/o alrededor de los ojos.
30. Uso del péptido de fórmula general (I) según la reivindicación 28 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina las arrugas faciales de expresión mediante aplicación por iontoforesis en la frente, en el espacio entre las cejas y/o en las arrugas y líneas finas alrededor de la boca y/o alrededor de los ojos.
31. Uso del péptido de fórmula general (I) según reivindicación 28 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina las arrugas faciales de expresión mediante aplicación por inyección subcutánea o intradérmica en la frente, en el espacio entre las cejas y/o en las arrugas y líneas finas alrededor de la boca y/o alrededor de los ojos.
32. Uso del péptido de fórmula general (I) según cualquiera de las reivindicaciones 1 a 9 en la elaboración de una composición cosmética o farmacéutica que reduce y/o elimina la espasticidad muscular.
Patentes similares o relacionadas:
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Procedimientos de tratamiento del cáncer usando antagonistas de unión al eje de PD-1 e inhibidores de TIGIT, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo antagonista anti-PD-L1 o fragmento de unión a antígeno del mismo y un anticuerpo antagonista anti-TIGIT o fragmento de unión a antígeno del mismo para su uso […]
Uso de CAR basados en ICOS para mejorar la actividad antitumoral y la persistencia del CAR, del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una secuencia de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde el CAR comprende un dominio de unión a antígeno, un dominio transmembrana […]
Péptido derivado de GPC3, composición farmacéutica para el tratamiento o la prevención de cáncer usando el mismo, inductor de inmunidad y método para producir células presentadoras de antígeno, del 17 de Junio de 2020, de CYTLIMIC INC: Composición farmacéutica para su uso en el tratamiento o la prevención de cáncer, que comprende un péptido que consiste en una secuencia de aminoácidos […]
Péptidos inhibidores derivados del transcrito de tipo TREM-1 (TLT-1) y sus usos, del 10 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido de 6 a 16 aminoácidos que comprende al menos 6 aminoácidos consecutivos de la secuencia de aminoácidos sec. con núm. de ident.: 4 para su uso en el tratamiento […]
Fijación eficaz como objetivo de la leucemia humana primaria utilizando células T modificadas con receptor de antígeno quimérico anti-CD123, del 3 de Junio de 2020, de NOVARTIS AG: Una molécula de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde dicho CAR comprende un dominio de unión anti-CD123 humanizado, […]
Dominios coestimuladores para su uso en células genéticamente modificadas, del 3 de Junio de 2020, de Precision Biosciences, Inc: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica un dominio coestimulador que comprende una secuencia de aminoácidos establecida […]
Método para proporcionar linfocitos T específicos de tumor, del 27 de Mayo de 2020, de HS Diagnomics GmbH: Un método para fabricar un receptor artificial de linfocitos T específicos de tumor, que comprende las etapas de: - proporcionar una preparación de linfocitos […]