METODO PARA LA LIBERACION CUANTITATIVA DE PROTEINAS, POLIPEPTIDOS O PEPTIDOS NATURALES O RECOMBINANTES.
Un método para la liberación cuantitativa de inmunoligandos termoestables,
capaces de unirse a la parte Fc de inmunoglobulinas, de complejos en diversas matrices de muestra, caracterizado por mezclar la muestra con un compuesto reactivo que es capaz de adsorber o unirse inespecíficamente a inmunoglobulinas y que tiene extremos hidrófobos así como negativamente cargados, y someter más tarde la muestra a una operación de tratamiento térmico seguida de una operación de enfriamiento, en el que se añaden un tampón y proteína antes de la operación de calentamiento con objeto de compensar las variaciones de la muestra en cuanto al pH y al contenido de proteína, respectivamente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/SE99/00828.
Solicitante: AMERSHAM PHARMACIA BIOTECH AB.
Nacionalidad solicitante: Suecia.
Dirección: BJIRKGATAN 30,751 84 UPPSALA.
Inventor/es: STEINDL, FRANZ.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- G01N33/563 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que interviene fragmentos de anticuerpos.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación PCT:
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
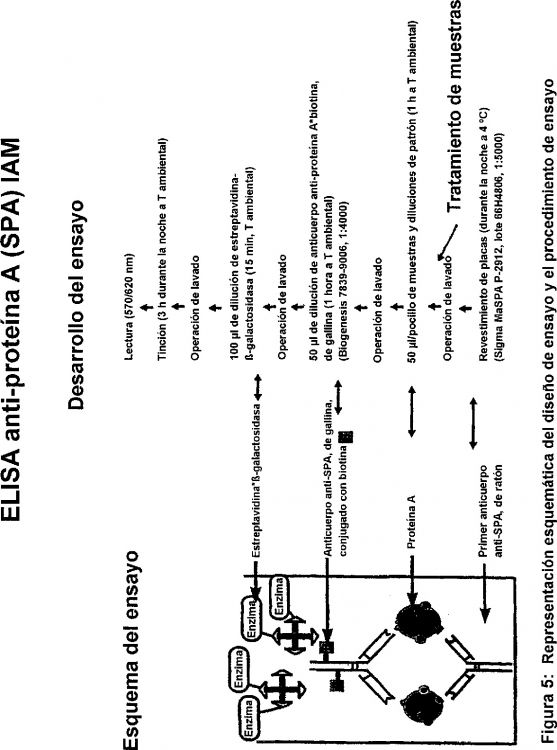
Fragmento de la descripción:
Método para la liberación cuantitativa de proteínas, polipétidos o péptidos naturales o recombinantes.
El presente invento se refiere a un método para la liberación cuantitativa de inmunoligandos termoestables, capaces de unirse a la parte Fc de inmunoglobulinas (anticuerpos; en particular de la clase IgG y que esencialmente llegan a unirse fuera del paratopo), de complejos en diversas matrices de muestra con objeto de hacer que estas proteínas, polipéptidos o péptidos naturales o recombinantes liberados estén cuantitativamente disponibles en ensayos inmunoquímicos y permanezcan cuantitativamente disponibles. El método de liberación está esencialmente destinado a ser utilizado como una operación previa en el inmunoensayo de la clase de proteínas, polipéptidos y péptidos recién mencionada cuando existen como contaminantes en diferentes preparaciones de inmunoglobulinas/anticuerpos o como preparaciones más o menos puras.
En el contexto de la presente solicitud, la expresión "de origen bacteriano" se refiere a un polipéptido o proteína que procede de un polipéptido o proteína que es producido naturalmente por bacterias u otros microorganismos. "Recombinante" designa una proteína, un polipéptido o un fragmento ligante de anticuerpo más corto, expresado en cualquier tipo de células por medio de ingeniería genética. "Péptido sintético" significa que la parte de una proteína o polipéptido que contiene la región funcional es producida por medio de síntesis peptídica química.
Las proteínas presentes en la naturaleza que son capaces de unirse a la parte Fc de inmunoglobulinas (Ig) esencialmente de clase G (IgG) de la mayoría de los mamíferos son principalmente de origen bacteriano. La fuerza de unión difiere de acuerdo con la especie y la subclase. Esta propiedad fue descrita por vez primera en relación con la proteína A de Staphylococcus aureus (SPA; del inglés, Staphylococcal protein A) en 1966 (A. Forsgren y J. Sjöquist, J. Immunol. 17: 822-27, 1966) y, algo más tarde, en relación con la proteína G de Streptococcus pneumoniae (SPG; del inglés, Streptococcal protein G) en 1973 (G. Kronvall, J. Immunol. 111: 1401-06, 1973). Estas proteínas se unen a anticuerpos en la región entre los dominios constantes 2 y 3 (CH2 y CH3) de las cadenas pesadas. Se sabe que las proteínas A y G son capaces de unirse además a la región variable de las cadenas pesadas de IgA, IgE, IgG e IgM, Igs que pertenecen a la familia VH3 (M. Inganäs et al., Scand. J. Immunol. 14: 379-88, 1981, y M. Erntell et al., Scand. J. Immunol. 17: 201-09, 1983). Aminoácidos de tres secciones de la región variable de las cadenas pesadas de los anticuerpos (FR1, CDR2 y FR3) están implicados en esta así llamada "reactividad alternativa" [K. N. Potter et al., J. Immunol. 157 (7): 2982-88, 1996, y K. N. Potter et al., Int. Rev. Immunol. 14 (4): 291-308, 1997]. Las proteínas A y G se unen a anticuerpos en el mismo sitio o, al menos, en sitios íntimamente solapantes [M. Eliasson et al., J. Immunol. 142 (2): 575-81, 1989]. La proteína A tiene 5 (A-E) subunidades ligantes de IgG [T. Moks et al., Eur. J. Biochem. 153 (3): 537-43, 1986]. La "reactividad alternativa" puede ser una función de todos los dominios individuales; sin embargo, ha sido satisfactoriamente examinada para dos fragmentos (dominios), para el dominio B (M. Inganäs et al., Scand. J. Immunol. 12: 23-31, 1980; M. Inganäs et al., Scand. J. Immunol. 13: 343-352, 1981; M. Inganäs et al., Scand. J. Immunol. 14: 379-388, 1981) y para el dominio D [P. W. Roben et al., J. Immunol. 154 (12): 6437-45, 1995].
Aparte de las proteínas A y G, se conocen otras proteínas ligantes de anticuerpo que, no obstante, tienen diferentes especificidades y regiones ligantes, tales como, por ejemplo, la proteína H [P. Akesson et al., Mol. Immunol. 27 (6): 523-31, 1990] y la clusterina [M. R. Wilson et al., Biochim. Biophys. Acta 1159 (3): 319-326, 1992]. Las proteínas, polipéptidos y péptidos ligantes de IgG anteriormente mencionados (que se unen fuera del paratopo) son relativamente resistentes al tratamiento térmico (en disolución), y, por lo tanto, en el presente documento, se hará referencia a ellos como inmunoligandos termoestables.
Estas proteínas (particularmente la proteína A) se utilizan en una diversidad de aplicaciones y se emplean a gran escala, principalmente en la purificación de anticuerpos monoclonales y policlonales. Tanto las formas nativas como las recombinantes se utilizan como ligandos en cromatografía de inmunoafinidad. Esta tecnología refinada proporciona una purificación muy eficaz de anticuerpos a partir de disoluciones de complejos. Los anticuerpos son normalmente unidos en un pH moderado a una matriz cromatográfica que lleva como ligando una de estas proteínas ligantes de inmunoglobulinas, y son desorbidos en un ambiente ácido (pH = 2,7-3,5 ó 2,7-3,2). Sin embargo, bajo estas condiciones, ha sido imposible hasta ahora evitar un cierto grado de pérdida de ligandos.
Esto es de fundamental importancia para las preparaciones de anticuerpos utilizadas para aplicaciones clínicas. Se supone que la proteína A (lo mismo se aplica a la proteína G) tiene una elevada actividad biológica, y en muchas publicaciones se describen efectos tóxicos en modelos animales y en seres humanos [W. I. Bensinger et al., J. Biol. Response Mod. 3 (3): 347-51, 1984; G. L. Messerschmidt et al., J. Biol. Response Mod. 3 (3): 325-29, 1984; D. S. Terman et al., Eur. J. Cancer Clin. Oncol., 21 (10): 1115-22, Octubre de 1985; G. J. Ventura et al., Cancer Treat. Rep. 71 (4): 411-13, Abril de 1987]. También se piensa que la proteína A, junto con las enterotoxinas A y B, desempeña un papel en la patogenicidad de las infecciones por Staphylococcus aureus. A causa de su "reactividad alternativa", también puede causar estimulación mitogénica de células B de la familia VH3. Por lo tanto, es esencial que estos ligandos puedan ser identificados sensible, específica y, sobre todo, correctamente en las preparaciones de inmunoglobulinas.
Muchas publicaciones y artículos de revisión tratan de los posibles modos de utilizar polipéptidos capaces de unirse a la parte Fc de los anticuerpos, y de sus posibles peligros cuando están presentes como contaminantes en productos para aplicaciones clínicas (por ejemplo, J. J. Langone et al., J. Adv. Immunol. 17: 157-252, 1982).
Hasta ahora, se han empleado ensayos inmunoquímicos, tales como el ensayo de inmunoabsorción con enzimas ligadas (ELISA; del inglés, enzyme-linked immunosorbent assay) y el radioinmunoensayo (RIA), en diferentes variaciones para detectar y cuantificar proteínas y/o polipéptidos ligantes de Ig.
Un problema con este tipo de ensayos es que una proteína (analito) ligante de Fc (IgG) formará complejos con la parte Fc de anticuerpos/inmunoglobulina G con diferentes afinidades dependiendo de la especie, la subclase de la IgG e, incluso, el anticuerpo. Esto ha sido previamente resuelto al utilizar fragmentos de anticuerpo (Fab, Fab'2) o anticuerpos específicos de gallina (que no se unen a las proteínas A o G por la parte Fc) para la detección (por ejemplo, J. J. Langone et al., J. Immunol. Meth. 63: 145-57, 1982).
Para liberar las proteínas y polipéptidos ligantes de Fc (IgG) de la parte Fc de la IgG con objeto de identificarlos en presencia de IgG, las muestras han sido convencionalmente ensayadas en un ambiente ácido (pH = 3,2 ó 3,5, respectivamente) (A. Berglund y M. Inganäs, Patente de EE.UU. nº 4.752.571, 1988; S. Knicker et al., J. Immunol. Meth. 142: 53-59, 1991). Este método es útil, por ejemplo, para determinar proteína A en muestras que contienen IgG de ratón (diversas subclases) en una concentración de hasta 250 µg de IgG/ml.
Este método previamente conocido tiene las limitaciones siguientes:
Reivindicaciones:
1. Un método para la liberación cuantitativa de inmunoligandos termoestables, capaces de unirse a la parte Fc de inmunoglobulinas, de complejos en diversas matrices de muestra, caracterizado por mezclar la muestra con un compuesto reactivo que es capaz de adsorber o unirse inespecíficamente a inmunoglobulinas y que tiene extremos hidrófobos así como negativamente cargados, y someter más tarde la muestra a una operación de tratamiento térmico seguida de una operación de enfriamiento, en el que se añaden un tampón y proteína antes de la operación de calentamiento con objeto de compensar las variaciones de la muestra en cuanto al pH y al contenido de proteína, respectivamente.
2. Un método de acuerdo con la Reivindicación 1, caracterizado por que se añade un agente quelante antes de la operación de calentamiento para que se una a los iones metálicos pesados que pueden estar presentes.
3. Un método de acuerdo con una de las Reivindicaciones 1 y 2, caracterizado por que el compuesto reactivo es dodecilsulfato sódico (SDS).
4. Un método de acuerdo con una de las Reivindicaciones 1 a 3, caracterizado por que la concentración del compuesto reactivo en la muestra antes de la operación de calentamiento está en el intervalo de 10 a 40 mM, preferiblemente de 30 a 40 mM.
5. Un método de acuerdo con una de las Reivindicaciones 1 a 4, caracterizado por que la operación de calentamiento se aplica durante un periodo de tiempo en el intervalo de 3 a 180 minutos y a una temperatura en el intervalo de 60 a 100ºC.
6. Un método de acuerdo con una de las Reivindicaciones 1 a 5, caracterizado por que, en la operación de enfriamiento después de la operación de calentamiento, se deja que la temperatura baje hasta una temperatura en el intervalo de 0 a 40ºC, preferiblemente de 4 a 35ºC.
7. Un método de acuerdo con una de las Reivindicaciones 1 a 6, caracterizado por que, durante la operación de calentamiento, el pH está en el intervalo de 5 a 8, preferiblemente de 6 a 7,5.
8. Un método de acuerdo con una de las Reivindicaciones 1 a 7, caracterizado por que se añaden tampones de fosfato o borato a la muestra antes de la operación de calentamiento.
9. Un método de acuerdo con una de las Reivindicaciones 1 a 8, caracterizado por que la concentración del tampón en la muestra antes de la operación de calentamiento es seleccionada del intervalo de 5 a 100 mM.
10. Un método de acuerdo con una de las Reivindicaciones 1 a 9, caracterizado por que la concentración de las proteínas añadidas en la muestra antes de la operación de calentamiento es seleccionada del intervalo de 1/20 a 1/100 de la concentración del compuesto reactivo añadido, es decir, de 0,1 a 2 mM, preferiblemente de 0,3 a 2 mM.
11. Un método de acuerdo con una de las Reivindicaciones 2 a 10, caracterizado por que el agente quelante está presente en la muestra, antes de la operación de calentamiento, en una concentración en el intervalo de 0,5 a 5 mM.
Patentes similares o relacionadas:
Inmunomoduladores, del 29 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la fórmula (I) **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de **(Ver fórmula)** en donde: […]
Métodos y composiciones para el diagnóstico y pronóstico de lesión renal e insuficiencia renal, del 29 de Julio de 2020, de Astute Medical, Inc: Un método para evaluar el estado renal en un sujeto, que comprende: realizar una pluralidad de ensayos configurados para detectar una […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Método para llevar a cabo el seguimiento de la enfermedad de Gaucher, del 15 de Julio de 2020, de Centogene GmbH: Un método para determinar la evolución de la enfermedad de Gaucher en un sujeto, que comprende la etapa de determinar en varios puntos en el […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
Biomarcadores de pronóstico y predictivos y aplicaciones biológicas de los mismos, del 1 de Julio de 2020, de INSTITUT GUSTAVE ROUSSY: Un método para evaluar la sensibilidad o la resistencia de un tumor frente a un agente antitumoral, que comprende evaluar la cantidad de complejo eiF4E-eiF4G (complejo Cap-ON) […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]