METODO PARA DETECTAR FOSFOLIPIDO PROCOAGULANTE.
Un método para determinar la cantidad de fosfolípido procoagulante en una muestra humana,
comprendiendo dicho método las etapas (i) a (iii) realizadas en el siguiente orden:
(i) formar una mezcla de la muestra humana y un plasma de sustrato no humano que se ha liberado o liberado sustancialmente de suficiente fosfolípido procoagulante para al menos reducir la capacidad del plasma de sustrato para coagular, en la que dicho plasma de sustrato se ha liberado o liberado sustancialmente de fosfolípido procoagulante por tratamiento con una fosfolipasa;
(ii) poner en contacto la mezcla con factor Xa en condiciones en las que el fosfolípido procoagulante es el componente limitante de velocidad de la mezcla; y
(iii) determinar el tiempo de coagulación de la mezcla
Tipo: Resumen de patente/invención. Número de Solicitud: W04001291AU.
Solicitante: HAEMATEX RESEARCH PTY LIMITED.
Nacionalidad solicitante: Australia.
Dirección: UNIT 9, 17 KING ROAD,HORNSBY, NSW 2077.
Inventor/es: EXNER, THOMAS.
Fecha de Publicación: .
Fecha Concesión Europea: 4 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- G01N33/86 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que interviene el tiempo de coagulación de la sangre.
- H03L7/22 ELECTRICIDAD. › H03 CIRCUITOS ELECTRONICOS BASICOS. › H03L CONTROL AUTOMATICO, ARRANQUE, SINCRONIZACION O ESTABILIZACION DE GENERADORES DE OSCILACIONES O DE IMPULSOS ELECTRONICOS (de generadores dinamoeléctricos H02P). › H03L 7/00 Control automático de frecuencia o fase; Sincronización (sintonización de circuitos resonantes en general H03J; sincronización en los sistemas de comunicación digital, ver los grupos apropiados en la clase H04). › utilizando más de un bucle.
Clasificación PCT:
- C12P1/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › Preparación de compuestos o de composiciones, no prevista en los grupos C12P 3/00 - C12P 39/00, utilizando microorganismos o enzimas; Procedimientos generales de preparación de compuestos o composiciones que utilizan microorganismos o enzimas.
- C12Q1/34 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una hidrolasa.
- C12Q1/56 C12Q 1/00 […] › en los que intervienen factores de coagulación de la sangre, p. ej. trombina, tromboplastina, fibrinógeno.
- G01N33/86 G01N 33/00 […] › en los que interviene el tiempo de coagulación de la sangre.
Clasificación antigua:
- C12P1/00 C12P […] › Preparación de compuestos o de composiciones, no prevista en los grupos C12P 3/00 - C12P 39/00, utilizando microorganismos o enzimas; Procedimientos generales de preparación de compuestos o composiciones que utilizan microorganismos o enzimas.
- C12Q1/34 C12Q 1/00 […] › en los que interviene una hidrolasa.
- C12Q1/56 C12Q 1/00 […] › en los que intervienen factores de coagulación de la sangre, p. ej. trombina, tromboplastina, fibrinógeno.
- G01N33/86 G01N 33/00 […] › en los que interviene el tiempo de coagulación de la sangre.
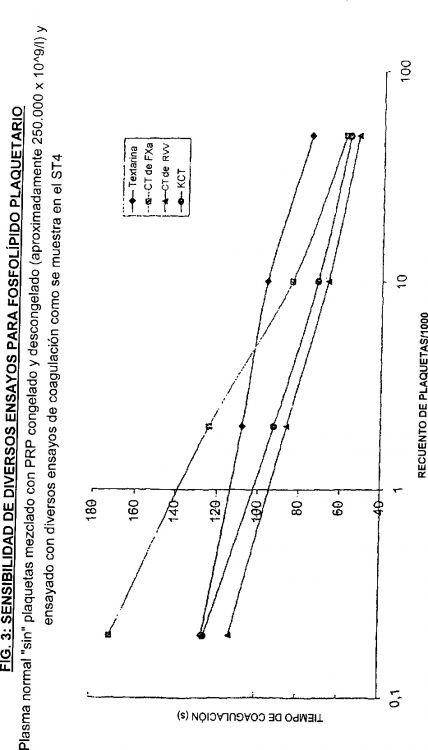
Fragmento de la descripción:
Método para detectar fosfolípido procoagulante.
Campo técnico
Esta invención se refiere a ensayos de coagulación sanguínea y, más particularmente, se refiere a un método mejorado para un marcador de trombosis y activación de plaquetas y un factor de riesgo trombótico potencial.
Técnica antecedente
Los fosfolípidos procoagulantes, incluyendo, por ejemplo, fosfolípidos aniónicos tales como fosfatidil serina, tienen un papel importante en el mecanismo de coagulación sanguínea. Los fosfolípidos procoagulantes son necesarios en la ruta de coagulación intrínseca para la conversión del factor X en Xa por los factores VIIIa y IXa, y también en la ruta común para escisión de protrombina en trombina por factor Xa. Forman parte del complejo activador de factor tisular. En mecanismos antitrombóticos están implicados en la activación de proteína C por el complejo de trombina/trombomodulina y en la destrucción del factor Va por proteína C activada.
Típicamente están presentes bajos niveles de fosfolípidos procoagulantes en la sangre de individuos sanos, probablemente como micropartículas derivadas de una diversidad de células, principalmente plaquetas, pero estos niveles aumentan cuando las plaquetas se activan, por ejemplo, en respuesta a una lesión y a la activación de la coagulación sanguínea, del complemento o de mecanismos inmunológicos. Las plaquetas in vitro expresan una actividad procoagulante máxima después de la congelación y descongelación o de la activación por colágeno/trombina o agentes de alteración de la membrana tales como ionóforos. La activación anormal de plaquetas in vivo se produce durante episodios trombóticos, embolia, septicemia, coagulación intravascular diseminada e infarto. Por el contrario, se produce una activación inadecuada de plaquetas en ciertos trastornos sanguíneos tales como enfermedad de von Willebrand y con diversas anomalías de plaquetas.
Pueden detectarse tradicionalmente fosfolípidos procoagulantes en una muestra de plasma sanguíneo de paciente mediante un ensayo de coagulación, por ejemplo, el ensayo de veneno de víbora de Russell (en lo sucesivo "RVVT"), aunque dichos ensayos se usan más convenientemente para diagnosticar el lupus anticoagulante. El veneno usado en el RVVT contiene metaloproteasas que activan específicamente los factores V y X. Después de la adición de veneno e iones de calcio, la coagulación se desarrolla con una dependencia casi absoluta de fosfolípido procoagulante en la muestra del paciente. La cantidad de fosfolípido procoagulante en la muestra del paciente se determina de acuerdo con el tiempo necesario para la mezcla de ensayo para formar fibrina y coagularse y, por lo tanto, cesar de fluir en un tubo o aumentar la turbidez óptica o bloquear un orificio o apertura. El tiempo de coagulación o tiempo necesario para que se forme un coágulo de fibrina puede sustituirse como un indicador de punto final en esta y en descripciones posteriores mediante un sustrato cromogénico que da un producto coloreado fácilmente detectable cuando actúa sobre él la enzima de coagulación principal, trombina.
Cuando se sospecha que un paciente tiene una deficiencia de un factor tal como Factor X, V, II o fibrinógeno insuficiente, o está recibiendo anticoagulantes, la muestra del paciente se mezcla típicamente con una muestra de plasma humano normal sin plaquetas con el fin de suministrar los factores en los que es deficiente la muestra. Este plasma humano normal sin plaquetas se conoce típicamente como "plasma de sustrato". El plasma de sustrato usado en estos ensayos es idealmente sin plaquetas ya que de otro modo la coagulación no dependería absolutamente del fosfolípido procoagulante contenido en la muestra del paciente.
En el RVVT y otros ensayos de coagulación, el plasma de sustrato se prepara habitualmente por centrifugación a alta velocidad y/o filtración. Una desventaja principal de este procedimiento es que es difícil controlar la reducción de fosfolípido procoagulante del plasma de sustrato. El plasma fresco es esencial y con frecuencia esto es poco práctico de obtener. Una vez que el plasma se ha congelado, las plaquetas contenidas en el mismo se activan y liberan el fosfolípido procoagulante. Por consiguiente, se limita la sensibilidad proporcionada por el RVVT y otros ensayos de coagulación para la detección de fosfolípido procoagulante en la muestra del paciente y la capacidad para regular la especificidad de estos ensayos. Una desventaja adicional es que estos procesos no eliminan algunas micropartículas de plaquetas que pueden tener una flotabilidad neutra o pueden ser demasiado pequeñas para eliminarse por filtración.
Otra desventaja de los métodos actuales para la determinación de fosfolípido procoagulante es su sensibilidad a inhibidores de la coagulación, tales como anticuerpos. Estos anticuerpos aparecen frecuentemente en enfermedades autoinmunes, por ejemplo, "síndrome antifosfolipídico" y causan la prolongación de la mayoría de ensayos de coagulación que emplean reactivos que contienen fosfolípidos y, por lo tanto, dan resultados falsos negativos en los ensayos actuales para fosfolípidos procoagulantes.
Boffa M. C., 1980 (Thrombosis research 17, páginas 567-572, 1980) describe un método para evaluar la actividad procoagulante relacionada con fosfolípidos en una muestra de plasma de un paciente. Dicho método consiste simplemente en añadir sucesivamente a plasma centrifugado a alta velocidad (es decir, a un plasma con fosfolípido reducido preparado por centrifugación), una muestra de plasma de paciente a analizar y fosfolipasa de berus. Después de la adición de cloruro cálcico, se registra el tiempo de coagulación y se compara con el de los controles.
Boffa M. C., 1974 (Thrombosis research 4, Número de Suplemento 1, páginas 89-90, 1974) describe un método para determinar la actividad procoagulante de fosfolípidos en una muestra de sangre o plasma de un paciente, usando una fosfolipasa A2 como inhibidor de fosfolípidos específicos de veneno. Dicho método consiste en las siguientes etapas: (i) un plasma "normal" se trata con una fosfolipasa A2 aislada del veneno de Vipera berus; (ii) la muestra de plasma o sangre a analizar se añade al plasma tratado; (iii) el tiempo de recalcificación de la mezcla se registra y se compara con el de los controles.
Sumario de la invención
En vista del papel de fosfolípidos procoagulantes en la patogénesis de episodios trombóticos y su potencial como marcadores de la activación de plaquetas, existe la necesidad de un método mejorado para detectar la presencia de y la cantidad de fosfolípido procoagulante en una muestra.
Por lo tanto, la presente solicitud describe un método para determinar la cantidad de fosfolípido procoagulante en una muestra, comprendiendo el método las etapas (i) a (iii) realizadas en el siguiente orden: (i) formar una mezcla de la muestra y un plasma de sustrato que se ha hecho liberado o liberado sustancialmente de suficiente fosfolípido procoagulante para al menos reducir la capacidad del plasma de sustrato para coagular, donde dicho plasma de sustrato se ha liberado o liberado sustancialmente de fosfolípido procoagulante por tratamiento con una fosfolipasa; (ii) poner en contacto la mezcla con un reactivo para activar la coagulación del plasma en condiciones en las que el fosfolípido procoagulante es el componente limitante de velocidad de la mezcla, y (iii) determinar el tiempo de coagulación de la mezcla.
De acuerdo con un primer aspecto de esta invención se proporciona un método para determinar la cantidad de fosfolípido procoagulante en una muestra humana, comprendiendo el método las etapas (i) a (iii) realizadas en el siguiente orden: (i) formar una mezcla de la muestra humana y un plasma de sustrato no humano que se ha liberado o liberado sustancialmente de suficiente fosfolípido procoagulante para al menos reducir la capacidad del plasma de sustrato para coagular, donde dicho plasma de sustrato se ha liberado o liberado sustancialmente de fosfolípido procoagulante por tratamiento con una fosfolipasa; (ii) poner en contacto la mezcla con factor Xa en condiciones en las que el fosfolípido procoagulante es el componente limitante de velocidad de la mezcla; y (iii) determinar el tiempo de coagulación de la mezcla.
La aplicación también describe un método de determinación de la cantidad de plaquetas activadas y micropartículas de plaquetas en una muestra, comprendiendo el método las etapas (i) a (iii) realizadas en el orden siguiente: (i) formar una mezcla de la muestra y un plasma de sustrato que...
Reivindicaciones:
1. Un método para determinar la cantidad de fosfolípido procoagulante en una muestra humana, comprendiendo dicho método las etapas (i) a (iii) realizadas en el siguiente orden:
2. Un método de acuerdo con la reivindicación 1, en el que la muestra se selecciona del grupo que consiste en sangre, plasma y suero.
3. Un método de acuerdo con la reivindicación 2, en el que dicha sangre es sangre anticoagulada.
4. Un método de acuerdo con la reivindicación 1, en el que la medición se realiza en comparación con plasmas de referencia o soluciones que contienen cantidades conocidas de fosfolípido procoagulante y los valores desconocidos pueden interpolarse a partir de una curva de calibración construida apropiadamente.
5. El método de la reivindicación 1, en el que dicho plasma de sustrato procede de sangre tratada con citrato.
6. El método de la reivindicación 1, en el que dicho plasma de sustrato se obtiene de un miembro seleccionado del grupo de animales vertebrados que consiste en cerdo, caballo, vaca, oveja, cabra, camello, mono, perro, gato, zorro, elefante, llama, conejo, visón, mapache, canguro y mezclas de los mismos.
7. El método de la reivindicación 6, en el que dicho plasma de sustrato se obtiene de cerdos.
8. El método de la reivindicación 1, en el que la fosfolipasa se obtiene del veneno seleccionado del grupo que consiste en Naja mossambica, Naja nigricollis, Agkistrodon halys, Vipera berus, Vipera russeli, Crotalus durissus, Enhyrdrina schistose, Oxyuranus scutellatus y Apis mellifera.
9. El método de la reivindicación 1, en el que la fosfolipasa se obtiene de uno de un grupo seleccionado que consiste en Streptomyces violaceoruber, especies de Vibrio, Clostridium perfringens o Bacillus cereus.
10. El método de la reivindicación 1, en el que el factor Xa procede de un mamífero distinto de un ser humano.
11. Un método para determinar la cantidad de plaquetas activadas y micropartículas de plaquetas en una muestra humana, comprendiendo dicho método las etapas (i) a (iv) realizadas en el siguiente orden:
12. Un método de acuerdo con la reivindicación 11, en el que dicho método determina si un paciente ha tenido un episodio trombótico reciente.
13. Un método de acuerdo con la reivindicación 11, en el que dicho método determina si un paciente ha tenido un trastorno clínico que implica activación de plaquetas.
14. El método de acuerdo con la reivindicación 12, en el que el episodio trombótico se selecciona del grupo que consiste en coagulación intravascular diseminada, trombosis venosa profunda, embolia, traumatismo tisular, septicemia e infarto.
15. El método de la reivindicación 11, en el que la fosfolipasa se obtiene de veneno seleccionado del grupo que consiste en Naja mossambica, Naja nigricollis, Agkistrodon halys, Vipera berus, Vipera russeli, Crotalus durissus, Enhyrdrina schistose, Oxyuranus scutellatus y Apis mellifera.
16. El método de la reivindicación 11, en el que la fosfolipasa se obtiene de uno de un grupo seleccionado que consiste en Streptomyces violaceoruber, especies de Vibrio, Clostridium perfringens o Bacillus cereus.
17. El método de la reivindicación 11, en el que el factor Xa procede de un mamífero distinto de un ser humano.
18. El método de la reivindicación 11, en el que el plasma de sustrato se ha formado a partir de factores V y protrombina.
19. El método de la reivindicación 18, en el que dichos factores V y protrombina están libres de fosfolípidos.
20. El método de la reivindicación 18, en el que dichos factores V y protrombina son de origen animal o humano.
21. El método de una cualquiera de las reivindicaciones 11 a 20, en el que dicho plasma de sustrato se obtiene de un miembro seleccionado del grupo que consiste en cerdo, caballo, vaca, oveja, cabra, camello, mono, perro, gato, zorro, elefante, llama, conejo, visón, mapache, canguro y mezclas de los mismos.
22. Un kit para determinar el nivel de fosfolípido procoagulante en una muestra humana, comprendiendo dicho kit:
Patentes similares o relacionadas:
UN MACRO ANALOGICO EMBEBIDO EN UNA MATRIZ PUERTA DIGITAL., del 1 de Febrero de 1995, de INTERNATIONAL BUSINESS MACHINES CORPORATION: SE DESCRIBE UN CHIP DE MATRIZ DE PUERTA LOGICA SIMPLE QUE TIENE UNA PRIMERA PORCION DEDICADA A LA GENERACION DE UNA O MAS SEÑALES DE RELOJ Y LA OTRA […]
CIRCUITO DE ESTABILIZACION DE BLOQUEO DE FASE., del 16 de Diciembre de 1993, de RCA THOMSON LICENSING CORPORATION: EN SU UTILIZACION EN UN RECEPTOR DIGITAL DE TELEVISION, EL INVENTO ESTA ASOCIADO CON UN PRIMER CIRCUITO DE BLOQUEO DE FASE QUE PRODUCE UNA […]
DISPOSITIVO OSCILADOR PARA PRODUCCION DE AL MENOS DOS FRECUENCIAS DIFERENTES, del 16 de Febrero de 1993, de HAGENUK GMBH: SE PROPONE UN DISPOSITIVO OSCILADOR PARA PRODUCCION DE AL MENOS DOS FRECUENCIAS DIFERENTES CON AL MENOS DOS CIRCUITOS REGULADOS DE FASES SEPARADOS PLL Y OSCILADORES […]
SISTEMA RADIOTELEFONICO PARA COMUNICAR SEÑALES DE INFORMACION POR UN CANAL DE FRECUENCIA ASIGNADA, del 16 de Diciembre de 1988, de INTERNATIONAL MOBILE MACHINES CORPORATION.: SISTEMA RADIOTELEFONICO PARA COMUNICAR SEÑALES DE INFORMACION POR UN CANAL DE FRECUENCIA ASIGNADA, COMBINANDO UN SINTETIZADOR PARA GENERAL LA SEÑAL CON UNA MEMORIA DE LECTURA […]
MEJORAS EN DISPOSICIONES GENERADORAS DE FRECUENCIAS MULTIPLES SELECCIONABLES DE TRANSMISOR Y RECEPTOR DE RADIO., del 16 de Febrero de 1980, de GENERAL ELECTRIC COMPANY: Se conecta en asociación un generador de frecuencia múltiple, un sintetizador de canal, un sintetizador de transmisor y un sintetizador de receptor. El sintetizador […]
APARATO DE BUCLE DE ENGANCHE DE FASE., del 1 de Marzo de 2007, de MARCONI MOBILE SPA: Un aparato de bucle de enganche de fase, que comprende un primer bucle de enganche de fase que tiene un detector de fase de muestreo dispuesto para […]
Procedimiento de prueba de plaquetas en sangre, del 15 de Julio de 2020, de FUJIMORI KOGYO CO., LTD: Procedimiento para someter a prueba la agregación plaquetaria, que comprende someter sangre anticoagulada a un tratamiento débil de activación […]
Composición para la determinación de las características de coagulación de un líquido de ensayo, del 6 de Mayo de 2020, de C A CASYSO AG: Una composición de diagnóstico para su uso en el análisis viscoelástico de un líquido de ensayo seleccionado de entre sangre entera o plasma sanguíneo, que comprende: […]