PROCEDIMIENTO PARA LA IDENTIFICACION Y CUANTIFICACION DE LOS ENANTIOMEROS DEL AMINOACIDO NO PROTEICO CARNITINA EN ALIMENTOS POR ELECTROFORESIS CAPILAR ACOPLADA A ESPECTROMETRIA DE MASAS.
Procedimiento para la identificación y cuantificación de los enantiómeros del aminoácido no proteico carnitina en alimentos por Electroforesis Capilar acoplada a Espectrometría de Masas.
El objetivo de la invención es el desarrollo de un procedimiento analítico quiral por Electroforesis Capilar (CE) acoplada a Espectrometría de Masas (MS) que permita determinar de forma fidedigna cada uno de los enantiómeros del aminoácido no proteico carnitina (L- y D-carnitina) en alimentos.
La invención consiste en una separación electroforética utilizando la ciclodextrina Succinil-·-ciclodextrina (Succ-·-CD, grado de sustitución 4) en tampón formiato a pH 2.5 seguida de una detección al final del capilar por MS2 (384 · 179 m/z) empleando un líquido envolvente compuesto por isopropanol: agua (50/50 v/v) con 0.1 % (p/v) ácido fórmico a 3.3 {mi}L/min; un potencial de electronebulización de 4.5 kV; una presión de nebulización y un flujo del gas de secado de 2 psi y de 5 L/min, respectivamente; unatemperatura de 300ºC; un voltaje de fragmentación de 86.7 V y una amplitud de fragmentación de 1.20 V
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200703122.
Solicitante: UNIVERSIDAD DE ALCALA..
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: MARINA ALEGRE,MARIA LUISA, GARCIA-RUIZ,CARMEN, CASTRO PUYANA,MARIA, SANCHEZ HERNANDEZ,LAURA, CREGO NAVAZO,ANTONIO LUIS.
Fecha de Solicitud: 26 de Noviembre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 15 de Febrero de 2010.
Clasificación Internacional de Patentes:
- A23J3/00 NECESIDADES CORRIENTES DE LA VIDA. › A23 ALIMENTOS O PRODUCTOS ALIMENTICIOS; SU TRATAMIENTO, NO CUBIERTO POR OTRAS CLASES. › A23J COMPOSICIONES A BASE DE PROTEINAS PARA LA ALIMENTACION; TRATAMIENTO DE PROTEINAS PARA LA ALIMENTACION; COMPOSICIONES A BASE DE FOSFATIDOS PARA LA ALIMENTACION. › Tratamiento de proteínas para la alimentación.
- A23L1/305
- G01J3/00 FISICA. › G01 METROLOGIA; ENSAYOS. › G01J MEDIDA DE LA INTENSIDAD, DE LA VELOCIDAD, DEL ESPECTRO, DE LA POLARIZACION, DE LA FASE O DE CARACTERISTICAS DE IMPULSOS DE LA LUZ INFRARROJA, VISIBLE O ULTRAVIOLETA; COLORIMETRIA; PIROMETRIA DE RADIACIONES. › Espectrometría; Espectrofotometría; Monocromadores; Medida del color.
- G01N27/26 G01 […] › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › investigando variables electroquímicas; utilizando la electrólisis o la electroforesis.
Clasificación PCT:
Fragmento de la descripción:
Procedimiento para la identificación y cuantificación de los enantiómeros del aminoácido no proteico carnitina en alimentos por Electroforesis Capilar acoplada a Espectrometría de Masas.
El procedimiento analítico propuesto permite la identificación inequívoca y la cuantificación de los enantiómeros del aminoácido no proteico carnitina en alimentos. La técnica empleada ha sido la Electroforesis Capilar (CE) acoplada a la detección por Espectrometría de Masas (MS), utilizando una pequeña concentración de ciclodextrina como selector quiral. Teniendo en cuenta que la D-carnitina presenta un efecto tóxico en la salud, debido a que en procesos bioquímicos causa la inhibición de la enzima carnitina aciltransferasa, este procedimiento supone un gran avance por la posibilidad de determinar cada uno de los enantiómeros de carnitina por separado y así poder establecer la pureza óptica de L-carnitina en alimentos con el fin de evaluar la seguridad y calidad de los mismos. Asimismo, el procedimiento propuesto podrá ser utilizado para evitar fraudes económicos, ya que el empleo de L-carnitina aumenta el coste de producción respecto a la utilización de la mezcla racémica del compuesto que es más económica.
Estado de la técnica
La carnitina es un aminoácido no proteico presente en los seres humanos por vías endógenas y exógenas, puesto que se genera in vivo por rutas biosintéticas a partir de lisina o metionina, o se ingiere en la dieta, siendo los productos cárnicos la mejor fuente de carnitina, mientras los lácteos, el marisco y el pescado tienen un bajo contenido, y los vegetales son los que presentan el menor contenido [1]. La adición de carnitina en alimentos ha de ser controlada debido a que es un compuesto quiral cuyas dos formas enantioméricas presentan una actividad biológica muy diferenciada. La L-carnitina, es imprescindible para la producción de energía a partir del metabolismo de ácidos grasos [2]; sin embargo, la D-carnitina inhibe la enzima carnitina aciltranferasa reduciendo los niveles de L-carnitina.
Los métodos desarrollados hasta el momento para la separación enantiomérica de carnitina únicamente se han aplicado en la industria farmacéutica, ya que en el campo de los alimentos sólo se han desarrollado métodos no quirales. En principio, el control de la pureza óptica de la L-carnitina en formulaciones farmacéuticas se llevaba a cabo fundamentalmente por aplicación de métodos de RMN [3] o con reacciones enzimáticas específicas [4], pero estas técnicas no permitían la detección de niveles de D-carnitina por debajo de un 1%. En los últimos años, se han desarrollado métodos donde se aplican técnicas de separación como la Cromatografia Líquida de Alta Eficacia (HPLC) y CE.
En relación al empleo de HPLC, la separación de los enantiómeros de carnitina se ha llevado a cabo en base a dos estrategias, empleando columnas capilares con [5-7] y sin derivatización [8], o bien empleando un agente derivatizante quiral ((+)-[1-(9-fluorenil)etil]-cloroformato, FLEC) y una columna no quiral [9-11]. Estos métodos han sido aplicados sólo a muestras sencillas como patrones o formulaciones farmacéuticas llegando a detectar el enantiómero D a niveles entre 0.1 y 1% en tiempos inferiores a 30 min.
La CE utilizando ciclodextrinas como selectores quirales es, en la actualidad, una técnica con un gran potencial para la separación de los enantiómeros de un compuesto quiral. En este campo, hay trabajos descritos en la bibliografia en los que también se utiliza el reactivo (+)-FLEC para la separación de los enantiómeros de la carnitina mediante electroforesis capilar en zona (CZE) [9]. Sin embargo, el elevado coste de este agente derivatizante (50 mg ~ 350
Finalmente, hay que destacar que en los métodos de análisis quiral de carnitina descritos hasta el momento se ha empleado un sistema de detección por absorción UV, el cual al no ser específico no permite confirmar de forma inequívoca la identificación de la carnitina en las muestras analizadas.
Teniendo en cuenta las limitaciones descritas en la bibliografia para la determinación enantiomérica de la carnitina, y que en ningún caso se describe su cuantificación en alimentos, donde hay un gran número de muestras que contienen dicho aminoácido, tales como suplementos para deportistas, productos dietéticos para quemar grasas o muestras de leche infantiles, nuestra invención supone un nuevo procedimiento de análisis quiral de carnitina en alimentos funcionales.
Descripción de la invención
El procedimiento para la identificación enantioselectiva del aminoácido no proteico carnitina por CE-MS utilizando una CD como selector quiral se caracteriza por las condiciones experimentales tabuladas en la Tabla 1.

Ventajas principales del procedimiento
Las ventajas principales del procedimiento inventado son las siguientes:
En la Figura 1 se muestran los electroforegramas correspondientes a una disolución de una muestra de bebida de 20 µg/ml que contiene carnitina y a la misma disolución de muestra enriquecida con el patrón racémico de 20 µg/ml. Se observa que sólo aparecen los picos correspondientes a los dos enantiómeros de carnitina (perfectamente separados, Rs ~ 3), por lo que el método es específico...
Reivindicaciones:
1. Procedimiento de análisis quiral de carnitina caracterizado porque permite la separación, identificación y cuantificación de los enantiómeros de este aminoácido no proteico en alimentos por Electroforesis Capilar (CE) con acoplamiento a la detección por Espectrometria de Masas (MS) empleando una ciclodextrina como selector quiral.
2. Procedimiento, según la reivindicación 1, caracterizado porque requiere diferente tratamiento de muestra, previamente a la derivatización de carnitina con FMOC según el protocolo establecido por Vogt y col., dependiendo de la complejidad del alimento funcional analizado:
3. Procedimiento, según la reivindicación 1, que consiste en un medio de separación quiral para CE con fórmico 0.5 M ajustado a pH 2.5 con hidróxido amónico al 25% y conteniendo como selector quiral, una pequeña concentración (0.2% (p/v) o 1.25 mM) de succinil-?-ciclodextrina (Succ-?-CD, grado de sustitución 4).
4. Procedimiento, según la reivindicación 3, caracterizado porque se realiza en un capilar de sílice fundida no recubierto de 50 µm de diámetro interno y 375 µm de diámetro externo con una longitud total de 1 m que debe acondicionarse con ácido fosfórico 0.1 M, agua, tampón (fórmico 0.5 M a pH 2.5) y tampón conteniendo Succ-?-CD 0.2% (p/v), cada uno de ellos durante 2 min a un bar, previamente a la inyección de los patrones y muestras (50 mbar durante 12 s) y a la separación electroforética sumergiendo los extremos del capilar en tampón fórmico 0.5 M a pH 2.5.
5. Procedimiento, según la reivindicación 4, caracterizado porque la separación electroforética de los enantiómeros de carnitina se realiza empleando una temperatura de 25ºC y un voltaje de separación de 25 kV.
6. Procedimiento, según la reivindicación 1, caracterizado porque se realiza una detección al final del capilar de separación. Las condiciones para la detección por espectrometría de masas (MS) consisten en el empleo de un líquido envolvente compuesto por isopropanol:agua (50:50 v/v) con 0.1% (p/v) de ácido fórmico a un flujo de 3.3 µL/min; un potencial de electronebulización de 4.5 kV; una presión de nebulización y un flujo del gas de secado de 2 psi y de 5 L/min, respectivamente; una temperatura de 300ºC; un número máximo de iones acumulados de 50000 y un tiempo máximo de acumulación de iones de 300 ms, un voltaje de fragmentación de 86.7 V y conductor de la trampa 38.0.
7. Procedimiento, según la reivindicación 6, caracterizado por el empleo de un modo de MS2 para mejorar la sensibilidad y selectividad de detección seleccionando un ión precursor con una relación masalcarga (m/z) de 384 m/z (correspondiente al ión molecular del derivado de carnitina con FMOC) y un ión producto de 179 m/z, utilizando como parámetros importantes para la fragmentación un valor de anchura de aislamiento de 4 unidades de m/z, una amplitud de fragmentación de 1.20 V y un límite de fragmentación de 106 m/z.
8. Procedimiento, según la reivindicación 1, caracterizado por la identificación inequívoca de los enantiómeros D y L carnitina, que presentan espectros MS2 idénticos, en alimentos.
9. Procedimiento, según la reivindicación 1, caracterizado porque permite la determinación cuantitativa de los enantiómeros D y L carnitina en alimentos.
Patentes similares o relacionadas:
Procedimiento de detección y de identificación directa de un microorganismo en una muestra biológica diluida en un caldo de enriquecimiento, del 19 de Febrero de 2020, de BIOMERIEUX: Procedimiento de detección de al menos un microorganismo presente en una muestra colocada en un contenedor cerrado, comprendiendo dicho método esencialmente las etapas siguientes: […]
MÉTODO DE DETECCIÓN DE PROTEÍNAS TOTALES EN UNA MUESTRA DE FLUIDO BIOLÓGICO EMPLEANDO TÉCNICAS ELECTROQUÍMICAS, del 9 de Enero de 2020, de ASOCIACIÓN CENTRO TECNOLÓGICO CEIT-IK4: Método de detección de proteínas totales en una muestra de fluido biológico empleando técnicas electroquímicas, que comprende emplear la muestra de fluido biológico; emplear […]
Calibración para ensayos de múltiples componentes, del 20 de Noviembre de 2019, de F. HOFFMANN-LA ROCHE AG: Un procedimiento de análisis de una muestra biológica usando un analizador y un ensayo , en el que se hace funcionar el analizador […]
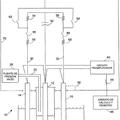 Configuración de electrodo para LIMCA, del 30 de Octubre de 2019, de NOVELIS, INC.: Un analizador de pureza de metal líquido que comprende:
una pared aislante que comprende un paso ;
un primer electrodo […]
Configuración de electrodo para LIMCA, del 30 de Octubre de 2019, de NOVELIS, INC.: Un analizador de pureza de metal líquido que comprende:
una pared aislante que comprende un paso ;
un primer electrodo […]
Estructura de resistencia, del 2 de Octubre de 2019, de Vivachek Biotech (Hangzhou) Co., Ltd: Una estructura de resistencia que comprende: un primer electrodo ; un segundo electrodo ; una pluralidad de primeros elementos de resistencia , en donde […]
Dispositivo de análisis y método para detectar monóxido de nitrógeno en una fase gaseosa, del 15 de Mayo de 2019, de CIRCASSIA AB: Un dispositivo de análisis para detectar un analito en una fase gaseosa, comprendiendo dicho dispositivo de análisis una fase líquida y al menos un sensor , […]
Método y aparato para el análisis de propiedades electroquímicas, del 22 de Abril de 2019, de AGAMATRIX, INC: Un método para evaluar una muestra para la presencia de un analito seleccionado que comprende las etapas de: (a) introducir la muestra […]
Banda de reactivo para tira de ensayo, del 24 de Septiembre de 2018, de F. HOFFMANN-LA ROCHE AG: Tira de ensayo , que comprende: un cuerpo de tira de ensayo que presenta extremos de inserción de medidor y de recepción de […]