PROCEDIMIENTO DE CLASIFICACION DE TEJIDOS IN VIVO.
Procedimiento de clasificación in vivo de tejido vivo empleando una agrupación ordenada de convertidores de ultrasonidos,
un dispositivo de control para la agrupación ordenada de convertidores, al menos una fuente de luz con pequeño ancho espectral en el dominio de longitudes de onda por encima de 500 nm, al menos un detector de luz y un ordenador de procesos para procesar los valores de medida del detector de luz, en donde el detector de luz capta solamente luz retrodispersada desde el tejido, la agrupación ordenada de convertidores de ultrasonidos irradia el tejido con ultrasonidos enfocados durante la iluminación con esta al menos una fuente de luz y el ordenador de procesos aísla la contribución de la luz dispersada en el foco de ultrasonidos a la intensidad de luz total medida por el detector de luz y calcula a partir de ella parámetros ópticos para el tejido en el foco de ultrasonidos, caracterizado porque el ordenador de procesos deriva de los parámetros ópticos calculados, como magnitud característica, la desviación de estos parámetros ópticos respecto de valores de referencia en tejido sano registrados durante la medición, cuya desviación es optimizada respecto de un criterio de optimalidad prefijado variando para ello la posición del foco de ultrasonidos en el tejido por medio del dispositivo de control de conformidad con el ordenador de procesos, y el ordenador de procesos compara los parámetros ópticos en la posición óptima descubierta del foco de ultrasonidos con una tabla de datos almacenada y clasifica así el tejido
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/DE2006/001174.
Solicitante: NIRLUS ENGINEERING AG.
Nacionalidad solicitante: Alemania.
Dirección: SALZWIESE 3,23560 LUBECK.
Inventor/es: HERRMANN VERA.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Abril de 2010.
Clasificación Internacional de Patentes:
- A61B5/00P
- A61B8/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Diagnóstico utilizando ondas ultrasónicas, sónicas o infrasónicas.
Clasificación PCT:
- A61B5/00 A61B […] › Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos.
- A61B8/00 A61B […] › Diagnóstico utilizando ondas ultrasónicas, sónicas o infrasónicas.
Fragmento de la descripción:
Procedimiento de clasificación de tejidos in vivo.
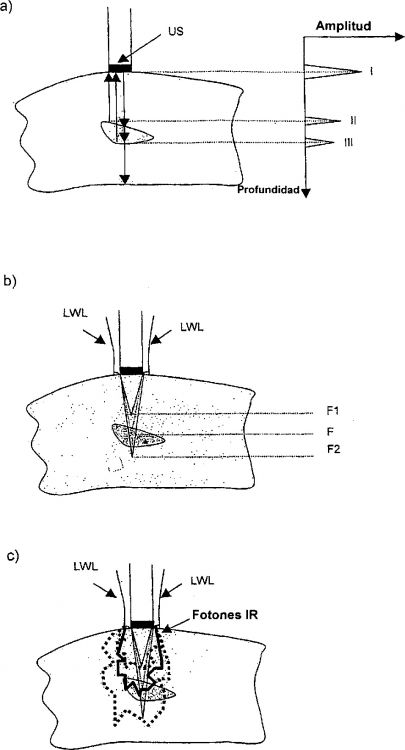
La invención concierne a un procedimiento de clasificación de tejidos in vivo, en el que se aplica radiación de ultrasonidos y de luz infrarroja a tejido vivo, especialmente al cuerpo humano o animal, y se deducen de la luz nuevamente saliente parámetros ópticos locales del tejido, especialmente el poder de absorción y/o de retrodispersión del mismo, con lo que se puede clasificar el tejido.
Las exploraciones con ultrasonidos para descubrir tejido normal en el organismo vivo son estado de la técnica desde hace mucho tiempo. Un campo de aplicación usual es el diagnóstico de mama, es decir, la detección de cáncer de mama en mujeres. El tejido maligno, especialmente el tejido canceroso, se caracteriza, entre otras cosas, por propiedades mecánicas diferentes de las del tejido sano circundante, de modo que en la irradiación con ultrasonidos los contrastes de impedancia en superficies límite conducen a la reflexión de las ondas acústicas. Esto se aprovecha para la localización de tejido normal. Sin embargo, la sola exploración con ultrasonidos no permite sacar ninguna conclusión acerca de si la anomalía descubierta del tejido consiste en un tumor maligno. Por este motivo, es corriente la toma de una muestra del candidato a tumor (biopsia) para la determinación definitiva en el laboratorio.
Con ayuda de las muestras tomadas no solo se puede clasificar exactamente el tejido, sino que también se pueden medir exactamente sus propiedades ópticas. En particular, se pone de manifiesto que las células cancerosas absorben determinadas longitudes de onda de la luz de los espectros de infrarrojo cercano (NIR) e infrarrojo medio (MIR) en una cuantía sensiblemente mayor que la de células sanas.
Como estado de la técnica se puede citar el documento DE 103 11 408 B3 proveniente de la inventora.
El cuerpo humano es ampliamente transparente, a causa de los mínimos de la banda de agua, en el dominio de longitudes de onda comprendido entre aproximadamente 600 y 1000 nm ("ventana biológica"). Es decir, la luz puede penetrar profundamente en el tejido, atravesarlo o bien retornar a la superficie iluminada. Existen aún otras "ventanas transparentes" en el espectro MIR caracterizadas por una pequeña absorción de agua en comparación con otros constituyentes del tejido, por ejemplo entre 5000 y 7500 nm e incluso entre 10 y 25 micrómetros.
Dentro de tales "ventanas transparentes" es posible especificar para cada constituyente individual del tejido una longitud de onda de luz que sea bien absorbida o dispersada por esta porción de tejido. Es ya conocido por estudios ex vivo de tejido tumoral extraído el hecho de que algunas longitudes de onda son especialmente características de células cancerosas, entre otras cosas porque éstas contienen determinadas sustancias que no se presentan en el tejido sano.
El documento WO 94/28795 propone un procedimiento para realizar una clasificación de tejidos in vivo mediante la aplicación combinada de irradiación de ultrasonidos enfocados y luz NIR. Como señal de medida sirve allí la radiación transmitida y/o retrodispersada -que sale del tejido- en el dominio de longitudes de onda de 600 a 1500 nm, la cual varía mientras se desplaza por el tejido el foco de ultrasonidos. El desplazamiento del foco es posible, por ejemplo, mediante una activación adecuada de una agrupación ordenada de transductores, descrita, por ejemplo, en el documento US 2 322 068.
El documento WO 94/28795 aporta en particular la enseñanza de que
- el foco deberá ser movido continuamente en tres dimensiones por el tejido a explorar para recorrer tanto tejido normal como tejido anormal a fin de que el tejido anormal pueda ser clasificado con ayuda del "contraste" con el tejido normal;
- la radiación de los ultrasonidos enfocados ha de aplicarse en forma modulada en amplitud para valorar el tejido respecto de parámetros mecánicos (por ejemplo, tiempo de relajación) con ayuda de la influencia de la amplitud variable sobre la señal luminosa;
- la posición del foco deberá mantenerse fija en el sitio de una influencia significativa de la amplitud de los ultrasonidos sobre la señal óptica para variar seguidamente la composición espectral de la luz NIR irradiada;
- a partir de la dependencia de la señal de medida respecto de la composición espectral se puede deducir la patología del tejido.
Todas las medidas citadas son seguramente razonables y posiblemente necesarias para un extenso análisis biofísico del tejido celular complejo. Como es sabido, las células vivas modifican, por ejemplo, sus propiedades ópticas bajo presión y en función de la temperatura. De aquí que los análisis detallados de las variaciones sean ciertamente el medio de elección para tener adecuadamente en cuenta todas las magnitudes de influencia importantes sobre la señal de medida óptica.
Sin embargo, en la práctica médica la cuestión interesante es en principio mucho más sencilla: se deberá extraer tejido sospechoso reconocido en la exploración con ultrasonidos y examinarlo en el laboratorio o quizá es esto evitable?
Habitualmente, una biopsia es ciertamente muy desagradable o incluso dolorosa para el paciente, pero para el médico que realiza el tratamiento está ligada más bien a un coste reducido. La cuantiosa medición según el documento WO 94/28795 es más bien desventajosa para el diagnóstico médico, puesto que
- solamente el desplazamiento continuo del foco de ultrasonidos (volumen < 1 mm3) por un campo de medida 3D al menos 1000 veces mayor es posible únicamente con lentitud y, por tanto, exige mucho tiempo;
- la observación de parámetros mecánicos de las células para descubrir areales malignos parece ser bastante complicada en comparación con la medición corriente por reflexión de ultrasonidos, aún cuando quizá permita un mapeado más exacto, si bien esto no le interesa imprescindiblemente al médico (al menos no para la detección prematura de cáncer);
- la variación de la composición espectral de la luz de medida requiere fuentes de luz y/o analizadores espectrales sintonizables que, tomados por separado, son ya componentes caros, de modo que el dispositivo propuesto permite esperar considerables costes de adquisición.
Aparte de estos inconvenientes, el dispositivo del documento WO 94/28795 está diseñado prioritariamente para la detección de luz transmitida, aún cuando se menciona explícitamente un dispositivo de medida unilateral que mide solamente luz retrodispersada. No obstante, la luz retrodispersada está sometida comúnmente a dispersiones múltiples, es decir que recorre un camino apenas previsible desde la fuente de luz hasta el detector dispuesto al lado de ella. Por tanto, no es tampoco seguro si la luz retornante ha recorrido, por ejemplo, el foco de ultrasonidos. Dicho de otra manera, en la retrodispersión pura existe el problema -no resuelto por el documento WO 94/28795- de la localización de la fuente para las contribuciones a la señal de medida óptica.
Sin embargo, el documento DE 103 11 408 B3 anteriormente mencionado describe una posibilidad de determinar la concentración de constituyentes de la sangre, por vía no invasiva, a partir de la retrodispersión de longitudes de onda IR especiales, posicionándose un foco de ultrasonidos en el interior de un vaso sanguíneo para marcar la región de retrodispersión. El procedimiento de evaluación está diseñado para diferenciar la luz retornante del foco frente a la restante luz retrodispersada y para determinar solamente propiedades ópticas para la región del foco. El dispositivo del documento DE 103 11 408 B3 emplea una pluralidad de diodos de láser IR cuyas longitudes de onda se han acomodado de antemano al problema planteado, especialmente a la medición de oxígeno en sangre. El dispositivo no es adecuado, sin más medidas, para la exploración general de tejidos, ya que, entre otras cosas, confía también en el descubrimiento de una posición adecuada del foco según el principio Doppler, presuponiendo este descubrimiento la presencia de un volumen suficiente de sangre circulante en forma dirigida.
El problema de la invención consiste ahora en perfeccionar el estado de la técnica en el sentido de que se obtenga un procedimiento simplificado para la clasificación no invasiva de tejido in vivo.
El problema se resuelve por medio de un procedimiento con las características de la reivindicación 1. Las reivindicaciones subordinadas...
Reivindicaciones:
1. Procedimiento de clasificación in vivo de tejido vivo empleando una agrupación ordenada de convertidores de ultrasonidos, un dispositivo de control para la agrupación ordenada de convertidores, al menos una fuente de luz con pequeño ancho espectral en el dominio de longitudes de onda por encima de 500 nm, al menos un detector de luz y un ordenador de procesos para procesar los valores de medida del detector de luz, en donde el detector de luz capta solamente luz retrodispersada desde el tejido, la agrupación ordenada de convertidores de ultrasonidos irradia el tejido con ultrasonidos enfocados durante la iluminación con esta al menos una fuente de luz y el ordenador de procesos aísla la contribución de la luz dispersada en el foco de ultrasonidos a la intensidad de luz total medida por el detector de luz y calcula a partir de ella parámetros ópticos para el tejido en el foco de ultrasonidos, caracterizado porque el ordenador de procesos deriva de los parámetros ópticos calculados, como magnitud característica, la desviación de estos parámetros ópticos respecto de valores de referencia en tejido sano registrados durante la medición, cuya desviación es optimizada respecto de un criterio de optimalidad prefijado variando para ello la posición del foco de ultrasonidos en el tejido por medio del dispositivo de control de conformidad con el ordenador de procesos, y el ordenador de procesos compara los parámetros ópticos en la posición óptima descubierta del foco de ultrasonidos con una tabla de datos almacenada y clasifica así el tejido.
2. Procedimiento según la reivindicación 1, caracterizado porque el criterio de optimalidad prefijado es la maximización de la magnitud característica.
3. Procedimiento según la reivindicación 1 ó 2, caracterizado porque antes de la medición de los parámetros ópticos se realiza un barrido con ultrasonidos en el que el dispositivo de control registra los tiempos de propagación de ondas acústicas reflejadas, y se determina a partir de ellos una región del tejido a clasificar en el que se debe formar el foco de ultrasonidos.
4. Procedimiento según cualquiera de las reivindicaciones 1 a 3, caracterizado porque la tabla de datos almacenada en el ordenador de procesos comprende clasificaciones de tejidos y sus parámetros ópticos obtenidos por mediciones ex vivo.
5. Procedimiento según la reivindicación 4, caracterizado porque el ordenador de procesos almacena opcionalmente parámetros ópticos medidos y presenta una interfaz de usuario a través de la cual se pueden asignar clasificaciones de tejido a los parámetros almacenados, actualizándose así la tabla de datos almacenada.
6. Procedimiento según cualquiera de las reivindicaciones 1 a 5, caracterizado porque el ordenador de procesos, al comparar los parámetros ópticos con la tabla de datos almacenada, calcula y facilita una probabilidad de la exactitud de la clasificación.
Patentes similares o relacionadas:
 Método para usar una cubierta de sonda, del 29 de Julio de 2020, de SABAN VENTURES PTY LIMITED: Un método para prevenir la contaminación de una sonda ultrasónica descontaminada que comprende el paso de, inmediatamente después de la desinfección, […]
Método para usar una cubierta de sonda, del 29 de Julio de 2020, de SABAN VENTURES PTY LIMITED: Un método para prevenir la contaminación de una sonda ultrasónica descontaminada que comprende el paso de, inmediatamente después de la desinfección, […]
FUNDA ELECTRÓNICA PARA ADAPTACIÓN DE DISPOSITIVOS MÓVILES CON INSTRUMENTOS DE DIAGNÓSTICO MÉDICO MULTIDISCIPLINAR, del 27 de Julio de 2020, de RUESGA DELGADO,OSCAR: Funda electrónica para adaptación de dispositivos móviles con instrumentos de diagnóstico médico multidisciplinar que comprende una funda de uso electrónico […]
Sonda de ultrasonidos con alojamiento y punta intercambiable, del 1 de Julio de 2020, de ECHOSENS: Una sonda de ultrasonidos que comprende una punta intercambiable , un alojamiento de sonda de ultrasonidos , al menos un imán (12, […]
Un dispositivo para realizar anestesia regional, del 3 de Junio de 2020, de The Queen Elizabeth Hospital King's Lynn NHS Foundation Trust: Un dispositivo de administración anestésica que comprende: a) una aguja anestésica regional; (b) un tubo de alimentación y un dispositivo de infusión en […]
Escáner de ultrasonido portátil, del 13 de Mayo de 2020, de Innuvatech S.r.l: Procedimiento operativo de un escáner de ultrasonido portátil , dicho escáner de ultrasonido portátil comprende: - transductores adecuados para […]
DISPOSITIVO DE SUJECIÓN PARA SONDA ECOGRÁFICA, del 5 de Mayo de 2020, de CALVO LOBO, César: 1. Dispositivo de sujeción para la sonda ecográfica , caracterizado por dos piezas izquierda y derecha enfrentadas, formadas por dos partes perpendiculares […]
Método para análisis y procesamiento de datos de dispositivo de detección de elasticidad, y dispositivo de detección de elasticidad, del 15 de Abril de 2020, de Wuxi Hisky Medical Technologies Co., Ltd: Método para análisis y procesamiento de datos de un dispositivo de detección de elasticidad, comprendiendo el dispositivo de detección de elasticidad […]
Transductor ultrasónico de resonancia, del 1 de Abril de 2020, de CHONGQING RONGHAI MEDICAL ULTRASOUND INDUSTRY LTD: Un transductor ultrasónico de resonancia que comprende una primera fuente de ultrasonidos para transmitir ultrasonidos y una unidad de reflexión […]