Sistema terapéutico transdérmico para la administración del principio activo buprenorfina.
Sistema terapéutico transdérmico para la administración de buprenorfina a la piel,
que comprende una capa dorsal impermeable al principio activo, al menos una capa de matriz autoadhesiva que contiene el principio activo buprenorfina y al menos un ácido carboxílico y dado el caso una capa protectora que es susceptible de ser quitada antes del uso, caracterizado por el hecho de que la capa de matriz está hecha a base de polisiloxanos o poliisobutileno, la buprenorfina está disuelta en el ácido carboxílico o en los ácidos carboxílicos, y esta solución está dispersada en forma de gutículas en la capa de matriz.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E14169050.
Solicitante: LTS LOHMANN THERAPIE-SYSTEME AG.
Nacionalidad solicitante: Alemania.
Dirección: LOHMANNSTRASSE 2 56626 ANDERNACH ALEMANIA.
Inventor/es: MULLER, WALTER, HILLE, THOMAS, HORSTMANN, MICHAEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/485 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Derivados del morfinano, p. ej. morfina, codeína.
- A61K9/70 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Bases para tiras, hojas o filamentos.
PDF original: ES-2543977_T3.pdf
Fragmento de la descripción:
Sistema terapéutico transdérmico para la administración del principio activo buprenorfina
[0001] La presente invención se refiere a un sistema terapéutico transdérmico con al menos un ácido carboxílico que determina la solubilidad de la buprenorfina en la capa matriz y es asimismo reabsorbible para la terapia del dolor con un claramente incrementando aprovechamiento del principio activo.
[0002] El principio activo buprenorfina (17-(cicloprop¡lmet¡l)-a-(1,1-d¡met¡let¡l)-4,5-epox¡-18,19-d¡h¡dro-3-hidroxi-6-metoxi- a-met¡l-6,14-etenomorf¡nan-7-metanol) es un opiato parcialmente sintético cuya ventaja frente a otros compuestos de esta clase de sustancias radica en una más alta eficacia. Esto significa que con dosis diarias de en torno a 1 mg puede lograrse ausencia de dolor en pacientes con cáncer o tumor con diagnóstico infausto en el estadio final. Además la buprenorfina se distingue del opioide sintético fentanilo y sus análogos en que su potencial de adicción es menor que el de estos compuestos. La desventaja consiste en que debido al alto peso molecular de la buprenorfina, que es de 467,64 daltons, resulta difícil llevarla a resorción transdérmica.
[0003] Sin embargo ya son obtenibles en el mercado sistemas transdérmicos con contenido de buprenorfina (como p. ej. el Transtec® o el Norspan®). En la patente alemana DE 39 39 376 C1 está descrita su forma de funcionamiento. El principio activo está disuelto homogéneamente en una matriz de poliacrilato, sirviendo de promotor de la permeación y solubilizante un ácido carboxílico.
[0004] Los sistemas en los que el principio activo está disuelto homogéneamente se distinguen por lo común por un bajo aprovechamiento del principio activo. El motivo de ello es el de que la actividad termodinámica del principio activo, que determina el aporte de principio activo, disminuye durante la aplicación debido al descenso de la carga de principio activo. Un aporte de principio activo uniforme durante todo el tiempo de aplicación se logra tan sólo mediante una carga de principio activo relativamente alta en comparación con la cantidad a aportar. De los datos publicados sobre el producto Transtec® 35 comercializado en Europa puede deducirse p. ej. un aprovechamiento del principio activo de únicamente un 17% a lo largo del espacio de tiempo de aplicación. Puesto que la buprenorfina es un principio activo caro, un más alto aprovechamiento del principio activo serla muy ventajoso desde el punto de vista de los costes.
[0005] Una carga lo menor posible del sistema con la buprenorfina, que pertenece a los anestésicos, y un contenido residual resultante de la misma lo más bajo posible tras el uso en los sistemas usados es además muy deseable desde el punto de vista de la seguridad.
[0006] La finalidad perseguida por la presente invención era por consiguiente la de desarrollar un sistema terapéutico transdérmico que con un claramente incrementado aprovechamiento del principio activo le hiciese al principio activo buprenorfina, del que es difícil lograr la reabsorción, accesible la aplicación transdérmica.
[0007] Esta finalidad es según la invención sorprendentemente alcanzada mediante un sistema terapéutico transdérmico para la administración de buprenorfina a la piel, en donde el sistema terapéutico transdérmico comprende una capa dorsal impermeable al principio activo, al menos una capa de matriz que es autoadhesiva y contiene el principio activo buprenorfina y al menos un ácido carboxílico, y dado el caso una capa protectora susceptible de ser desprendida antes del uso. La capa de matriz está hecha a base de polisiloxanos o poliisobutileno. La buprenorfina está disuelta en el ácido carboxílico o en los ácidos carboxllicos y esta solución está dispersada en forma de gutículas en la capa de matriz. Esto es tanto más asombroso, por cuanto que la buprenorfina, debido a sus conocidas propiedades fisicoquímicas, y en particular debido a su mala solubilidad, a su comparativamente alto punto de fusión de 216°C y a su ya mencionado alto peso molecular, tiende fácilmente a la cristalización. Por este motivo se usa un solvente con al menos un grupo ácido, para impedir la cristalización de la buprenorfina durante el almacenamiento de la forma medicinal. Tanto la propia buprenorfina como los ácidos carboxllicos tienen una extremadamente baja solubilidad en polisiloxanos o poliisobutileno. Debido a ello es posible disolver buprenorfina en un ácido carboxílico y dispersar esta solución en forma de gutículas en una capa de matriz hecha a base de polisiloxanos, preferiblemente de dimetilpolisiloxanos amino-resistentes, con particular preferencia de una mezcla de un dimetilpolisiloxano amino- resistente y un dimetilpolisiloxano no amino-resistente, estando el dimetilpolisiloxano no amino-resistente contenido en hasta un máximo de un 40% en peso, y preferiblemente en un porcentaje de un 2 a un 20% en peso, o de poliisobutileno como polímero base. Además es importante que la mezcla de buprenorfina y ácido carboxílico o ácidos carboxllicos sea liquida.
[0008] Habitualmente los ácidos carboxllicos que se usan son poco solubles en los solventes orgánicos de los adhesivos. Por consiguiente, la mezcla liquida de buprenorfina y ácido carboxílico puede ser dispersada en la solución del adhesivo, manteniéndose la dispersión tras haber sido quitado el solvente. La solubilidad de la buprenorfina depende en una capa de matriz de este tipo prácticamente tan sólo de la cantidad de ácido carboxílico o de ácidos carboxllicos. La cantidad de la solución dispersada puede ser de hasta un 40% en peso, no sobrepasándose preferiblemente un 20% en peso. El propio tamaño de las gutículas no deberla preferiblemente sobrepasar las 50 pm. El tamaño preferido depende además del espesor de la capa de matriz.
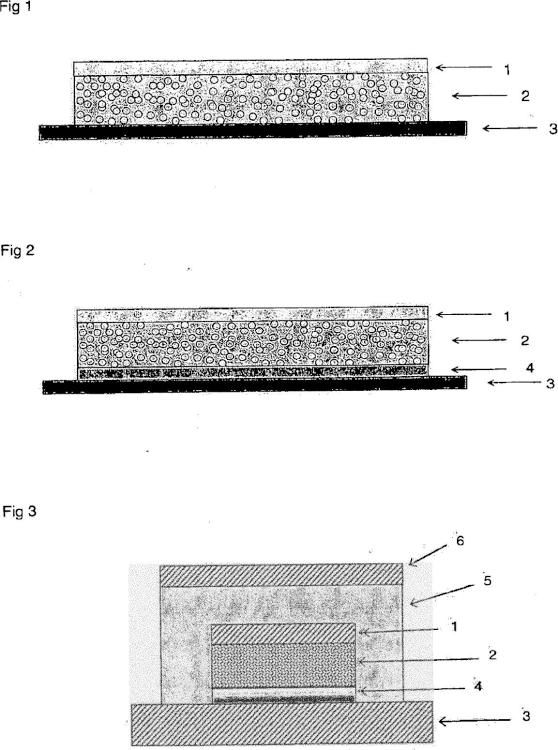
[0009] La Figura 1 muestra una representación esquemática de un sistema autoadhesivo unicapa de este tipo. En la Figura 2 está representado un sistema con capa de contacto con la piel, y la Figura 3 muestra un sistema multicapa con sobreparche. Ahí los distintos números de referencia significan lo siguiente:
1 Capa dorsal
2 Capa de matriz a base de polisiloxanos con gutículas dispersadas de una solución de buprenorfina en ácido carboxílico
3 Capa protectora a retirar antes del uso
4 Capa de contacto con la piel hecha a base de un adhesivo de poliacrilato
Capa autoadhesiva sin buprenorfina
6 Capa dorsal (p. ej. de color piel)
[0010] Puesto que los ácidos carboxílicos pueden ser asimismo reabsorbidos a través de la piel, se reduce durante el tiempo de aplicación su cantidad en el sistema y con la misma también la solubilidad a saturación de la buprenorfina. Gracias a ello se compensa la disminución de la actividad termodinámica de la buprenorfina, ocasionada por la liberación. La selección del ácido carboxílico se rige por la reabsorción a través de la piel, la cual, en comparación con la buprenorfina, es exactamente igual de rápida, y preferiblemente más rápida. Preferiblemente se usan ácidos carboxílicos líquidos a la temperatura de la piel. El ácido carboxílico o los ácidos carboxílicos se selecciona(n) de entre los miembros del grupo que consta de ácido oleico, ácido levulínico, ácido linólico y ácido linolénico. Con una adecuada realización se logra alcanzar estados sobresaturados durante el tiempo de aplicación. En los sistemas sobresaturados está incrementada la actividad termodinámica del principio activo y con la misma también la tasa de permeación por unidad de superficie en correspondencia con el factor de sobresaturación. Ventajosamente gracias a ello puede minimizarse la superficie de liberación y también la superficie del sistema. Durante el almacenamiento tanto la buprenorfina como el ácido permanecen en la matriz polímera, con lo cual el sistema está saturado al máximo durante este tiempo y queda excluida una recristalización del principio activo.
[0011] Otro aspecto de la invención concierne al efecto de que el aumento de la actividad termodinámica en tales sistemas con una liberación demasiado rápida del ácido puede conducir a que aumente excesivamente la tasa de permeación tras la aplicación. La consecuencia es la de que el sistema terapéutico transdérmico se agota prematuramente debido a una liberación del principio activo demasiado rápida. Se ha descubierto ahora que un efecto de este tipo se evita mediante la adición de otra capa hecha a base de poliacrilatos. Esta capa se encuentra preferiblemente entre la capa de matriz polímera con contenido de principio activo y la piel o bien entre la capa de matriz y la capa dorsal. Esta capa adicional se realiza preferiblemente como capa autoadhesiva de contacto con la piel
... [Seguir leyendo]
Reivindicaciones:
1. Sistema terapéutico transdérmico para la administración de buprenorfina a la piel, que comprende una capa dorsal Impermeable al principio activo, al menos una capa de matriz autoadhesiva que contiene el principio activo buprenorfina y al menos un ácido carboxíllco y dado el caso una capa protectora que es susceptible de ser quitada antes del uso, caracterizado por el hecho de que la capa de matriz está hecha a base de pollslloxanos o polllsobutlleno, la buprenorfina está disuelta en el ácido carboxíllco o en los ácidos carboxíllcos, y esta solución está dispersada en forma de gutículas en la capa de matriz.
2. Sistema terapéutico transdérmico según la reivindicación 1, caracterizado por el hecho de que el polisiloxano es un dlmetllpollslloxano amino-resistente.
3. Sistema terapéutico transdérmico según la reivindicación 1, caracterizado por el hecho de que el polisiloxano es una mezcla de un dlmetilpolisiloxano amino-resistente y un dlmetllpollsiloxano no amino-resistente, en donde el dlmetllpollslloxano no amino-resistente está contenido en un porcentaje de hasta un 40% en peso.
4. Sistema terapéutico transdérmico según una o varias de las reivindicaciones precedentes, caracterizado por el hecho de que el ácido carboxílico se difunde en la piel más rápidamente que el principio activo buprenorfina.
5. Sistema terapéutico transdérmico según una o varias de las reivindicaciones precedentes, caracterizado por el hecho de que la cantidad de la solución dispersada es de hasta un 40% en peso, y preferiblemente de hasta un 20% en peso.
6. Sistema terapéutico transdérmico según una o varias de las reivindicaciones precedentes, caracterizado por el hecho de que el ácido carboxílico es líquido a la temperatura de la piel.
7. Sistema terapéutico transdérmico según la reivindicación 6, caracterizado por el hecho de que el ácido carboxílico es seleccionado de entre los miembros del grupo que consta de ácido oleico, ácido levulínico, ácido llnóllco y ácido llnolénlco.
8. Sistema terapéutico transdérmico según la reivindicación 6 o 7, caracterizado por el hecho de que la buprenorfina y el ácido levulínico están en la misma relación en peso.
9. Sistema terapéutico transdérmico según una o varias de las reivindicaciones precedentes, caracterizado por el hecho de que se alcanza un aprovechamiento del principio activo bajo condiciones in vivo de al menos un 30%, preferiblemente de al menos un 40%, y con particular preferencia de al menos un 50%.
10. Sistema terapéutico transdérmico según una o varias de las reivindicaciones precedentes para su uso en la terapia del dolor.
Patentes similares o relacionadas:
Regímenes de dosificación de buprenorfina, del 1 de Julio de 2020, de Indivior UK Limited: Buprenorfina para su uso en un método para tratar el trastorno por uso de opioides en un ser humano que lo necesite, que comprende las etapas […]
 Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Gránulos de dispersión rápida, comprimidos de desintegración oral y métodos, del 3 de Junio de 2020, de Adare Pharmaceuticals, Inc: Microgránulos de dispersión rápida, farmacéuticamente aceptables, que tienen una mediana del tamaño de partícula en el rango de 100 μm a 300 […]
Dispositivos de administración transdérmica resistentes al abuso y composiciones que comprenden un agonista de opioides y un derivado N-óxido no administrado por vía transdérmica de un antagonista de opioide para el tratamiento del dolor, del 22 de Abril de 2020, de EURO-CELTIQUE S.A.: Un dispositivo de administración transdérmica que comprende una composición farmacéutica, en el que dicha composición comprende un derivado […]
Pulverizador de buprenorfina sublingual, del 22 de Abril de 2020, de Fresh Cut Development, LLC: Una formulación de pulverización sublingual que comprende una cantidad efectiva de buprenorfina, o una sal farmacéuticamente aceptable de la misma, […]
Formulación farmacéutica a base de ibuprofeno y codeína que tiene estabilidad mejorada, del 15 de Abril de 2020, de FARMASIERRA MANUFACTURING S.L: Formulación farmacéutica a base de ibuprofeno y codeínade estabilidad mejorada. La invención consiste en una nueva formulación farmacéuticaen forma […]
Parche transdérmico de oximorfona, del 8 de Abril de 2020, de Buzzz Pharmaceuticals Limited: Un parche transdérmico que tiene una capa que contiene el fármaco que comprende oximorfona o una sal farmacéuticamente aceptable de la misma, […]
Composiciones de buprenorfina y antagonistas del receptor de opioides mu, del 1 de Abril de 2020, de Alkermes Pharma Ireland Limited: Una composición que comprende buprenorfina y un antagonista del receptor opioide μ, en donde la composición está caracterizada por un Índice […]