Proceso para preparar amidas de ácidos carboxílicos pirazólicos.
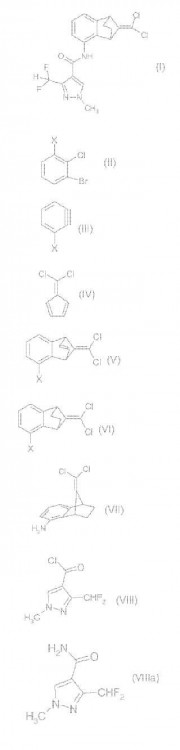
Un proceso para preparar el compuesto de fórmula I**Fórmula**
comprendiendo el proceso
a) hacer reaccionar un compuesto de fórmula II**Fórmula**
donde X es cloro o bromo,
con una especie organometálica en una atmósfera inerte para obtener un halobencino de fórmula III **Fórmula**
donde X es cloro o bromo; hacer reaccionar el halobencino de fórmula III formado de este modo con un fulveno de fórmula IV **Fórmula**
para obtener un compuesto de fórmula V **Fórmula**
donde X es cloro o bromo;
b) hidrogenar el compuesto de fórmula V en presencia de un catalizador metálico adecuado para obtener un compuesto de fórmula VI **Fórmula**
donde X es cloro o bromo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2011/055872.
Solicitante: SYNGENTA PARTICIPATIONS AG.
Nacionalidad solicitante: Suiza.
Dirección: SCHWARZWALDALLEE 215 4058 BASEL SUIZA.
Inventor/es: VETTIGER, THOMAS, GRIBKOV,DENIS, STOHLER,REMO, ROMMEL,MICHAEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C25/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 25/00 Compuestos que contienen al menos un halógeno unido a un ciclo aromático de seis miembros. › Hidrocarburos aromáticos halogenados con cadenas laterales insaturadas.
- C07D231/14 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 231/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,2 o diazol-1,2 hidrogenado. › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos, con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente a los átomos de carbono del ciclo.
PDF original: ES-2453919_T3.pdf
Fragmento de la descripción:
Proceso para preparar amidas de ácidos carboxílicos pirazólicos La presente invención se refiere a un proceso para preparar la (9-diclorometilen-1, 2, 3, 4-tetrahidro-1, 4metanonaftalen-5-il) amida del ácido 3-difluorometil-1-metil-1H-pirazol-4-carboxílico y a intermedios novedosos útiles 5 para este proceso.
El compuesto (9-diclorometilen-1, 2, 3, 4-tetrahidro-1, 4-metanonaftalen-5-il) amida del ácido 3-difluorometil-1-metil-1Hpirazol-4-carboxílico y sus propiedades microbicidas se describen, por ejemplo, en WO 2007/048556.
La preparación de la (9-diclorometilen-1, 2, 3, 4-tetrahidro-1, 4-metanonaftalen-5-il) amida del ácido 3-difluorometil-1metil-1H-pirazol-4-carboxílico se describe en WO 2007/048556. Dicho compuesto se puede preparar de acuerdo con 10 los esquemas 1 y 4 mediante los siguientes pasos:
a) hacer reaccionar el compuesto de fórmula A
COOH
NH2
(A) en presencia de un nitrito de alquilo con un compuesto de fórmula B
(B) , donde R’ y R’’ son, p. ej., alquilo C1-C4, para obtener un compuesto de fórmula C
NO2
(C) ,
b) hidrogenar el compuesto de fórmula C en presencia de un catalizador metálico adecuado para obtener un compuesto de fórmula D
NO2
c) ozonizar el compuesto de fórmula D y tratamiento posterior con un agente reductor para obtener un compuesto de fórmula E
NO2
d) hacer reaccionar el compuesto de fórmula E en presencia de trifenilfosfano/tetracloruro de carbono para obtener el 2, 9-diclorometiliden-5-nitrobenzonorborneno de fórmula F
NO2
e) hidrogenar el compuesto de fórmula F en presencia de un catalizador metálico para obtener el 2, 9diclorometiliden-5-aminobenzonorborneno de fórmula G
NH2
f) y hacer reaccionar el compuesto de fórmula G con un compuesto de fórmula H
FH
ClF O
N N
(H) ,
CH3
para obtener la (9-diclorometilen-1, 2, 3, 4-tetrahidro-1, 4-metanonaftalen-5-il) amida del ácido 3-difluorometil-1-metil1H-pirazol-4-carboxílico.
Una desventaja significativa de este proceso de la técnica anterior es la reacción de ozonólisis, que es difícil de controlar a gran escala. Además, el gran número de pasos de reacción reduce el rendimiento global del proceso e incrementa los costos de producción. Dichas desventajas hacen que este proceso sea poco rentable y especialmente inadecuado para una producción a gran escala.
Por consiguiente, el objetivo de la presente invención consiste en proporcionar un proceso novedoso para producir la (9-diclorometilen-1, 2, 3, 4-tetrahidro-1, 4-metanonaftalen-5-il) amida del ácido 3-difluorometil-1-metil-1H-pirazol-4
carboxílico que no presente las desventajas del proceso conocido y que permita preparar la (9-diclorometilen1, 2, 3, 4-tetrahidro-1, 4-metanonaftalen-5-il) amida del ácido 3-difluorometil-1-metil-1H-pirazol-4-carboxílico con rendimientos elevados y calidad satisfactoria de forma rentable.
Por lo tanto, de acuerdo con la presente invención, se proporciona un proceso para preparar el compuesto de fórmula I
CH3
comprendiendo el proceso a) hacer reaccionar un compuesto de fórmula II
X
Cl (II) ,
Br
donde X es cloro o bromo, con una especie organometálica tal como un (alquil C1-6) - o fenillitio o un haluro de (alquil C1-6) - o fenilmagnesio en atmósfera inerte para obtener un halobencino de fórmula III
(III)
X
donde X es cloro o bromo; hacer reaccionar el halobencino de fórmula III formado de este modo con un fulveno de fórmula IV
Cl
Cl
(IV) ,
para obtener un compuesto de fórmula V
X
donde X es cloro o bromo;
b) hidrogenar el compuesto de fórmula V en presencia de un catalizador metálico adecuado para obtener un compuesto de fórmula VI
X
donde X es cloro o bromo; y o bien c1) hacer reaccionar el compuesto de fórmula VI con NH3 en presencia de un catalizador que comprenda paladio y al menos un ligando para obtener el compuesto de fórmula VII
ClCl
(VII) ; H2N
y d) hacer reaccionar el compuesto de fórmula VII en presencia de una base con un compuesto de fórmula VIII
CHF2
(VIII) ,
H3C
para obtener el compuesto de fórmula I; o bien c2) hacer reaccionar el compuesto de fórmula VI
X
donde X es cloro o bromo, preferentemente bromo; en presencia de un disolvente, una base, un catalizador de cobre y al menos un ligando, con el compuesto de fórmula VIIIa H2N
(VIIIa) ,
CHF2
H3C
para obtener el compuesto de fórmula I.
Paso de reacción a) :
El compuesto de fórmula II, donde X es bromo, es conocido y se describe, por ejemplo, en Recueil des Travaux Chimiques des Pays-Bas, 81, 365 (1962) . El compuesto de fórmula II, donde X es cloro o bromo, se describe, por 15 ejemplo, en WO 2008/049507. El 1-bromo-2, 3-diclorobenceno se puede preparar mediante la denominada reacción de Sandmeyer a partir de 2, 3-dicloroanilina. Estas reacciones de Sandmeyer se pueden llevar a cabo o bien empleando un éster de tipo nitrito orgánico, tal como nitrito de tert-butilo o nitrito de isopentilo, en un disolvente orgánico, tal como acetonitrilo, en presencia de un bromuro cúprico como agente bromante (según se describe en Journal of Organic Chemistr y , 1977, 42, 2426-31) o bien mediante una reacción de dos pasos que implica la diazoación en un medio de reacción acuoso ácido a temperaturas comprendidas entre 0°C y 15°C empleando un nitrito inorgánico y a continuación la adición de la mezcla de reacción a una solución de bromuro cuproso (según se describe en Recueil des Travaux Chimiques des Pays-Bas et de la Belgique, 1932, 51, 98-113 y JP-6-2114-921) .
El 6, 6-diclorofulveno de fórmula IV (RN 35310-97-5) se describe en Chemical Communications, 20 (1971) , 12931294.
El compuesto de fórmula V es novedoso, se ha desarrollado especialmente para el proceso de acuerdo con la invención y, por consiguiente, constituye un objetivo adicional de la invención.
La reacción se puede llevar a cabo a temperaturas comprendidas entre -78 y 20 °C, preferentemente a -20 °C.
La reacción se lleva a cabo en condiciones de flujo continuo o semidiscontinuo, preferentemente en condiciones semidiscontinuas.
Para llevar a cabo el intercambio halógeno-litio, se emplean, como especies organometálicas, compuestos de aril-y alquillitio, por ejemplo, fenillitio, metillitio o n-butillitio, preferentemente n-butillitio.
Como disolventes, se emplean disolventes apróticos, preferentemente hidrocarburos tales como tolueno.
Se prefiere añadir tanto el alquillito como el trihalogenobenceno a una solución de diclorofulveno en un disolvente durante de 15 a 180 minutos, pero también se puede realizar la adición del alquillitio a una mezcla del trihalogenobenceno y el compuesto de fórmula IV en un disolvente. También es posible añadir el alquillitio y el compuesto de fórmula IV a una solución del trihalogenobenceno en un disolvente.
Normalmente se consigue una conversión completa de 15 a 180 minutos después de finalizar la adición de los reactivos correspondientes.
Paso de reacción b) :
El compuesto de fórmula VI se puede preparar mediante la reducción selectiva del doble enlace no clorado empleando níquel Raney (o catalizadores de Rh, Pd, Ir, Pt, Co y Fe, tanto soportados en un portador como combinados con un ligando) . La reacción se puede llevar a cabo a presión de hidrógeno atmosférica o elevada, preferentemente a presión atmosférica.
La reacción se puede llevar a cabo a temperatura ambiente o elevada, preferentemente a temperatura ambiente, en particular de 20 a 25 °C.
La reacción se lleva a cabo en disolventes que sean inertes al níquel Raney. Un disolvente preferido es acetato de etilo.
El compuesto de fórmula VI es novedoso, se ha desarrollado especialmente para el proceso de acuerdo con la invención y, por consiguiente, constituye un objetivo adicional de la invención.
Paso de reacción c1) :
De las dos variantes del proceso, del paso c1) al paso d) y el paso c2) , se prefiere la variante del paso c1) al paso d) . El catalizador que comprende paladio y al menos un ligando empleado en el proceso se formará generalmente a partir de un precursor de paladio y al menos un ligando adecuado. Cuando el proceso se lleve a cabo en un disolvente, normalmente el complejo será soluble en el disolvente. En el contexto de este proceso, los complejos de paladio incluyen explícitamente los constituidos por compuestos de paladio orgánicos cíclicos... [Seguir leyendo]
Reivindicaciones:
1. Un proceso para preparar el compuesto de fórmula I
CH3
comprendiendo el proceso a) hacer reaccionar un compuesto de fórmula II
Cl (II) , Br
donde X es cloro o bromo, con una especie organometálica en una atmósfera inerte para obtener un halobencino de 10 fórmula III
(III) ,
X
donde X es cloro o bromo; hacer reaccionar el halobencino de fórmula III formado de este modo con un fulveno de fórmula IV
Cl
Cl
(IV) ,
para obtener un compuesto de fórmula V
donde X es cloro o bromo; b) hidrogenar el compuesto de fórmula V en presencia de un catalizador metálico adecuado para obtener un
compuesto de fórmula VI
X
donde X es cloro o bromo; y o bien c1) hacer reaccionar el compuesto de fórmula VI con NH3 en presencia de un catalizador que comprenda paladio y al menos un ligando para obtener el compuesto de fórmula VII
Cl
Cl
(VII) , H2N
y d) hacer reaccionar el compuesto de fórmula VII en presencia de una base con un compuesto de fórmula VIII
CHF2
(VIII) , H3C
para obtener el compuesto de fórmula I; o bien 10 c2) hacer reaccionar el compuesto de fórmula VI
X
donde X es cloro o bromo, en presencia de un disolvente, una base, un catalizador de cobre y al menos un ligando, con el compuesto de fórmula VIIIa H2N
(VIIIa) , CHF2
H3C
para obtener el compuesto de fórmula I.
2. Un proceso de acuerdo con la reivindicación 1, donde en el paso a) la especie organometálica se selecciona entre haluros de (alquil C1-6) - o fenilitio y haluros de (alquil C1-6) - o fenilmagnesio.
3. Un proceso de acuerdo con la reivindicación 1, donde en el paso c) el ligando se selecciona entre ligandos de tipo ferrocenil-bifosfano.
4. Un proceso de acuerdo con la reivindicación 1, que comprende hacer reaccionar el compuesto de fórmula VI con NH3 en presencia de un catalizador que comprenda paladio y al menos un ligando para obtener el compuesto de fórmula VIII
Cl
Cl
(VII) ,
H2N y hacer reaccionar el compuesto de fórmula VII en presencia de una base con un compuesto de fórmula VIII
CHF2
(VIII) ,
H3C para obtener el compuesto de fórmula I.
5. El compuesto de fórmula V
donde X es cloro o bromo.
6. El compuesto de fórmula VI
X15 donde X es cloro o bromo.
Patentes similares o relacionadas:
Composiciones y métodos para tratar trastornos del SNC, del 6 de Mayo de 2020, de Sage Therapeutics, Inc: Un compuesto de la Fórmula (I): **(Ver fórmula)** una sal farmacéuticamente aceptable del mismo, en la que: A es un heterociclilo o un heteroarilo monocíclico o bicíclico […]
Inhibidores de 3,5-diaminopirazol quinasa, del 15 de Abril de 2020, de SMA Therapeutics, Inc: Compuesto de fórmula (II-a): **(Ver fórmula)** o un estereoisómero, enantiómero, mezcla de enantiómeros, mezcla de diastereómeros o variante isotópica de los mismos, o […]
Ligandos de receptores de neurotensina, del 8 de Abril de 2020, de 3B Pharmaceuticals GmbH: Un compuesto de fórmula (I): **(Ver fórmula)** en donde R1 se selecciona del grupo que consiste en hidrógeno, metilo y ciclopropilmetilo; AA-COOH es un aminoácido […]
Proceso de hidrogenación catalítica para preparar pirazoles, del 11 de Marzo de 2020, de BASF SE: Un proceso para preparar un compuesto de pirazol de formula V, o una sal, estereoisomero, tautomero o N-oxido del mismo **(Ver fórmula)** que comprende […]
Moduladores de teramuteína, del 15 de Enero de 2020, de HMI Medical Innovations, LLC: Un método in vitro para detectar o identificar una sustancia de prueba que es un inhibidor o activador de una proteína endógena que alberga una […]
Procedimiento para la síntesis de derivados de N-bencil-N-ciclopropil-1H-pirazol-4-carboxamida, del 7 de Noviembre de 2019, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Procedimiento de síntesis de pirazol carboxamida de fórmula (I)**Fórmula** en la que R está seleccionado entre el listado de 2-isopropilfenilo, […]
Procedimiento de promoción del crecimiento vegetal usando derivados de carboxamida, del 2 de Octubre de 2019, de BAYER CROPSCIENCE AG: Un procedimiento para promover, en plantas que se encuentran en un estado sin enfermedad, al menos un efecto de crecimiento vegetal seleccionado del grupo que consiste […]
Compuestos N-((het)arilmetil)-heteroaril-carboxamidas como inhibidores de la calicreína plasmática, del 3 de Julio de 2019, de Kalvista Pharmaceuticals Limited: Un compuesto seleccionado de:**Fórmula** y sus sales y solvatos farmacéuticamente aceptables.