Método para monofluorometilación de sustratos orgánicos para preparar compuestos orgánicos biológicamente activos.
Un método para preparar un compuesto farmacéuticamente activo que contiene un resto "CH2F" en un átomo de azufre,
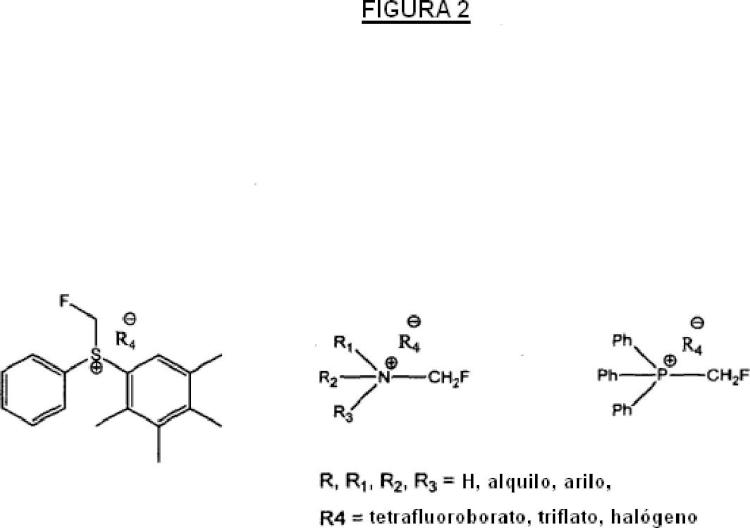
método que comprende el uso de un reactivo de monofluorometilación caracterizado por una de las siguientes fórmulas I, II y III:**Fórmula**
en las que:
R1, R2, R3 se seleccionan independientemente entre el grupo que consiste en hidrogeno, alquilo o arilo; y
R4 es un anión adecuado para formar una sal de los reactivos presentados anteriormente, seleccionado entre el grupo que consiste en tetrafluoroborato, triflato y halógeno, en donde el compuesto farmacéuticamente activo es un compuesto de Fórmula IV:**Fórmula**
en la que:
R se selecciona entre el grupo que consiste en hidroxilo, furoato y propionato.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2011/000834.
Solicitante: Hovione Inter Limited.
Nacionalidad solicitante: Suiza.
Dirección: Bahnohfstrasse 21 6000 Lucerne 7 SUIZA.
Inventor/es: LEITÃO,EMILIA PERPÉTUA TAVARES.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07J31/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07J ESTEROIDES (seco-steroides C07C). › Esteroides normales que contienen uno o más átomos de azufre que no pertenecen a un heterociclo.
PDF original: ES-2533061_T3.pdf
Fragmento de la descripción:
Método para monofluorometilación de sustratos orgánicos para preparar compuestos orgánicos biológicamente activos El enlace carbono-flúor se encuentra normalmente en productos farmacéuticos y agroquímicos, debido a que por lo general es metabólicamente estable y el átomo de flúor actúa como un bioisóstero del átomo de hidrógeno (Ann M. Thayer "Fabulous Fluorine" Chemical and Engineering News, 5 de junio de 2006, Volumen 84, pp. 15-24) . En la actualidad aproximadamente un 20 % de todos los compuestos farmacéuticos y un 30-40 % de los compuestos agroquímicos en el mercado contienen flúor. La fluoración y la fluoroalquilación son los dos métodos de síntesis principales para preparar de forma selectiva compuestos orgánicos fluorados. La monofluorometilación (introducción selectiva de un grupo CH2F en la molécula orgánica) se estudia menos que la fluoración.
La exploración de compuestos di-y monofluorometilados como compuestos orgánicos biológicamente activos ha surgido recientemente. Como resultado, se han desarrollado una de diversidad de fármacos estructuralmente diversos que contienen CH2F, tales como: Afloqualona, Propionato de Fluticasona (Jinbo Hu; Wei Zhang; Fei wang; Chem. Commum., 2009, 7465-7478) , el anestésico Sevoflurano, Furoato de Fluticasona.
La incorporación eficaz y selectiva de restos monofluorometilados en la molécula orgánica es beneficioso para la síntesis de la molécula diana. El proceso por lo general se realiza directamente usando CH2FBr (Véase el documento de patente WO-A-02/12266) o indirectamente, usando CH2BrI o ClCH2I entre otros. Estos compuestos se conocen como hidroclorofluorocarbonos o freones (HCFC) , que es una subclase de los clorofluorocarbonos (CFC) .
Se ha examinado cada permutación de flúor, cloro, e hidrógeno en el núcleo de metano y etano y la mayor parte se ha comercializado. Además, se conocen muchos ejemplos que contienen bromo por tener índices de carbono más elevados así como compuestos relacionados. El uso de esta clase de compuestos incluye refrigerantes, agentes de soplado, propelentes en aplicaciones médicas, y disolventes desengrasantes (M. Rossberg et al. "Chlorinated Hydrocarbons" en Ullmannâ?s Encyclopedia of Industrial Chemistr y 2006, Wiley-VCH, Weinheim) .
Desafortunadamente, debido a su estabilidad elevada, los CFC no se descomponen en la atmósfera inferior del mismo modo que lo hacen muchos agentes químicos industriales. De hecho se acumulan y con el tiempo suben a la estratosfera. La radiación ultravioleta en la estratosfera destruye CFC, y los átomos de cloro liberados destruyen la capa de ozono. Por esta razón, la fabricación de tales compuestos se está eliminando gradualmente de acuerdo con el Protocolo de Montreal (Pool, R. 1989. The elusive replacements for CFCs. Science 242: 666) . De acuerdo con el Protocolo de Montreal, se acordó el comienzo de la reducción de su consumo y producción en 2015.
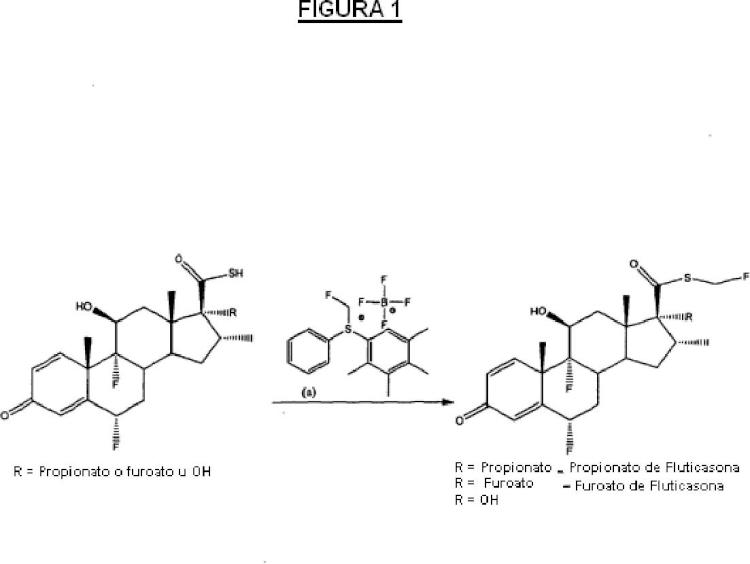
Recientemente, Prakash et al. informaron sobre un nuevo reactivo de monofluorometilación electrófilo para transferencia directa de +CH2F (tetrafluoroborato de S-monofluorometil-S-fenil-2, 3, 4, 5-tetrametilfenilsulfonio) a determinados nucleófilos tales como ácidos sulfónicos, aminas terciarias, derivados de imidazol, y fosfina (G. K. Sur y a Prakash; Istvan Ledneczki; Sujith Chacko; George A. (Olah; Org. Lett., vol. 10, Nº 4, 2008 páginas 557-560) . En la actualidad los inventores han ideado una forma de introducir el grupo -CH2F en un átomo de azufre, en particular un grupo tiol (S-H) para preparar derivados de fluticasona de fórmula IV tal como se define en las reivindicaciones, y de esta forma son capaces de evitar el uso de reactivos que agotan la capa de ozono. Por lo tanto, por ejemplo, se pueden usar tetrafluoroborato o triflato de S-monofluorometil-S-fenil-2, 3, 4, 5tetrametilfenilsulfonio (a) para preparar Propionato de Fluticasona y Furoato de Fluticasona tal como se muestra en la Fig. 1.
** (Ver fórmula) **
Este método también se puede usar para la preparación de compuestos intermedios monofluorometilados, tales como aminas cuaternarias, sales de tetrafluoroborato, sales de tetrafluoroborato y sales sulfónicas de imidazoles monofluorometilados y a su vez cada uno de estos compuestos también se puede usar para preparar Propionato de Fluticasona y Furoato de Fluticasona.
De acuerdo con la presente invención, se proporciona un método para preparar un compuesto orgánico biológicamente activo de fórmula IV que contiene un resto "CH2F", cuyo método comprende el uso de un reactivo de monofluorometilación caracterizado por una de las siguientes fórmulas I, II y III:
** (Ver fórmula) **
en las que:
R1, R2, R3 se seleccionan independientemente entre el grupo que consiste en hidrogeno, alquilo o arilo; y R4 es un anión adecuado para formar una sal de los reactivos presentados anteriormente, seleccionado entre el grupo que consiste en tetrafluoroborato, triflato y halógeno.
El método de la invención se usa para proporcionar un compuesto de Fórmula IV, tal como furoato de fluticasona o propionato de fluticasona.
De forma adecuada, el compuesto orgánico biológicamente activo de fórmula IV se puede obtener por monofluorometilación de un sustrato orgánico adecuado, que por lo general es un compuesto precursor. El sustrato orgánico puede ser un compuesto intermedio o compuesto precursor directo para el compuesto orgánico biológicamente activo, o puede ser un compuesto intermedio anterior en cualquier etapa apropiada en el proceso de síntesis. La etapa de monofluorometilación en el proceso de síntesis por lo general se determinará mediante el compuesto en cuestión, tal como será evidente para los expertos en la materia.
Preferentemente, el sustrato orgánico o compuesto precursor de fluticasona comprende un grupo tiol (S-H) .
Además, si se desea, el sustrato orgánico o compuesto precursor puede comprender uno o más grupos hidroxilo (-OH) . Los inventores han encontrado que, de forma sorprendente, los compuestos que tienen uno o más grupos hidroxilo se pueden monofluorometilar de forma satisfactoria (especialmente en un grupo tiol (S-H) ) sin necesidad de proteger el grupo hidroxilo (por ejemplo, en la posición C11 en un compuesto esteroideo) .
Por lo tanto, de acuerdo con la invención, se proporciona un método para preparar un compuesto orgánico biológicamente activo que contiene un resto "CH2F" de fórmula IV, cuyo método comprende la etapa de monofluorometilar un sustrato orgánico o compuesto precursor para el compuesto activo mencionado, cuyo sustrato o precursor comprende un grupo tiol (S-H) , usando un reactivo de monofluorometilación caracterizado por una de las siguientes fórmulas I, II y III: 40
** (Ver fórmula) **
en las que:
R1, R2, R3 se seleccionan independientemente entre el grupo que consiste en hidrogeno, alquilo o arilo; y R4 es un anión adecuado para formar una sal de los reactivos presentados anteriormente, seleccionado entre el grupo que consiste en tetrafluoroborato, triflato y halógeno.
Los compuestos orgánicos biológicamente activos de fórmula IV se pueden obtener por monofluorometilación de sustratos orgánicos con los siguientes reactivos de monofluorometilación:
** (Ver fórmula) **
En el compuesto de fórmula II, "alquilo" es preferentemente un alquilo primario con uno a cinco átomos de carbono (C1-C5) , siendo metilo particularmente preferente. Sin embargo, se puede usar alquilo ramificado si se desea, y puede estar opcionalmente sustituido. "Arilo" es preferentemente fenilo o fenilo sustituido.
En términos de las cantidades usadas de sustrato y reactivo de monofluorometilación, se usan preferentemente de 0, 9 a 2 equivalentes en moles de reactivo de monofluorometilación por mol de sustrato orgánico (o compuesto precursor) . Es particularmente adecuada una relación de aproximadamente 1:1 a 1:1, 2 (sustrato:reactivo) , particularmente cuando se preparan derivados de fluticasona o compuestos esteroideos similares.
La temperatura a la que se realiza la reacción entre el sustrato y el reactivo de monofluorometilación es de forma adecuada de -15 º C a 50 º C. Para muchas reacciones, es adecuada la temperatura ambiente (20-25 º C) .
Ejemplos
Los siguientes reactivos se proporcionan como ejemplos pero no limitan el alcance de la invención:
- tetrafluoroborato de S-monofluorometil-S-fenil-2, 3, 4, 5-tetrametilfenilsulfonio, triflato de S-monofluorometil-S-fenil2, 3, 4, 5-tetrametilfenilsulfonio, sales de los mismos -tetrafluoroborato de P-monofluorometiltrifenilfosfonio, triflato de P-monofluorometiltrifenilfosfonio y sales de los 25 mismos -tetrafluoroborato de N- (monofluorometil)... [Seguir leyendo]
Reivindicaciones:
1. Un método para preparar un compuesto farmacéuticamente activo que contiene un resto "CH2F" en un átomo de azufre, método que comprende el uso de un reactivo de monofluorometilación caracterizado por una de las siguientes fórmulas I, II y III:
** (Ver fórmula) **
en las que:
R1, R2, R3 se seleccionan independientemente entre el grupo que consiste en hidrogeno, alquilo o arilo; y R4 es un anión adecuado para formar una sal de los reactivos presentados anteriormente, seleccionado entre el grupo que consiste en tetrafluoroborato, triflato y halógeno, en donde el compuesto farmacéuticamente activo es un compuesto de Fórmula IV:
** (Ver fórmula) **
en la que: 20 R se selecciona entre el grupo que consiste en hidroxilo, furoato y propionato.
2. Un método de acuerdo con la reivindicación 1, en el que el reactivo de monofluorometilación es uno cualquiera de los siguientes compuestos:
(i) un compuesto con la Fórmula I:
** (Ver fórmula) **
en la que:
R4 se selecciona entre el grupo que consiste en tetrafluoroborato, triflato y halógeno, preferentemente R4 es triflato o tetrafluoroborato;
(ii) un compuesto con la Fórmula II:
** (Ver fórmula) **
en la que: R1, R2 y R3 se seleccionan independientemente entre el grupo que consiste en hidrogeno, alquilo o arilo; y R4 se selecciona entre el grupo que consiste en tetrafluoroborato, triflato y halógeno; 10 (iii) un compuesto con la Fórmula III:
** (Ver fórmula) **
en la que:
R4 se selecciona entre el grupo que consiste en tetrafluoroborato, triflato y halógeno, preferentemente R4 es triflato o tetrafluoroborato.
3. Un método de acuerdo con la reivindicación 2, en el que en el compuesto de fórmula II R1, R2 y R3 son grupos 20 etilo y R4 es tetrafluoroborato o triflato.
4. Un método de acuerdo con la reivindicación 2, en el que en el compuesto de fórmula II R1, R2 son ambos metilo, R3 es arilo y R4 es tetrafluoroborato o triflato.
6. Un método de acuerdo con la reivindicación 1, en el que R es propionato o furoato. 5. Un método de acuerdo con la reivindicación 2, en el que en el compuesto de fórmula II R1, R2 son ambos metilo, R3 es fenilo y R4 es tetrafluoroborato o triflato.
Patentes similares o relacionadas:
Forma polimórfica de propionato de fluticasona, del 15 de Julio de 2020, de Nicox Ophthalmics, Inc: Nanocristales de propionato de fluticasona que tienen un patrón de difracción de rayos X en polvo que incluye picos a aproximadamente 7,8, 15,7, 20,8, 23,7, 24,5 y 32,5 […]
Esteroides neuroactivos 19-nor para métodos de tratamiento, del 25 de Marzo de 2020, de Sage Therapeutics, Inc: Un compuesto de Fórmula (Ila): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo; en donde: ----- representa un enlace simple o doble según lo […]
Composiciones y métodos para el tratamiento de trastornos del SNC, del 26 de Febrero de 2020, de Sage Therapeutics, Inc: Compuesto de fórmula (II): **(Ver fórmula)** o una sal farmacéuticamente aceptable de los mismos. en la que: el anillo A es arilo […]
Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1, del 4 de Diciembre de 2019, de Bar Pharmaceuticals S.r.l: Un compuesto seleccionado del grupo que consiste en:**Fórmula**
Formas de sales polimórficas y amorfas de dilactato de escualamina, del 15 de Octubre de 2019, de Enterin, Inc: Forma amorfa de la sal de dilactato de 38-(N-[3-aminopropil]-1,4-butanodiamina)-7a,24R-dihidroxi-5a-colestano-24- sulfato, donde un patrón de difracción del […]
Compuestos anfifílicos con propiedades neuroprotectoras, del 2 de Octubre de 2019, de Ustav Organicke Chemie a Biochemie AV CR, v.v.i: Compuesto anfifílico, seleccionado de: 3-sulfato de piridinio(3R,5R,8S,9S,10 S,13S,14S)-10,13-dimetilhexadecahidro-1H-ciclopenta[a]fenantren-3- […]
 Inhibidores de SHIP y uso de los mismos, del 31 de Julio de 2019, de THE RESEARCH FOUNDATION OF THE STATE UNIVERSITY OF NEW YORK: Una composición farmacéutica que comprende:
un compuesto inhibidor de SHIP de fórmula (I), o una sal farmacéuticamente aceptable del […]
Inhibidores de SHIP y uso de los mismos, del 31 de Julio de 2019, de THE RESEARCH FOUNDATION OF THE STATE UNIVERSITY OF NEW YORK: Una composición farmacéutica que comprende:
un compuesto inhibidor de SHIP de fórmula (I), o una sal farmacéuticamente aceptable del […]
Procedimiento para la preparación de acetato de abiraterona y sus productos intermedios, del 24 de Julio de 2019, de OLON S.p.A: Procedimiento para la preparación de abiraterona o acetato de abiraterona **Fórmula** que comprende las siguientes etapas: a) conversión de trifluoroacetato […]