Preparación de ácido biliar sintético.
Un método para preparar ácido desoxicólico (DCA) o una sal farmacéuticamente aceptable del mismo:
**Fórmula**
comprendiendo dicho método
(a) hacer reaccionar 9α-hidroxiandrost-4-en-3,17-diona 1 con H2 bajo unas condiciones de hidrogenación para formar el compuesto 2**Fórmula**
(b) hacer reaccionar el compuesto 2 con ácido para formar el compuesto 3**Fórmula**
(c) hacer reaccionar el compuesto 3 con un agente reductor para formar el compuesto 4 como una mezcla de 4 y 5**Fórmula**
(d) hacer reaccionar el compuesto 4 con un reactivo de olefinación de dos carbonos bajo unas condiciones de formación de olefina para formar el compuesto 6**Fórmula**
(e) convertir el compuesto 6 en un compuesto de la fórmula 7**Fórmula**
(f) hacer reaccionar el compuesto de la fórmula 7 con un propiolato de alquilo de la fórmula CH-CC(O)OR o un acrilato de alquilo de la fórmula CH2≥CHC(O)OR en la que R es alquilo, en presencia de un ácido de Lewis para formar un compuesto de la fórmula 8 en la que P es un grupo protector, R es alquilo y la línea de trazos ------ es un enlace simple o doble;**Fórmula**
(g) hacer reaccionar el compuesto de la fórmula 8 con H2 bajo unas condiciones de hidrogenación para formar un compuesto de la fórmula 9 en la que P es un grupo protector y R es alquilo;**Fórmula**
(h) hacer reaccionar el compuesto de la fórmula 9 con un agente oxidante para formar un compuesto de la fórmula 10 en la que P es un grupo protector tal como acetilo y R es alquilo;**Fórmula**
(i) hacer reaccionar el compuesto de la fórmula 10 con H2 bajo unas condiciones de hidrogenación para formar un compuesto de la fórmula 11 en la que P es un grupo protector y R es alquilo;**Fórmula**
(j) hacer reaccionar el compuesto de la fórmula 11 con un agente reductor para formar un compuesto de la fórmula 12 en la que P es un grupo protector y R es alquilo;**Fórmula**
(k) exponer el compuesto de la fórmula 12 a unas condiciones de desprotección para formar un éster del mismo y a unas condiciones de hidrólisis adecuadas para formar ácido desoxicólico o una sal farmacéuticamente aceptable del mismo.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11181831.
Solicitante: Kythera Biopharmaceuticals, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 30930 Russell Ranch Road, 3rd Floor Westlake Village, CA 91362 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MORIARTY, ROBERT, M., DAVID,NATHANIEL E, MAHMOOD,NADIR AHMEDUDDIN, PRASAD,ACHAMPETA RATHAN, SWARINGEN,ROY A. JR, REID,JOHN GREGORY, SAHOO,AKHILA KUMAR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/575 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › sustituidos en posición 17 beta por una cadena de al menos tres átomos de carbono, p. ej. colano, colestano, ergosterol, sitosterol.
- A61K8/63 A61K […] › A61K 8/00 Cosméticos o preparaciones similares para el aseo. › Esteroides; Sus derivativados.
- A61P3/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Anorexiantes; Medicamentos para el tratamiento de la obesidad.
- A61Q19/06 A61 […] › A61Q USO ESPECIFICO DE COSMETICOS O DE PREPARACIONES SIMILARES PARA EL ASEO. › A61Q 19/00 Preparaciones para el cuidado de la piel. › para eliminar la celulitis.
- C07J1/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07J ESTEROIDES (seco-steroides C07C). › Esteroides normales que contienen carbono, hidrógeno, halógeno u oxígeno no sustituidos en posición 17 beta por un átomo de carbono, p. ej. estrano, androstano.
- C07J13/00 C07J […] › Esteroides normales que contienen carbono, hidrógeno, halógeno u oxígeno, teniendo un enlace doble carbono-carbono a partir de o hacia la posición 17.
- C07J9/00 C07J […] › Esteroides normales que contienen carbono, hidrógeno, halógeno u oxígeno, sustituidos en posición 17beta por una cadena de más de dos átomos de carbono, p. ej. colano, colestano, coprostano.
PDF original: ES-2550504_T3.pdf
Fragmento de la descripción:
Preparación de ácido biliar sintético Campo de la invención
La presente invención se refiere a métodos para la síntesis de ácido desoxicólico y productos intermedios útiles del mismo. Cabe destacar que los ácidos biliares preparados mediante la presente invención no se aíslan a partir de organismos mamíferos y microbianos que producen de forma natural estos ácidos y, por lo tanto, se encuentran libres de cualesquiera toxinas y contaminantes asociados con tales organismos.
Antecedentes de la invención
La colanología, el estudio de los ácidos biliares, y en particular la química del ácido biliar ha resultado de interés durante casi todo un siglo. A pesar de que se sabe mucho, la química del ácido biliar comporta una amplia diversidad de entidades químicas, muchas con unas propiedades sorprendentes. Para una revisión, véase, por ejemplo, Mukhopadhyay, S. y U. Maitra., Current Science 87: 1666- 1683 (2004) ("Chemistry and biology of bile acids").
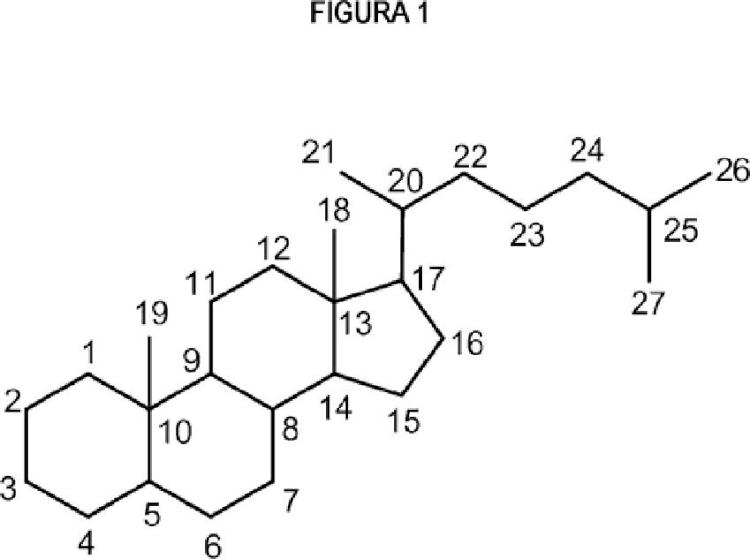
Los ácidos biliares se caracterizan por dos unidades de conexión, un núcleo de esteroide rígido y una cadena lateral alifática corta (véase la figura 1 de la presente solicitud). Véase, Hofmann, A. F., y col. Para una nomenclatura propuesta para los ácidos biliares, véase J. Lipid Res. 33: 599 - 604 (1992). Tanto el núcleo como la cadena lateral tienen un gran número de posibles disposiciones estéricas. El núcleo puede alterarse mediante la expansión o la contracción de anillos individuales, y la cadena lateral puede acortarse o alargarse. Además, ambas partes de la molécula de ácido biliar tienen un gran número de posibles sustituyentes polares. Pueden encontrarse presentes grupos ionizantes en el núcleo o la cadena lateral. Por último, pueden encontrarse presentes grupos de conjugación en el núcleo (por ejemplo, sulfato, glucuronato, fosfato) o en la cadena lateral (glicina o taurina u otros aminoácidos, o incluso azúcares). La estructura de la cadena lateral determina la clase del compuesto (ácidos biliares o sales biliares).
Los ácidos biliares son anfifílicos, teniendo tanto una "cara" anfifílica como una antipática:
Hofman, A. F., News Physiol. Sci. 14: 24 - 29 (1999) ("Bile Acids: The good, the Bad, and the Ugl/, en p. 25, figura 1).
Por convención, la superficie hidrófoba se denomina la "cara (3" y la superficie hidrófila se denomina la "cara a". La cara (3 es liposoluble y la cara a es relativamente polar, en general. Hay ácidos biliares, tales como los que tienen grupos polares (grupos hidroxilo, en ácidos biliares de origen natural) sobre la cara hidrófoba así como sobre la cara hidrófila, por ejemplo, ácido ursodesoxicólico. La naturaleza antipática de la molécula es responsable de la formación por parte de esta de micelas mixtas con lípidos antipáticos pero insolubles en agua, tales como la
**(Ver fórmula)**D
R
r
O
F
O
B
O
O
fosfatidilcolina. Los ácidos biliares no solubilizarán lípidos dietéticos en forma de micelas mixtas a menos que los ácidos biliares se encuentren por encima de una concentración crítica, que se denomina la concentración crítica de micelación.
Los ácidos biliares que se hallan en la mayor proporción en los seres humanos son el ácido quenodesoxicólico y el ácido desoxicólico. El ácido desoxicólico también se conoce como desoxicolato, ácido colanoico y 3a,12a-dihidrox¡- 5(3-colanato. En el cuerpo humano, el ácido desoxicólico se usa en la emulsificación de grasas para la absorción en el intestino. En la investigación, el ácido desoxicólico se usa como un detergente suave para el aislamiento de proteínas asociadas a membrana. Cuando es sustancialmente puro, el ácido desoxicólico es una forma de polvo cristalino de color blanco a blanco apagado. El ácido desoxicólico es uno de los cuatro ácidos principales producidos por el hígado. Este es soluble en alcohol y ácido acético. El número CAS para el ácido desoxicólico es [83-44-3],
La eliminación rápida de la grasa corporal es un antiguo ideal, y se ha afirmado que muchas sustancias logran tales resultados, a pesar de que pocas han mostrado resultados. La "mesoterapia", o el uso de inyectables para la eliminación de grasa, no está aceptada de forma generalizada entre los facultativos médicos debido a las preocupaciones de seguridad y de eficacia, a pesar de que se han realizado afirmaciones homeopáticas y cosméticas desde la década de 1950. La mesoterapia se concibió originalmente en Europa como un método de utilización de inyecciones cutáneas que contienen una mezcla de compuestos para el tratamiento de estados médicos y cosméticos locales. A pesar de que la mesoterapia se empleó tradicionalmente para el alivio del dolor, sus aplicaciones cosméticas, en particular la eliminación de grasas y la celulitis, han recibido recientemente atención en los Estados Unidos. Un tratamiento notificado de este tipo para una reducción de la grasa localizada, que se popularizó en Brasil y usa inyecciones de fosfatidilcolina, se ha considerado de forma errónea sinónimo de la mesoterapia. A pesar de su atractivo como una presunta inyección de "disolución de grasa", la seguridad y la eficacia de estos tratamientos cosméticos sigue siendo ambigua para la mayor parte de los pacientes y médicos. Véase, Rotunda, A. M. y M. Kolodney, Dermatologic Surgery 32: 465-480 (2006) ("Mesotherapy and Phosphatidylcholine Injections: Histórica! Clarifícation and RevieW).
El documento WO 2006/133160 describe métodos de lipoescultura, por ejemplo, la reducción de un depósito de grasa, mediante la administración de un antagonista del receptor del neuropéptido Y al sitio del depósito de grasa. Kolonin M. G. y col., Nat. Med. junio 10 (6): 625-32 (2004), describe péptidos pro-apoptóticos selectivos de grasa que tienen unos potentes efectos de destrucción de adipocitos. Los péptidos pro-apoptóticos que se describen requieren acceso a la vasculatura para destruir.
Literatura de publicación reciente informa de que el ácido desoxicólico presenta propiedades de eliminación de grasa cuando se inyecta en depósitos grasos in vivo. Véanse los documentos WO 2005/117900 y WO 2005/112942, así como US2005/0261258; US2005/0267080; US2006/127468; y US20060154906. El desoxicolato que se inyecta en tejido graso tiene dos efectos: 1) este destruye adipocitos por medio de un mecanismo citolítico; y 2) este da lugar a un estiramiento de la piel. Ambos de estos efectos son requeridos para mediar en las correcciones estéticas deseadas (es decir, el modelado del cuerpo). Debido a que el desoxicolato que se inyecta en grasa se inactiva rápidamente mediante la exposición a una proteína y a continuación vuelve rápidamente a los contenidos intestinales, sus efectos están espacialmente restringidos. Como resultado de este efecto de atenuación que confiere seguridad clínica, por lo general las terapias de eliminación de la grasa requieren 4-6 sesiones. Esta eliminación de la grasa localizada sin la necesidad de cirugía es beneficiosa no solo para el tratamiento terapéutico en relación con los depósitos de grasa localizada patológica (por ejemplo, dislipidemias que sobrevienen como resultado de la intervención médica en el tratamiento del VIH), sino también para una eliminación cosmética de la grasa sin el consiguiente riesgo inherente en cirugía (por ejemplo, liposucción). Véase, Rotunda y col., Dermatol. Surgery 30: 1001 - 1008 (2004) ("Detergent effects of sodium deoxycholate are a major feature of an injectable phosphatidylcholine formulation used for localized fat dissolution") y Rotunda y col., J. Am. Acad. Dermatol. 2005: 973 - 978 ("Lipomas treated with subcutaneous deoxycholate injections").
Las preparaciones de ácido biliar de calidad farmacéutica se encuentran comercialmente disponibles con un coste relativamente bajo. Este bajo coste se debe al hecho de que los ácidos biliares se obtienen a partir de carcasas de animales, en particular animales grandes tales como ganado vacuno y ovino. Cabe destacar que, al igual que con todos los medicamentos a partir de fuentes animales, existe la preocupación de que los productos de ácido biliar derivados de animales puedan contener patógenos animales y otros agentes nocivos tales como toxinas y metabolitos animales o microbianos, incluyendo toxinas bacterianas tales como pirógenos.
Tales patógenos animales pueden incluir priones, que se cree que son un tipo de proteína patogénica infecciosa que puede dar lugar a enfermedades priónicas. Las enfermedades priónicas son trastornos degenerativos del sistema nervioso. Una enfermedad de este tipo, la enfermedad de las "vacas locas" (que se cree que es una variante de la enfermedad de Creutzfeldt-Jakob (ECJ)), se... [Seguir leyendo]
Reivindicaciones:
1. Un método para preparar ácido desoxicólico (DCA) o una sal farmacéuticamente aceptable del mismo:
**(Ver fórmula)**co2h
comprendiendo dicho método
(a) hacer reaccionar 9a-hidroxiandrost-4-en-3,17-diona 1 con H2 bajo unas condiciones de hidrogenación para 10 formar el compuesto 2
**(Ver fórmula)**(b) hacer reaccionar el compuesto 2 con ácido para formar el compuesto 3
**(Ver fórmula)**(c) hacer reaccionar el compuesto 3 con un agente reductor para formar el compuesto 4 como una mezcla de 4 y 5
**(Ver fórmula)** **(Ver fórmula)**(d) hacer reaccionar el compuesto 4 con un reactivo de oleflnaclón de dos carbonos bajo unas condiciones de formación de olefina para formar el compuesto 6
**(Ver fórmula)**(e) convertir el compuesto 6 en un compuesto de la fórmula 7
**(Ver fórmula)**acrllato de alquilo de la fórmula CH2=CHC(0)0R en la que R es alquilo, formar un compuesto de la fórmula 8 en la que P es un grupo protector, R enlace simple o doble;
alquilo de la fórmula CHeCC(0)OR o un en presencia de un ácido de Lewis para es alquilo y la línea de trazos-----es un
**(Ver fórmula)**(g) hacer reaccionar el compuesto de la fórmula 8 con H2 bajo unas condiciones de hidrogenación para formar un compuesto de la fórmula 9 en la que P es un grupo protector y R es alquilo;
**(Ver fórmula)**(h) hacer reaccionar el compuesto de la fórmula 9 con un agente oxidante para formar un compuesto de la fórmula 10 en la que P es un grupo protector tal como acetilo y R es alquilo;
**(Ver fórmula)**(i) hacer reaccionar el compuesto de la fórmula 10 con H2 bajo unas condiciones de hidrogenación para formar un compuesto de la fórmula 11 en la que P es un grupo protector y R es alquilo;
po
**(Ver fórmula)**H
co2r
(j) hacer reaccionar el compuesto de la fórmula 11 con un agente reductor para formar un compuesto de la fórmula 12 en la que P es un grupo protector y R es alquilo;
(k) exponer el compuesto de la fórmula 12 a unas condiciones de desprotección para formar un éster del mismo y a unas condiciones de hidrólisis adecuadas para formar ácido desoxlcólico o una sal farmacéuticamente aceptable del mismo.
2. El método de la reivindicación 1, en el que las condiciones de hidrogenaclón de la parte (a) comprenden un catalizador de Pd / C.
3. El método de la reivindicación 1, en el que el ácido de la parte (b) es un ácido mineral, tal como H2SO4.
4. El método de la reivindicación 1, en el que el agente reductor de la parte (c) es LiAI(OtBu)3H.
5. El método de la reivindicación 1, en el que el reactivo de olefinación de dos carbonos de la parte (d) es un agente de Wittig tal como Ph3PCH2CH3+Br'.
6. El método de la reivindicación 1, en el que el grupo protector P del compuesto 7 -12 es -C(0)CH3.
7. El método de la reivindicación 1, en el que el ácido de Lewis de la parte (f) es EtAICI2.
8. El método de la reivindicación 1, en el que el propiolato de alquilo de la parte (f) es proprlolato de metilo.
9. El método de la reivindicación 1, en el que el acrilato de alquilo de la parte (f) es acrllato de metilo.
10. El método de la reivindicación 1, en el que las condiciones de hidrogenaclón de la parte (g) comprenden un catalizador de Pt02 o de Pd / C.
11. El método de la reivindicación 1, en el que el agente oxidante de la parte (h) es Cr03.
12. El método de la reivindicación 1, en el que las condiciones de hidrogenaclón de la parte (i) comprenden un catalizador de Pd / C.
13. El método de la reivindicación 1, en el que el agente reductor de la parte (j) es LiAI(OtBu)3H.
14. El método de la reivindicación 1, en el que las condiciones de desprotección y de hidrólisis de la parte (k) cuando P es -C(0)CH3 comprenden hacer reaccionar el compuesto 12 con LiOH.
**(Ver fórmula)**H
C02R
**(Ver fórmula)**15. Un compuesto de la fórmula 2
**(Ver fórmula)**5 16. Un compuesto de la fórmula 3
**(Ver fórmula)**17. Un compuesto de la fórmula 6
**(Ver fórmula)**18. Un compuesto de la fórmula 7
**(Ver fórmula)**en la que P es un grupo protector, tal como acetilo.
19. Un compuesto de la fórmula 8
**(Ver fórmula)**en la que P es un grupo protector, tal como acetilo.
Patentes similares o relacionadas:
Compuestos de alquilamido y usos de los mismos, del 6 de Mayo de 2020, de Nogra Pharma Limited: Compuesto de fórmula: **(Ver fórmula)** que presenta una configuración S, o una sal farmacéuticamente aceptable del mismo, para la utilización en el […]
Compuestos o-quinónicos como agentes neutralizantes del óxido nítrico, del 29 de Abril de 2020, de INSTITUT DES SUBSTANCES VEGETALES: Compuesto de fórmula (I) **(Ver fórmula)** en la que R1 se selecciona entre el grupo que constituido por: • -CH=CH-COOR2 […]
Uso de desoxicolato de sodio para la eliminación no quirúrgica de grasa, del 8 de Abril de 2020, de Lundquist Institute for Biomedical Innovation at Harbor-UCLA Medical Center: Uso de desoxicolato de sodio para la eliminación no terapéutica y no quirúrgica de acumulación de grasa localizada.
Composición cosmética en forma de gel, del 25 de Marzo de 2020, de Società Italo Britannica L. Manetti - H. Roberts & C.p.A: Composición cosmética en forma gel que tiene una viscosidad que oscila entre 50.000 y 200.000 mPa·s, medida a 20 °C y a presión atmosférica con un viscosímetro rotativo, […]
Composición de bebida para mejorar la piel, del 18 de Marzo de 2020, de Bottled Science Limited: Una composición de bebida que comprende colágeno y vitamina C, o un derivado de la misma y metil sulfonil metano, en la que dicho colágeno está presente en una […]
Composición cosmética bifásica y su uso por aplicación tópica, del 11 de Marzo de 2020, de PIERRE FABRE DERMO-COSMETIQUE: Composición cosmética y/o dermatológica, que comprende una fase acuosa y una fase oleosa distintas entre sí y superpuestas entre sí, caracterizada porque la fase acuosa contiene […]
Exopolisacárido para el tratamiento y/o cuidado de la piel, medios de cultivo y composiciones de estos, del 14 de Agosto de 2019, de Lipotec, S.A.U: Uso del exopolisacárido producido por una cepa de la especie Halomonas anticariensis para el tratamiento cosmético, no terapéutico y/o el cuidado cosmético no terapéutico […]
Procedimiento para el tratamiento cosmético de la piel, del 14 de Agosto de 2019, de Tecnología para la Medicina y la Estética, S.L: Procedimiento para el tratamiento cosmético de la piel que comprende la aplicación sobre la piel afectada de diatermia junto con la aplicación de un gel conductor y uno o más […]