METODO DE FABRICACION DE UN FORMA AMORFA DE SAL SEMICALCICA DEL ACIDO (3R,5R)7-3-FENIL-4-FENILCARBAMOIL-2-(4-FLUOROFENIL)-5-ISOPROPIL-PIRROLL-1-IL)-3,5-DIHIDROXIHEPTANOICO (ATORVASTATINA).
Método de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,
5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico de fórmula I
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CZ03/00007.
Solicitante: ZENTIVA, K.S.
Nacionalidad solicitante: República Checa.
Dirección: DOLNI MECHOLUPY 130,102 37 PRAHA 10.
Inventor/es: RADL,STANISLAV, STACH,JAN.
Fecha de Publicación: .
Fecha Concesión Europea: 8 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- C07D207/337 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Radicales sustituidos por átomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo.
Clasificación PCT:
- C07D207/34 C07D 207/00 […] › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente a los átomos de carbono del ciclo.
Fragmento de la descripción:
Método de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico (atorvastatina).
Sector técnico
La presente invención se refiere a un método nuevo de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico, conocido bajo el nombre no registrado de atorvastatina. Dicho fármaco es un representante importante de los medicamentos hipolipidémicos e hipocolestéricos.
Técnica anterior
La atorvastatina (fórmula I) se fabrica según las patentes publicadas (patentes de Estados Unidos Nos. 4.681.893; 5.003.080; 5.097.045; 5.103.024; 5.124.482; 5.149.837; 5.155.251; 5.216.174; 5.245.047; 5.248.793; 5.273.995; 5.397.792; 5.342.952) o según, por ejemplo, Tetrahedron Letters 1992, 33, 2283-2284, habitualmente a partir de la sal sódica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico y una sal cálcica soluble en agua adecuada, preferentemente de acetato o cloruro cálcico.
La sal sódica de partida del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico se puede obtener a partir de dicho ácido, que se obtiene normalmente a partir del (3R,5R) (6-{2-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-etil}-2,2-dimetil-[1,3]-dioxano-4-il)-acetato de tert-butilo (fórmula II).
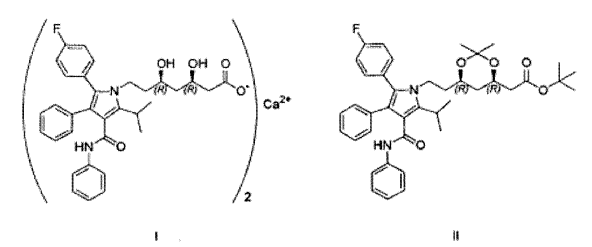
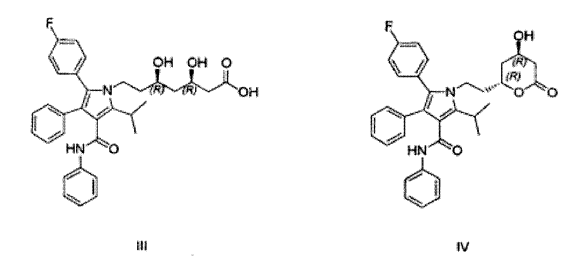
Este intermedio clave se convierte en la sal sódica del ácido respectivo mediante la mezcla en primer lugar con ácido clorhídrico y, posteriormente, con un gran exceso de hidróxido sódico, que está, sin embargo, acompañado con una gran cantidad de hidróxido en exceso y también de cloruro sódico. La acidificación seguida de extracción permite obtener a continuación una solución del ácido respectivo (fórmula III) sin impurezas inorgánicas. De este modo, el ácido obtenido se convierte a continuación en la lactona respectiva (fórmula IV), la cual se puede purificar mediante cristalización, y la lactona purificada se convierte a continuación en la sal sódica mediante la mezcla con un equivalente de hidróxido sódico; no se puede utilizar un exceso, ya que formaría, con la sal de calcio, hidróxido de calcio en la siguiente etapa que no se puede extraer totalmente del producto en las etapas posteriores del proceso según las patentes anteriores. Sin embargo, cuando se utiliza un equivalente del hidróxido la reacción consume tiempo y debe controlarse mediante HPLC. Otra desventaja de este proceso es una pérdida de, aproximadamente, el 20% del rendimiento.
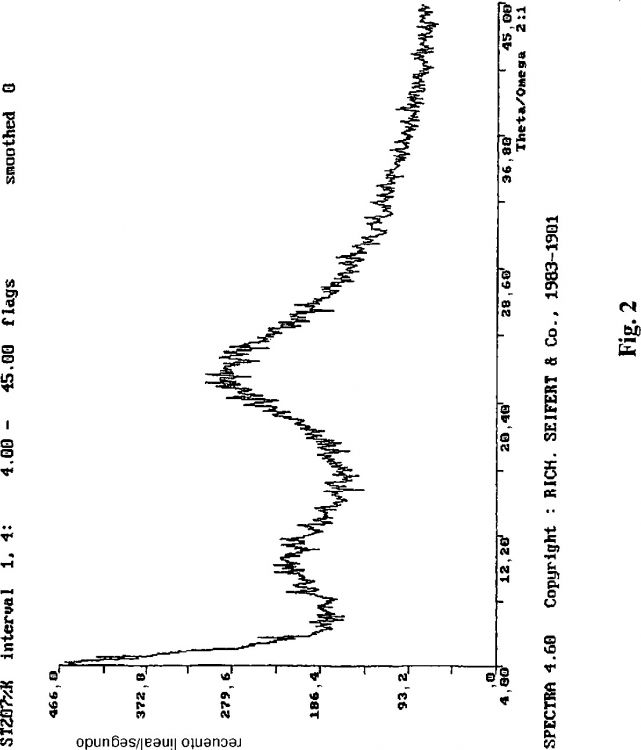
Dependiendo del modo de elaboración, la atorvastatina se obtiene en algunas de sus formas cristalinas o como atorvastatina amorfa. En las patentes originales (por ejemplo, las patentes de Estados Unidos Nos. 4.681.893 y 5.273.995), no se menciona la forma de la sustancia obtenida bajo estas patentes. Patentes posteriores (patentes de Estados Unidos Nos. 5.969.156 y 6.121.461), que dan a conocer formas cristalinas de atorvastatina, sugieren que la sustancia obtenida según las patentes originales era amorfa. La patente EP 839.132, que da a conocer un nuevo método de obtención de la forma amorfa de atorvastatina mediante la disolución de atorvastatina cristalina de la forma I en un disolvente no hidroxilado (la patente menciona tetrahidrofurano y una mezcla de tetrahidrofurano y tolueno como ejemplos de dichos disolventes), seguido de secado, repite de nuevo que las patentes originales dan lugar a atorvastatina amorfa, pero que dicho método es difícil de reproducir. Según nuestra experiencia, la atorvastatina obtenida según las patentes previas (US 4.681.893, 5.298.627 y 5.273.995) no es perfectamente amorfa y según un análisis por rayos X, muestra la presencia de componentes cristalinos (véase la figura 1). La patente original de Estados Unidos 4.681.893 también describe la posibilidad de purificación de la sustancia no adecuada mediante la disolución en acetato de etilo, la filtración a través de supercel y la precipitación de la solución con hexano a 50ºC. Una patente de Ranbaxy Laboratories (WO 00/71116 A1) da a conocer la conversión de la forma cristalina de la atorvastatina en un disolvente no hidroxilado y la precipitación de la solución resultante con un disolvente de hidrocarburo no polar. Se describe una estrategia similar en una patente de Lek (WO 01/42209 A1), la cual describe la conversión de la forma cristalina de atorvastatina en la forma amorfa mediante la disolución en un conjunto de disolventes que incluyen tanto disolventes no hidroxilados como alcoholes inferiores, seguido de la precipitación de estas soluciones con disolventes en los que la atorvastatina es insoluble. De nuevo, dichos disolventes están ampliamente definidos y, además de los disolventes de hidrocarburos no polares, se incluyen éteres alifáticos.
El objetivo de la presente invención es describir un método nuevo mejorado de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico que no mostraría las desventajas de los procesos mencionados anteriormente.
Características de la invención
Las ventajas de la atorvastatina amorfa para algunas aplicaciones se destacaron en la patente mencionada anteriormente EP 839.132. La materia de la presente invención es un método nuevo de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico, que comprende la conversión, en hidrólisis ácida, seguido de hidrólisis alcalina, del (3R,5R) (6-{2-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-etil}-2,2-dimetil-[1,3]-dioxano-4-il)-acetato de tert-butilo en una sal del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico con un metal alcalino, cuya sal se extrae a continuación en un disolvente orgánico seleccionado del grupo de ésteres de ácidos C1-C5 con alcoholes C1-C5 y, después de operaciones de purificación, se convierte mediante el tratamiento de una sal de calcio o de hidróxido de calcio, o de un alcoholato C1-C5 de calcio, en la sal semicálcica, seguido de la precipitación de la misma con un hidrocarburo C5-C12 o un dialquil éter de fórmula R1OR2, en la cual cada uno de R1 y R2 es un grupo alquilo C1-C5, formando así una fase amorfa sólida.
Todo el proceso anterior se basa en el sorprendente descubrimiento de que en acetato de etilo y en algunos disolventes relacionados, son fácilmente solubles no sólo el ácido libre correspondiente a la atorvastatina, sino un conjunto de sus sales, por ejemplo, la sal sódica, la sal potásica, las sales de amonio derivadas del amoniaco, aminas primarias, secundarias y terciarias y también la propia sal semicálcica.
A continuación, se da a conocer una descripción más detallada de la presente invención.
Preferentemente, la forma amorfa de la atorvastatina se obtiene directamente mediante la precipitación de una solución de la sal semicálcica de atorvastatina en un disolvente adecuado, preferentemente en un éster de un ácido C1-C5 y un alcohol C1-C5, siendo la utilización de acetato de etilo particularmente ventajosa, con un disolvente no polar, preferentemente con pentano, hexano, heptano o ciclohexano, opcionalmente con un dialquil éter R1OR2, en el que cada uno de R1 y R2 es un grupo alquilo C1-C5, preferentemente con dietil éter, diisopropil éter o t-butil metil éter. A efectos de incrementar la pureza del producto, se ha demostrado que es útil diluir la solución de atorvastatina en acetato de etilo, antes de la precipitación, con un codisolvente adicional, por ejemplo tolueno, tert-butil metil éter o tetrahidrofurano, en una cantidad de un 5 a un 95%, preferentemente de un 30 a un 70%. La forma amorfa también...
Reivindicaciones:
1. Método de fabricación de una forma amorfa de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico de fórmula I
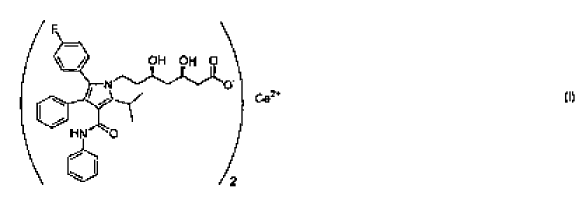
caracterizado porque el (3R,5R) (6-{2-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-etil}-2,2-dimetil-[1,3]-dioxano-4-il)-acetato de tert-butilo de fórmula II
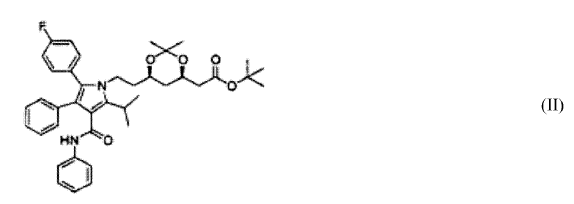
se convierte en primer lugar, en hidrólisis ácida, seguido de hidrólisis alcalina, en una sal del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico con un metal alcalino, el cual se extrae a continuación en un disolvente orgánico seleccionado del grupo de ésteres de ácidos C1-C5 con alcoholes C1-C5, en el que, después de operaciones de purificación, se convierte mediante el tratamiento con una sal de calcio o hidróxido de calcio o un alcoholato C1-C5 de calcio, en la sal semicálcica, y ésta última se precipita con un hidrocarburo C5-C12 o un dialquil éter de fórmula R1OR2, en el que cada uno de R1 y R2 es un grupo alquilo C1-C5.
2. Método, según la reivindicación 1, caracterizado porque la sal semicálcica se precipita a partir de una solución de acetato de etilo.
3. Método, según, como mínimo, una de las reivindicaciones 1 y 2, caracterizado porque la precipitación se lleva a cabo mediante la adición de un disolvente no polar del grupo que incluye pentano, hexano, heptano o ciclohexano, o un dialquil éter de fórmula R1OR2, en el que cada uno de R1 y R2 es un grupo alquilo C1-C5, a una solución de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico en el disolvente respectivo.
4. Método, según, como mínimo, una de las reivindicaciones 1 a 3, caracterizado porque se añade la solución de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico en el éster de un ácido C1-C5 con un alcohol C1-C5 a un disolvente no polar del grupo que incluye pentano, hexano, heptano o ciclohexano, o dialquil éter de fórmula R1OR2, en el que cada uno de R1 y R2 es un grupo alquilo C1-C5.
5. Método, según, como mínimo, una de las reivindicaciones 1 a 4, caracterizado porque la solución de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico en el éster respectivo se diluye, antes de la precipitación, con un 5 a 95% de un codisolvente adecuado.
6. Método, según, como mínimo, una de las reivindicaciones 1 a 5, caracterizado porque la solución de la sal semicálcica del ácido (3R,5R) 7-[3-fenil-4-fenilcarbamoil-2-(4-fluorofenil)-5-isopropil-pirrol-1-il]-3,5-dihidroxiheptanoico en el éster respectivo se diluye, antes de la precipitación, con un 30 a 70% de un codisolvente adecuado.
7. Método, según las reivindicaciones 5 ó 6, caracterizado porque se utiliza tolueno, t-butil metil éter o tetrahidrofurano como codisolvente.
Patentes similares o relacionadas:
Fenilacetilenos, del 20 de Mayo de 2020, de University Of Oregon: Un compuesto, o un protonato o una sal del mismo, que tiene la fórmula de: **(Ver fórmula)** en la que R1 es un grupo aromático sustituido con un aminoalcoxi, alquilamino, […]
Benzamidas sustituidas para el tratamiento de artrópodos, del 26 de Septiembre de 2018, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Compuestos de la fórmula (Ia")**Fórmula** donde D1 representa C-R11 o un heteroátomo seleccionado de N u O; D2 representa C-R11 o un heteroátomo seleccionado […]
Benzamidas sustituidas para el tratamiento de artrópodos, del 26 de Septiembre de 2018, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Compuestos de la fórmula (Ia")**Fórmula** donde D1 representa C-R11 o un heteroátomo seleccionado de N u O; D2 representa C-R11 o un heteroátomo seleccionado […]
Compuestos que inhiben la actividad de la catecol O-metiltransferasa, del 4 de Enero de 2017, de ORION CORPORATION: Un compuesto de fórmula I, **Fórmula** en donde R1 es alquilo C1-C6, alquenilo C2-C6, alquinilo C2-C6, cicloalquilo C3-C7, cicloalquenilo C4-C10, arilo, (R2)2C≥C-, […]
Pirrolocarboxamidas fluorometil-sustituidas como bloqueantes del canal de Ca CaV2.2, del 26 de Octubre de 2016, de GRUNENTHAL GMBH: Compuesto de fórmula general (I), **(Ver fórmula)** caracterizado porque n representa 0, 1 ó 2; R1 representa alquilo(C1-6), alquenilo(C2-6), […]
Derivados de 3,4-dihidropirrolo[1,2-a]pirazina-2,8(1H)-dicarboxamida, su preparación y uso terapéutico de los mismos, del 17 de Agosto de 2016, de SANOFI: Compuestos que corresponden a la fórmula general (I):**Fórmula** en la cual R2 representa: - un grupo alquilo C1-10, cicloalquil C3-7-alquilo C1-6, alquil […]
Nitroésteres de 1,5-diaril-2-alquilpirrol-3-sustituidos, inhibidores de COX-2 selectivos y donadores de óxido nítrico, del 20 de Enero de 2016, de Rottapharm Biotech S.r.l: Compuesto de fórmula (I), un solvato del mismo o sal farmacéuticamente aceptable:**Fórmula** en la que: - el sustituyente en posición […]
Inhibidores de COX-2 altamente selectivos y eficaces por vía oral de 1,5-diaril-2-alquil-pirroles 3-sustituidos, del 4 de Enero de 2016, de Rottapharm Biotech S.r.l: Compuesto de fórmula I:**Fórmula** en la que: - el sustituyente en la posición 1 del anillo de pirrol es un fenilo, sustituido en la posición […]