Péptidos quelantes del uranio y sus aplicaciones.
Péptido aislado, caracterizado porque es seleccionado dentro del grupo constituido por las secuencias SEQ ID NO: 4 a 7, 9, 10 y 12.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FR2004/001698.
Solicitante: COMMISSARIAT A L'ENERGIE ATOMIQUE ET AUX ENERGIES ALTERNATIVES.
Nacionalidad solicitante: Francia.
Dirección: BATIMENT "LE PONANT D" 25, RUE LEBLANC 75015 PARIS FRANCIA.
Inventor/es: VITA,CLAUDIO, LE CLAINCHE,LOÏC, MONJARDET,VÉRONIQUE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Reoviridae, p. ej. rotavirus, virus de la lengua azul de la oveja, virus de la fiebre de garrapatas del Colorado.
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C07K16/18 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C12N15/62 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
PDF original: ES-2543162_T3.pdf

Fragmento de la descripción:
Péptidos quelantes del uranio y sus aplicaciones
La presente invención se refiere a péptidos quelantes del uranio, as: como a sus aplicaciones para la descontaminación de suelo y aguas, y también para la detección y tratamiento de personas contaminadas por uranio.
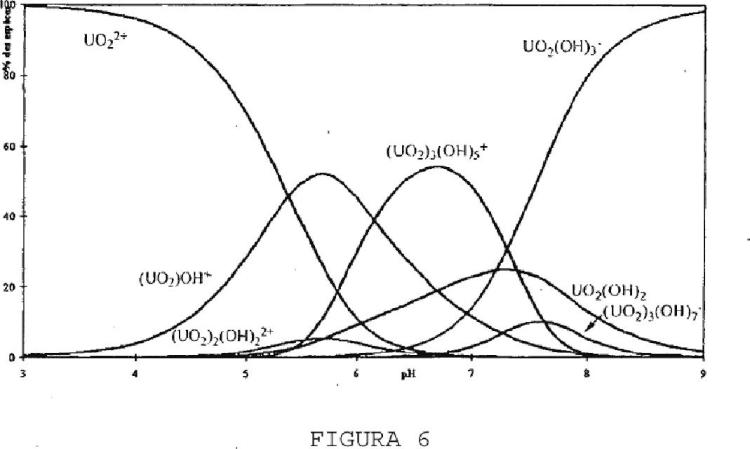
El uranio se encuentra normalmente presente en el medio ambiente en concentraciones muy reducidas, en forma de isótopos 238 (99,27%) y 235 (0,72%) que se descomponen por emisión de partículas alfa de baja toxicidad radiológica; la forma uranilo (UC^*) representa la forma más común del uranio en una atmósfera que contiene oxígeno.
No obstante, en ciertos sitios específicos, tales como cerca de las minas de minerales de uranio, de sitios de almacenamiento (control nuclear o almacenamiento de municiones con uranio empobrecido) o bien en ei caso de accidente nuclear, la concentración de este metal puede ser mucho más elevada y representa un peiigro para ei hombre, por el hecho de su acumulación en los riñones y en los huesos, toxicidad para los tejidos renales y desarrollo de cánceres de tejidos óseos.
La descontaminación de los lugares y de las personas contaminadas requiere disponer, por una parte, medios para neutralizar la toxicidad del uranio en el medio ambiente y en los organismos de los individuos contaminados y, por otra parte, reactivos de detección, eficaces y específicos para este metal. No obstante, no existen en la actualidad medios eficaces de detección y de descontaminación del uranio, en especial por la ausencia de ligandos específicos del uranio, capaces de detectar el uranio (sensor) y de quelar este metal tóxico que podría encontrarse presente en un entorno y/o en un medio biológico contaminado, con la finalidad de realizar su descontaminación.
El tratamiento actual de descontaminación de suelo se realiza principalmente por excavación, recogida y almacenamiento en lugares apropiados o por extracción del uranio con ayuda de agentes quelantes; estos tratamientos físico-químicos son caros, poco específicos o no específicos y poco adaptados al tratamiento de superficies contaminadas muy extensas y presentan además un riesgo de contaminación elevado para los operarios, por el hecho de una exposición repetida al uranio. De modo alternativo, se ha propuesto utilizar organismos vivos (microorganismos o vegetales superiores) para descontaminar los suelos y las aguas contaminadas por uranio. Este procedimiento se basa en la absorción de los metales y, por lo tanto, en su secuestro por estos organismos. Por ejemplo, ciertos vegetales son capaces de absorber los metales tóxicos por las raíces y acumularlos en las hojas, que son recogidas a continuación y almacenadas en lugares apropiados; los organismos actualmente disponibles no permiten una descontaminación eficaz de suelos y aguas contaminadas por su débil capacidad de extracción, de tolerancia y de acumulación de concentraciones elevadas de metales tóxicos.
La detección del uranio en las personas susceptibles de haber sido contaminadas por uranio se realiza ex situ por espectrometría de masas de plasma (ICP-MS); esta técnica es pesada de realizar y onerosa.
El tratamiento de las personas contaminadas por uranio se efectúa por administración de agentes quelantes que ligan el uranio, favoreciendo de esta manera su excreción y reduciendo, como consecuencia, su depósito en los riñones y los huesos. Entre los principales agentes quelantes del uranio se pueden citar: el acido dietilen triamina pentacético (DTPA), el ácido 5-aminosalicílico (5-AS), el ácido gálico, el sulfocatecol, el carboxicatecol y la hidroxipiridinona; presentando estos agentes quelantes el inconveniente de no ser específicos del uranio.
Se han desarrollado diferentes enfoques para detectar de manera específica algunos metales, en especial en medio acuoso o en muestras biológicas:
- sensores químicos fluorescentes (Tsien, 1993: Fluorescent chemosensors for ión and molecule recognition, páginas 130-146, Czarnik AW (ed), American Chemical Society, Washington DC); estos sensores fluorescentes son específicos del sodio, el potasio, el calcio y del magnesio; por el contrario, ningún sensor químico específico del uranio ha sido descrito.
- sensores peptídicos fluorescentes (biosensores) constituidos por un péptido de 26 aminoácidos, aproximadamente derivado de un dominio en dedo de zinc o "Zinc finger domain", marcado, como mínimo, por un grupo fluorescente (Walkup y otros, 1996, J. Am. Soc., 119, 3443-3450; Godwin y otros, 1998, J. Am. Soc., 118, 6514-6515; Walkup y otros, 1997, J. Am. Soc., 119, 3443-3540). En presencia de iones de zinc, estos biosensores peptídicos se estructuran alrededor del metal y exponen el grupo fluorescente a cambios de entorno que se traducen por una variación de emisión de fluorescencia que es función de la concentración del metal. De manera alternativa, cuando los péptidos están conjugados a dos grupos fluorescentes apropiados, el enlace del zinc al péptido comporta una modificación de conformación favorable a una transferencia eficaz de energía entre los dos fluoróforos (Fluorescencia Resonance Energy Transfer ou FREI), resultando en la emisión de una señal fluorescente proporcional a la concentración del metal (Walkup y otros, 1996, cita anterior). Por el hecho de la estructura del dominio en "dedo de zinc" que está adaptada a la quelación de iones con geometría tetraèdrica, como el zinc, estos
bíosensores no permiten ia queiación dei uranio, que en su forma de uraniio (UC^), ia más corriente en medio oxigenado, presenta una geometría bípíramídai de base pentágona! o hexagona! con un número de coordinación de 7-8 (uranio Vi).
- sensores proteicos fluorescentes, denominados ("camaieones"), constituidos por una proteína de fusión que comprende sucesivamente desde su extremo NH2 hacia su extremo COOH: un muíante azui o ciánico (EBFP o ECFP, donante de florescencia) de ia proteína fiuorescente GFP derivada de ¡a medusa Aequorea victoria, ¡a caimoduüna (CaM), que comprende ios dominios terminaos N y C y ¡os sitios ¡ y ii de fijación de! ión caicío, un péptído de 26 residuos que se eniaza a ia caimoduüna y que es derivado de! dominio que entaza ¡a caimoduüna de una quínasa de ia cadena ügera de ia míosína (MLCK), y otro muíante verde o amariüo de ¡a misma proteína fiuorescente (EGFP o EYFP, aceptador de florescencia), (Miyawaki y otros, Nature, 1997, 388, 882-887). El enlace dei caicío a ia caimoduüna provoca un cambio de conformación en ¡a proteína de fusión, que forma un nuevo sitio a! cuai se fija ei péptído y que produce una asociación entre ¡as dos proteínas fiuorescentes y un posicionamiento en el espacio favorabie a una transferencia eficaz de energía de! donante (EBFP o ECFP) hacia el aceptador de florescencia (EGFP o EYFP), produciendo de esta manera un aumento de ¡a florescencia emitida por el aceptador de florescencia (EGFP o EYFP). Otros indicadores fiuorescentes "camaieones" más sensibles y específicos para una gama de concentraciones de caicío más ampiia han sido igualmente obtenidos (Truong y otros, Nature Struct. Bíoi., 2001, 8, 1069-1073). Este sistema de indicador fiuorescente que se basa en ias variaciones de conformación inducidas por ei enlace dei caicío ai compiejo calmodulina-MLCKp es específico de! caicío y no permite, por ¡o tanto, detectar otros iones metáücos, tai como, por ejemplo, e¡ uraniio.
- ligando peptídicos seiectívos de metates pesados, derivados de motivos hélice-bucle-hélice (Borin y otros, Biopolymer, 1989, 28, 353-369; Dadiez y otros, FEBS Lett., 1991, 282, 143, 146; Marsden y otros, Biochem. CeN. Biol., 1990, 68, 587-601; Shaw y otros, Science, 1990, 249, 280-283; Reíd y otros, Arch. Biochem. Biophys., 1995, 323, 115-119; Procyshyn y otros, J. BioL Chem., 1994, 269, 1641-1647); estos péptidos presentan una débü estructuración de sus hélices en medios acuosos, así como reducidas afinidades para ios metates bivatentes (Kd det orden milimolar).
- bacterias que contienen un promotor que puede traducir ia presencia de un metai tóxico en una seña! tuminosa (Bechor y otros Biotechnol., 2002, 94, 125-132; Lee y otros, Bíosen. Bíoeiectron., 2003, 18, 571-577); en estos sistemas, el tóxico actúa como factor de estrés celular e induce por esta razón una expresión atterada de una proteína bioluminiscente, que representa la señal detectada; estos sistemas no son, por io tanto, específicos dei uranio y de los metales tóxicos en general.
Se han sintetizados péptidos correspondientes al sitio I de la caimoduüna. La mutación dei residuo de ácido glutámico del bucle de coordinación del calcio (E31D) suprime la afinidad pore! caldo pero conserva la afinidad para los lantánidos que muestran que la... [Seguir leyendo]
Reivindicaciones:
1. Péptido aislado, caracterizado porque es seleccionado dentro del grupo constituido por ¡as secuencias SEQ ¡D NO: 4 a 7, 9, 10 y 12.
2. Péptido, según la reivindicación 1, caracterizado porque está conjugado, como mínimo, a un ftuoróforo.
3. Péptido, según la reivindicación 2, caracterizado porque dicho fluoróforo es una proteína fluorescente seleccionada entre: EBFP, ECFP, EYFP, EGFP, DsRed, CopGFP y PhiYFP.
4. Péptido, según la reivindicación 2, caracterizado porque dicho fluoróforo es seleccionado entre dansito, cumarina, fluoresceína y los derivados Alexa.
5. Polipéptido, caracterizado porque comprende la concatenación de, como mínimo, dos péptidos idénticos o diferentes, según cualquiera de las reivindicaciones 1 a 4.
6. Proteína de fusión, caracterizada porque está constituida por la fusión de la secuencia de, como mínimo, un péptido, según la reivindicación 1, con la secuencia de una proteína apropiada.
7. Proteína de fusión, según la reivindicación 6, caracterizada dicha proteína apropiada y seleccionada dentro de! grupo constituido por calmodulina, proteínas camaleón procedentes de la anterior, y proteínas que poseen un motivo de tipo hélice-bucle-hélice, capaces de ligar el calcio.
8. Proteína de fusión, según la reivindicación 6 ó 7, caracterizada porque está conjugada, como mínimo, a un fluoróforo, tal como el definido en la reivindicación 3 ó 4.
9. Proteína de fusión, según la reivindicación 8, caracterizada porque uno de los extremos de dicha proteína está acoplado a un donante de fluorescencia, y el otro está acopiado a un aceptador de la fluorescencia.
10. Proteína de fusión, según la reivindicación 9, caracterizada porque comprende en uno de sus extremos la secuencia del EBFP o ECFP y en el otro extremo ia secuencia del EGFP o EYFP.
11. Molécula de ácido nucléico aislada, caracterizado porque comprende una secuencia codificante para un péptido, una polipéptido o una proteína de fusión, según cualquiera de ias reivindicaciones 1 a 10.
12. Vector recombinante eucariota o procariota, caracterizado porque comprende un inserto constituido por una molécula de ácido nucléico, según la reivindicación 11.
13. Célula eucariota o procariota, caracterizada porque está modificada por un vector recombinante, según la reivindicación 12.
14. Organismo anima! no humano transgénico, caracterizado porque comprende células modificadas por una molécula de ácido nudéico, según la reivindicación 11.
15. Planta transgénica, caracterizada porque comprende células modificadas por una molécula de ácido nucléico, según la reivindicación 11.
16. Utilización de, como mínimo, un péptido aislado, según cuaiquiera de las reivindicaciones 1 a 4, de un polipéptido, según ¡a reivindicación 5, o una proteína de fusión, según cualquiera de las reivindicaciones 6 a 10, para la preparación de un reactivo destinado a la detección de suelos y aguas contaminados por uranio.
17. Utilización de, como mínimo, un péptido aislado, según cuaiquiera de las reivindicaciones 1 a 4, de un polipéptido, según la reivindicación 5, o una proteína de fusión, según cualquiera de las reivindicaciones 6 a 10, para la preparación de un reactivo destinado al diagnóstico de individuos contaminados por uranio.
18. Utilización de, como mínimo, una célula, según la reivindicación 13, para la recuperación de suelos y aguas contaminados por uranio.
19. Utilización de una planta transgénica, según la reivindicación 15, para la recuperación de suelos y aguas contaminados por uranio.
20. Péptido, polipéptido o proteína de fusión, según una de ¡as reivindicaciones 1 a 10, para utiüzación como medicamento para el tratamiento de individuos contaminados por uranio.
21. Péptido para utilización como medicamento, según ¡a reivindicación 20, caracterizado porque está asociado, como mínimo, a una molécula que permite e¡ direccionado a¡ riñón y/o a huesos.
22. Péptido para la utilización como medicamento, según la reivindicación 20 ó 21, caracterizado porque está asociado a una molécula que favorece su excreción in vivo.
5 23. Kit para la detección de contaminación por uranio, caracterizado porque comprende, como mínimo, un péptido
aislado, un polipéptido o una proteína de fusión, según cualquiera de las reivindicaciones 1 a 10.
Patentes similares o relacionadas:
Cadena ligera de enteroquinasa modificada, del 22 de Julio de 2020, de NOVO NORDISK A/S: Un análogo de la cadena ligera de la enteroquinasa bovina que comprende una secuencia de aminoácidos establecida en la SEQ ID NO: 1, en donde dicho análogo comprende […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Métodos y composiciones para escisión dirigida y recombinación, del 20 de Mayo de 2020, de Sangamo Therapeutics, Inc: Un método in vitro para la escisión selectiva de un gen HLA clase I, un gen HLA que codifica una proteína de clase 1 del Complejo de Histocompatibilidad Mayor (MHC) […]
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Utilización diagnóstica de un polipéptido de fusión que comprende una proteína vírica y un enzima MGMT, del 15 de Abril de 2020, de INSTITUT PASTEUR: Utilización in vitro de un polipéptido de fusión que comprende una proteína vírica y i) el enzima 6-metilguanina-ADN-metiltransferasa (MGMT, EC 2.1.1.63) o un homólogo […]