Empleo de glicosaminoglicanos tales como p.ej. Heparina para el tratamiento de trastornos respiratorios tales como COPD.
Uso de un glicosaminoglicano o de una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento para facilitar el aclaramiento de moco de las vías aéreas centrales y periféricas de un sujeto humano con limitación crónica del flujo aéreo (CAL) que presenta hipersecreción de moco,
en el que el citado glicosaminoglicano o la sal tienen un peso molecular medio de 12 a 18 kilodáltones.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2003/000663.
Solicitante: OCKHAM BIOTECH LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: MANOR FARM SWANWICK LANE SWANWICK HAMPSHIRE SO31 7HA REINO UNIDO.
Inventor/es: SHUTE,JANIS KAY, DR.CONWAY,JOY H, HOCKEY,PETER MOREY, CARROLL,MARY PATRICIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/726 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Glicosaminoglicanos, es decir mucopolisacáridos (sulfato de condroitina, sulfato de dermatano A61K 31/737).
- A61K31/727 A61K 31/00 […] › Heparina; Heparano.
- A61K31/728 A61K 31/00 […] › Acido hialurónico.
- A61K31/737 A61K 31/00 […] › Polisacáridos sulfatados, p. ej. sulfato de condroitina, sulfato de dermatano (A61K 31/727 tiene prioridad).
- A61K38/46 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hidrolasas (3).
- A61K47/36 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/12 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aerosoles; Espumas.
- A61K9/72 A61K 9/00 […] › para fumar o inhalar.
- A61P11/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del aparato respiratorio.
PDF original: ES-2315479_T3.pdf
Fragmento de la descripción:
Empleo de glicosaminoglicanos tales como p.ej. heparina para el tratamiento de trastornos respiratorios tales como COPD.
Campo del invento
El presente invento se refiere a la fabricación de medicamentos para tratar la limitación crónica del flujo aéreo del pulmón.
Antecedentes del invento
La limitación crónica del flujo aéreo (CAL; del inglés, chronic airflow limitation) es una enfermedad mundial común. La mayoría de los individuos con CAL son fumadores o han sido fumadores, y se piensa que esto es una de las causas primarias del estado. Sin embargo, no todos los que padecen CAL son fumadores, y también se cree que la exposición a contaminantes y/o a ciertos productos químicos inhalados puede ser un factor que contribuya al desarrollo de la CAL.
En la actualidad, la CAL sólo se trata en sus fases más avanzadas usando una diversidad de broncodilatadores tales como agonistas β2 y agentes anticolinérgicos. Una proporción de quienes padecen CAL responde a esteroides tales como glucocorticosteroides. Los tratamientos existentes para la CAL son generalmente considerados sólo parcialmente eficaces, y no se cree que detengan la progresiva decadencia de la función pulmonar. Un factor desafortunado es que la CAL sólo se diagnostica en sus fases últimas, momento en que la decadencia de la función pulmonar está ya bien avanzada.
La única intervención reconocida para la CAL que en la actualidad ha demostrado modificar la enfermedad es la cesación de la acción de fumar. Dejar de fumar sólo puede enlentecer la progresiva decadencia de la función pulmonar hallada en la CAL. Se cree que puede continuar la inflamación incluso después de haber dejado de fumar y que la inflamación existente, y en particular las células inflamatorias presentes en el pulmón, pueden causar la liberación de mediadores inflamatorios que prolonguen o incluso amplifiquen la inflamación existente. Además, el dejar de fumar es a menudo difícil para quienes padecen CAL, algunos de los cuales no dejan de fumar en absoluto o vuelven a fumar más tarde. Por término medio, menos de la tercera parte de los pacientes es capaz de abandonar los cigarrillos incluso con ayuda.
El Documento US 6.077.683 trata de un método para la síntesis de heparina desulfatada y al uso de la misma para la inhibición de elastasa y catepsina.
Rao et al. (1990) , American Review of Respirator y Disease 142 (2) : 407-412, se refieren a polisacáridos sulfatados que evitan el enfisema y el daño pulmonar agudo inducidos por elastasa de leucocitos humanos en hámsteres.
Frommherz et al. (1991) , Advances in Experimental Medicine and Biology, 161-165, Springer Press, se refieren al efecto de glicosaminoglicanos sulfatados sobre la inhibición de la elastasa de neutrófilos por el inhibidor de alfa-1-proteinasa.
El Documento WO 99/06025 se refiere a métodos y composiciones para tratar enfermedades inflamatorias y reacciones alérgicas de fase tardía.
Sumario del invento
En consecuencia, el presente invento proporciona el uso de un glicosaminoglicano o una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento para facilitar el aclaramiento de moco de las vías aéreas centrales y periféricas de un sujeto humano con limitación crónica del flujo aéreo (CAL) que presenta hipersecreción de moco, en que el citado glicosaminoglicano o su sal tienen un peso molecular medio de 12 a 18 kilodáltones. Se prefiere especialmente el uso de heparina. También se prefiere particularmente el uso de la administración por inhalación y/o intranasalmente.
Breve descripción de las figuras
Figura 1
Efecto de agentes mucolíticos sobre el esputo de CAL (n = 3)
Como se describe en el Ejemplo 1, se homogeneizó esputo de CAL y se añadió un mucolítico en una cantidad de 10% en volumen/peso. Se llevó a cabo un mezclamiento usando una aguja de calibre 19. Se añadieron glóbulos fluorescentes modificados con carboxilato a la muestra de esputo en una relación 1:1 (volumen/peso) . Tras revolvimiento con formación de remolinos, se añadieron 20 μl de muestra a cada pocillo superior de una microcámara de Boy den. Los pocillos superiores e inferiores de la cámara estaban separados por un filtro de policarbonato de 8 μm, y los pocillos inferiores contenían 25 μl de disolución salina tamponada con fosfato (PBS; del inglés, phosphate buffered saline) . Se centrifugó la cámara durante 5 minutos a 1000 rpm para eliminar las burbujas de aire antes de una incubación a 37ºC, 900 rpm, durante 4 horas en la oscuridad. Después de la incubación, se desmontó la cámara y se midió la fluorescencia de la disolución de los pocillos inferiores. En el gráfico superior se muestran los resultados para PBS, heparina, DNasa y sulfato de dextrano (un testigo no glicosaminoglicano) . En el gráfico inferior se muestran los resultados para una mezcla de los sulfatos de condroitina A y C.
Figura 2
Formación de imágenes de DNA por microscopía de fuerzas atómicas (AFM; del inglés, atomic force microscopy)
Como se describe en el Ejemplo 2, se trató DNA de timo de ternera (0, 1 mg/ml) con heparina (0, 1 mg/ml) y se llevó a cabo una AFM al aire bajo condiciones ambientales usando un microscopio de sonda de barrido TopoMetrix TMX2000 (ThermoMicroscopes, Bicester, Reino Unido) . La Imagen A muestra DNA no tratado y la Imagen B muestra DNA tratado con heparina.
Figura 3
Formación de imágenes de DNA por microscopía de fuerzas atómicas (AFM)
Más micrografías de fuerzas atómicas de DNA (100 μg/ml) tratado con heparina en concentraciones menores. La Imagen A muestra los resultados para DNA no tratado; la Imagen B para DNA tratado con 0, 1 μg/ml de heparina; la Imagen C para DNA tratado con 1 μg/ml de heparina; y la Imagen D para DNA tratado con 10 μg/ml de heparina.
Descripción detallada del invento
El trastorno de la limitación crónica del flujo aéreo (CAL) es un estado progresivamente incapacitante que a menudo es fatal. Es una de las causas más frecuentes de mortalidad en adultos. El presente invento proporciona diversos medicamentos para el tratamiento de quienes padecen CAL. Estos medicamentos comprenden un glicosaminoglicano o una sal del mismo. El glicosaminoglicano o su sal tendrán un peso molecular medio de 12 a 18 kilodáltones.
Sujetos tratados
Los medicamentos del presente invento van a ser usados para tratar a sujetos que padecen CAL o presentan riesgo de desarrollar CAL. Típicamente, el sujeto será un ser humano pero, como se discute más adelante, puede ser un animal vertebrado. La CAL es un estado morboso caracterizado por una limitación del flujo aéreo que no es totalmente reversible. Normalmente, la limitación del flujo aéreo es tanto progresiva como asociada con una respuesta inflamatoria anormal de los pulmones a partículas o gases nocivos. En particular, aunque no exclusivamente, la CAL está asociada con la acción de fumar.
Para los fines del presente invento, la CAL puede ser definida como un estado en el que hay una decadencia progresiva de la función pulmonar, teniendo el sujeto afectado un FEV1 inferior al 80% del previsto para un individuo de esa edad/raza y/o altura, y/o que presenta una relación FEV1/FVC inferior a 70%. En una realización especialmente preferida, el sujeto que se va a tratar tendrá un FEV1 inferior al 75% del previsto.
Típicamente, la reducción del FEV1 sólo es parcialmente reversible. En particular, la reducción del FEV1 sólo es parcialmente reversible mediante el tratamiento con broncodilatadores tales como, por ejemplo, agonistas adrenérgicos β2 y, en particular, salbutamol.
El FEV1 se define como el volumen forzado máximo que puede ser expirado en un segundo a partir de la inspiración máxima (European Resp. Journal, 1993, 6: Suppl. 16; y Coates, "Lung Function: Assesment and Applications in Medicine", 4ª edición, Oxford, Blackwell, 1969) . Puede ser medido mediante técnicas estándares bien conocidas en este campo; es decir, por espirometría. El FEV1 de un individuo puede ser del 10 al 80% del previsto. Típicamente, el FEV1 del sujeto será del 10 al 75% del valor previsto. Preferiblemente, el sujeto puede tener un FEV1 del 60 al 75% del valor previsto, más preferiblemente del 40 al 60% del previsto, y aún más preferiblemente un valor inferior al 40% del previsto. El sujeto puede tener un FEV1 inferior al 70%, preferiblemente inferior al 60%, más... [Seguir leyendo]
Reivindicaciones:
1. Uso de un glicosaminoglicano o de una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento para facilitar el aclaramiento de moco de las vías aéreas centrales y periféricas de un sujeto humano con limitación crónica del flujo aéreo (CAL) que presenta hipersecreción de moco, en el que el citado glicosaminoglicano o la sal tienen un peso molecular medio de 12 a 18 kilodáltones.
2. Un uso de acuerdo con la Reivindicación 1, en el que el sujeto humano tiene un FEV1 del 10 al 75% del valor previsto.
3. Un uso de acuerdo con la Reivindicación 1 ó 2, en el que el sujeto padece una infección bacteriana o vírica.
4. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el moco contiene DNA genómico extracelular.
5. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el glicosaminoglicano o la sal fisiológicamente aceptable comprende unidades repetitivas de disacárido de fórmula general (1)
en la que:
cada A es igual o diferente y representa un grupo de fórmula (i) o (ii)
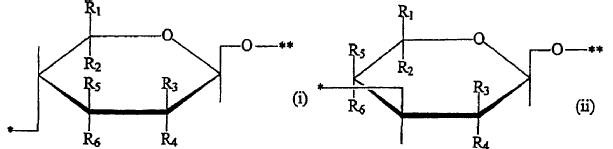
en las que:
- uno de R1 y R2 es hidrógeno y el otro es -CO2H, -SO3H o -CH2OR en que R es hidrógeno o -SO3H;
- uno de R3 y R4 es hidrógeno y el otro es -OR en que R es hidrógeno o -SO3H;
- uno de R5 y R6 es hidrógeno y el otro es -OH;
- * representa un enlace directo a un átomo de hidrógeno o un grupo B adyacente; y
- ** representa un enlace directo a un grupo B adyacente;
cada B es igual o diferente y representa un grupo de fórmula (iii) o (iv) :
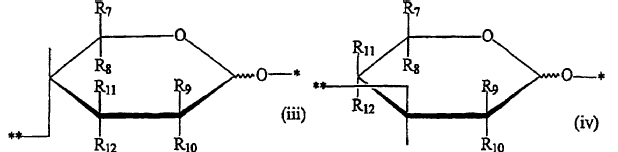
en las que:
- uno de R7 y R8 es hidrógeno y el otro es -CH2OH o -CH2OSO3H;
- uno de R9 y R10 es hidrógeno y el otro es -NHAc, -NH2 o -NHSO3H;
- uno de R11 y R12 es hidrógeno y el otro es -OH o -OSO3H;
-  indica un enlace con cualquier orientación estereoquímica;
indica un enlace con cualquier orientación estereoquímica;
- * representa un enlace directo a un átomo de hidrógeno o un grupo A adyacente; y
- ** representa un enlace directo a un grupo A adyacente;
o una sal fisiológicamente aceptable del mismo.
6. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el glicosaminoglicano es sulfato de condroitina A, sulfato de condroitina C, heparina, sulfato de heparina, heparano, sulfato de heparano, un derivado de cualquiera de los mismos o una mezcla de dos cualesquiera de los mismos.
7. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que se usa la sal sódica de heparina o sulfato de heparina.
8. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el glicosaminoglicano o la sal:
9. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el medicamento es:
10. Un uso de acuerdo con cualquiera de las reivindicaciones precedentes, en el que el sujeto es o ha sido un fumador.
11. Un glicosaminoglicano o una sal fisiológicamente aceptable del mismo para uso en la facilitación del aclaramiento de moco de las vías aéreas centrales y periféricas de un sujeto humano con limitación crónica del flujo aéreo (CAL) que presenta hipersecreción de moco, en que el citado glicosaminoglicano o la sal tienen un peso molecular medio de 12 a 18 kilodáltones.
Patentes similares o relacionadas:
Composiciones que comprenden una proteína de fusión de VIP-ELP para su uso en el tratamiento de fibrosis quística, del 29 de Julio de 2020, de Phasebio Pharmaceuticals, Inc: Una composición farmacéutica que comprende una proteína de fusión que comprende un péptido intestinal vasoactivo (VIP) y uno o más péptidos de tipo elastina (ELP), que […]
Compuestos que tienen actividad antagonista del receptor muscarínico y agonista del receptor beta2 adrenérgico, del 29 de Julio de 2020, de CHIESI FARMACEUTICI S.P.A.: Un compuesto de fórmula general I **(Ver fórmula)** en la que Q es un grupo de fórmula Q1 **(Ver fórmula)** Z es H u OH; […]
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Nuevos moduladores de receptores de fosfato de esfingosina, del 15 de Julio de 2020, de THE SCRIPPS RESEARCH INSTITUTE: Una composicion farmaceutica que comprende un compuesto de formula 265: **(Ver fórmula)** o una sal, estereoisomero, hidrato o solvato farmaceuticamente aceptable […]
Derivados de 5-[2-(piridin-2-ilamino)-1,3-tiazol-5-il]-2,3-dihidro-1H-isoindol-1-ona y su uso como inhibidores dobles de fosfatidilinositol··3-cinasa delta y gamma, del 15 de Julio de 2020, de ASTRAZENECA AB: Compuesto de formula (I) **(Ver fórmula)** donde X es C(O) o SO2; Y es SO2NHR5 o SO2R6; R1 se selecciona de alquilo C1-4, […]
Inhibidor de fibrosis, del 1 de Julio de 2020, de NIPPON SHINYAKU CO., LTD.: Composición farmacéutica que comprende un derivado heterocíclico seleccionado de ácido 2-{4-[N-(5,6-difenilpirazin-2-il)-N-isopropilamino]butiloxi}acético […]
Dispositivo para el tratamiento de, tratamiento de complicaciones ocasionadas por, y/o prevención de trastornos respiratorios causados por infecciones bacterianas, víricas, protozoarias, fúngicas y/o microbianas, preferiblemente para el tratamiento de complicaciones ocasionadas por fibrosis quística, del 1 de Julio de 2020, de Linde GmbH: Óxido nítrico gaseoso para usar como un medicamento inhalable en el tratamiento y/o prevención de trastornos respiratorios secundarios de la región respiratoria […]
Vacuna subunitaria contra Mycoplasma spp., del 1 de Julio de 2020, de Agricultural Technology Research Institute: Una composición para prevenir una infección por Mycoplasma spp., que comprende: un principio activo, que comprende una proteína de PdhA; y un adyuvante […]