Composición de medio de cultivo para cultivar células madre mesenquimales derivadas del amnios y método para cultivar células madre mesenquimales derivadas del amnios utilizando la misma.
Una composición de medio para el cultivo de células madre mesenquimales,
comprendiendo el medio:
(i) DMEM-P que contiene DMEM-HG, 0,2 mM de ácido L-ascórbico 2-fosfato, suero fetal bovino al 10%, 10 ng/ml de factor de crecimiento de fibroblastos básico (b-FGF), 10 μl/ml de aminoácido no esencial (NEAA); y
(ii) KSFM-P que contiene Queratinocitos-SFM definidos, 0,2 mM de ácido L-ascórbico 2-fosfato, 5 μg/ml de insulina, 2 mM de N-acetil-L-cisteína, 0,09 mM de cloruro de calcio, 74 ng/ml de hidrocortisona, suero fetal de bovino al 5%,
en donde el aminoácido no esencial (NEAA) consiste en 750 mg/L de glicina, 890 mg/L de L-alanina, 1.320 mg/L de L-asparagina, 1.330 mg/L de ácido L-aspártico, 1.470 mg/L de ácido L-glutámico, 1.150 mg/L de L-prolina y 1.050 mg/L de L-serina, y la relación en volumen de DMEM-P : KSFM-P es 2:1, 1:1 o 1:3.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/KR2011/005258.
Solicitante: RNL Bio Co., Ltd.
Nacionalidad solicitante: República de Corea.
Dirección: 1596-7 Bongcheon-dong Gwanak-gu Seoul 151-050 REPUBLICA DE COREA.
Inventor/es: RA,JEONG CHAN, KANG,SUNG KEUN, SEO,JU YEON, KIM,HYOEUN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
- C12N5/0775 C12N 5/00 […] › Células madre mesenquimales; Células madre derivadas de tejido adiposo.
PDF original: ES-2527253_T3.pdf
Fragmento de la descripción:
Composición de medio de cultivo para cultivar células madre mesenquimales derivadas del amnios y método para cultivar células madre mesenquimales derivadas del amnios utilizando la misma.
CAMPO TÉCNICO
La presente invención se refiere a un medio para cultivar células madre mesenquimales, y más particularmente a una composición de medio para cultivar células madre mesenquimales, que contiene medio basal, ácido L-ascórbico 2-fosfato, suero fetal bovino, factor de crecimiento de fibroblastos básico (b- FGF), aminoácidos no esenciales (NEAAs - siglas en inglés), insulina, N-acetil-L-cisteína, cloruro de calcio e hidrocortisona según se define en las reivindicaciones, y a un método de cultivar células madre mesenquimales utilizando la misma.
TÉCNICA DE ANTECEDENTES
Células madre se refieren a células que tienen no sólo la capacidad de auto-replicación, sino también la capacidad de diferenciarse en al menos dos tipos de células, y pueden dividirse en células madre totipotentes, células madre pluripotentes y células madre multipotentes.
Células madre adultas se obtienen tomando células de diversos órganos humanos y desarrollando las células en células madre y se caracterizan por que se diferencian en tejidos específicos solamente. Sin embargo, recientemente, experimentos para la diferenciación de células madre adultas en diversos tejidos, incluyendo células del hígado, fueron drásticamente un éxito, lo cual entra en un foco de atención.
Células madre multipotentes fueron aisladas primero de la médula ósea de adultos (Y. Jiang et al., Nature, 418:41, 22), y luego se encontraron también en otros varios tejidos adultos (C.M. Verfaillie, Trends Cell Biol., 12:52, 22). En otras palabras, la médula ósea es la fuente de células madre más ampliamente conocida, también se encontraron células madre multipotentes en la piel, vasos sanguíneos, músculos y cerebro (J.G. Toma et al., Nat. Cell Biol., 3:778, 21; M. Sampaolesi et al., Science, 31:487, 23; Y. Jiang et al., Exp. Hematol., 3:896, 22). Sin embargo, las células madre están muy rara vez presentes en el tejido adulto tal como la médula ósea, y este tipo de células son difíciles de cultivar sin inducir una diferenciación y, por lo tanto, son difíciles de cultivar en ausencia de medios específicamente rastreados. Es decir, es muy difícil mantener las células madre aisladas in vitro. Mientras tanto, los resultados de estudios sobre el aislamiento de células madre mesenquimales de tejido fetal revelaron que hay abundantes células madre mesenquimales en el tejido fetal. Sin embargo, el uso de tejido fetal como fuente de agentes terapéuticos celulares ha sido limitado debido a consideraciones éticas. Células madre mesenquimales también fueron aisladas de sangre de cordón umbilical (UCB - siglas en inglés) como fuente de células madre mesenquimales fetales (MSCs - siglas en inglés), pero sus números eran muy pequeños, y mostraron una proliferación deficiente.
En los últimos años, se sabe que células madre mesenquimales están presentes en el amnios (membrana amniótica o membrana de revestimiento amniótico), es decir, el delgado saco de la membrana más interna que rodea la placenta y a un embrión de mamífero en desarrollo. Por lo tanto, se han desarrollado tecnologías para aislar y cultivar este tipo de células madre mesenquimales (Publicación de patente internacional PCT N° WO 26/19357, Patentes de Corea N°s de Registro 79578 y 818214).
El documento WO 25/85422 describe un medio de cultivo para células madre humanas adultas que comprende calcio, NAC, hidrocortisona, insulina, EGF, suero fetal bovino al 1% y un antioxidante (reivindicaciones 74, 86). El antioxidante puede ser A2P (reivindicación 79). D1 describe, por lo tanto, una composición del medio que comprende todos los aditivos requeridos en la reivindicación 1, excepto bFGF y NEAAs. El medio se ha de utilizar para células madre adultas, incluidas células madre mesenquimales (p. ej., reivindicación 54). El mismo medio también se describe en Lin etal., Stem cells and Development 14, 92-12 (25).
El documento WO 29/6124 también muestra una composición de medio que comprende FBS, ácido ascórbico, hidrocortisona, NAC e insulina, para uso en el cultivo de células madre adultas procedentes del amnios (pág. 12, líneas 4-9). D2 describe otra composición de medio (pág. 12, líneas 1-4) que comprende DMEM, ácido ascórbico, EGF y NEAAs (pero no hidrocortisona ni NAC).
Sin embargo, los métodos convencionales para el cultivo de células madre derivadas de amnios tienen unas limitaciones, debido a que el tiempo necesario para que las células madre proliferen es largo.
Por consiguiente, los autores de la presente invención han hecho grandes esfuerzos para desarrollar un método capaz de aumentar la tasa de proliferación de células madre derivadas del amnios, manteniendo al mismo tiempo la capacidad de diferenciarse y, como resultado, han encontrado que, cuando células madre derivadas del amnios se cultivan en un medio que contiene DMEM-P y KSFM-P, la capacidad de las células de proliferar se puede aumentar al tiempo que se mantiene la capacidad de diferenciarse, completando así la presente invención.
DESCRIPCIÓN DE LA INVENCIÓN
PROBLEMA TÉCNICO
Es un objeto de la presente invención proporcionar un medio para cultivar células madre mesenquimales que muestre una alta tasa de proliferación celular al tiempo que mantenga la capacidad de las células de diferenciarse.
Otro objeto de la presente invención es proporcionar un método de cultivar células madre mesenquimales utilizando el medio anterior.
SOLUCIÓN TÉCNICA
Para conseguir los objetos anteriores, la presente invención proporciona una composición de medio para el cultivo de células madre mesenquimales, comprendiendo el medio:
(i) DMEM-P que contiene DMEM-HG, ,2 mM de ácido L-ascórbico 2-fosfato, suero fetal bovino al 1%, 1 ng/ml de factor de crecimiento de fibroblastos básico (b-FGF), 1 pl/ml de aminoácido no esencial (NEAA); y
(ii) KSFM-P que contiene Queratinocitos-SFM definidos, ,2 mM de ácido L-ascórbico 2-fosfato, 5 pg/ml de insulina, 2 mM de N-acetil-L-cisteína, ,9 mM de cloruro de calcio, 74 ng/ml de hidrocortisona, suero fetal de bovino al 5%,
en donde el aminoácido no esencial (NEAA) consiste en 75 mg/L de glicina, 89 mg/L de L-alanina, 1.32 mg/L de L-asparagina, 1.33 mg/L de ácido L-aspártico, 1.47 mg/L de ácido L-glutámico, 1.15 mg/L de L-prolina y 1.5 mg/L de L-serina, y la relación en volumen de DMEM-P : KSFM-P es 2:1, 1:1 o 1:3.
La presente invención también proporciona un método para cultivar células madre mesenquimales, comprendiendo el método cultivar las células madre mesenquimales en la composición del medio anterior.
Otras características y realizaciones de la presente invención resultarán más evidentes a partir de las siguientes descripciones detalladas y las reivindicaciones adjuntas
BREVE DESCRIPCIÓN DE LOS DIBUJOS
FIG. 1 muestra fotografías de células madre mesenquimales derivadas de amnios, cultivadas en DMEM-P, KSFM-P o un medio mixto de DMEM-P y KSFM-P durante 3 días.
FIG. 2 muestra fotografías de células madre mesenquimales derivadas de amnios, cultivadas en DMEM-P, KSFM-P o un medio mixto de DMEM-P y KSFM-P durante 4 días.
FIG. 3 muestra los resultados de análisis de citometría de flujo de cada uno de los grupos para CD31.
FIG. 4 muestra los resultados de análisis de citometría de flujo de cada uno de los grupos para CD34.
FIG. 5 muestra los resultados de análisis de citometría de flujo de cada uno de los grupos para CD45.
FIG. 6 muestra los resultados de análisis de citometría de flujo de cada uno de los grupos para CD29.
FIG. 7 muestra los resultados de análisis de citometría de flujo de cada uno de los grupos para CD44.
FIG. 8 muestra los resultados de citometría de flujo en cada uno de los grupos para CD73.
FIG. 9 es un conjunto de fotografías que muestran células madre mesenquimales de amnios, cultivadas en un medio mixto de DMEM-P y KSFM-P (Grupo 2) en el paso 1 (P1).
FIG. 1 es un conjunto de fotografías que muestran células madre mesenquimales de arrimos, cultivadas en un medio mixto de DMEM-P y KSFM-P (Grupo 2) en el paso 2 (P2).
FIG. 11 muestra los resultados de analizar la diferenciación osteogénlca de células madre mesenquimales de amnios, cultivadas en un medio mixto de DMEM-P y KSFM-P (Grupo 2), utilizando tinción de rojo de alizarina S en
diversas condiciones.
FIG. 12 es un gráfico que muestra una comparación entre la concentración cuantlficada de rojo de alizarina S en células madre mesenquimales... [Seguir leyendo]
Reivindicaciones:
1. Una composición de medio para el cultivo de células madre mesenquimales, comprendiendo el medio:
(i) DMEM-P que contiene DMEM-HG, ,2 mM de ácido L-ascórbico 2-fosfato, suero fetal bovino al 1%, 1 ng/ml de factor de crecimiento de fibroblastos básico (b-FGF), 1 pl/ml de aminoácido no esencial (NEAA); y
(ii) KSFM-P que contiene Queratlnocltos-SFM definidos, ,2 mM de ácido L-ascórbico 2-fosfato, 5 pg/ml de
insulina, 2 mM de N-acetil-L-cisteína, ,9 mM de cloruro de calcio, 74 ng/ml de hidrocortisona, suero fetal de bovino al 5%,
en donde el aminoácido no esencial (NEAA) consiste en 75 mg/L de glicina, 89 mg/L de L-alanina, 1.32 mg/L de L-asparagina, 1.33 mg/L de ácido L-aspártico, 1.47 mg/L de ácido L-glutámico, 1.15 mg/L de L-prolina y 1 1.5 mg/L de L-serina, y la relación en volumen de DMEM-P : KSFM-P es 2:1, 1:1 o 1:3.
2. La composición de medio de la reivindicación 1, en donde las células madre mesenquimales se derivan del amnios.
3. Un método para cultivar células madre mesenquimales, comprendiendo el método cultivar las células madre mesenquimales en la composición de medio de la reivindicación 1.
4. El método de la reivindicación 3, en el que las células madre mesenquimales se derivan del amnios.
Patentes similares o relacionadas:
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Estimulación de la vía wnt en la reprogramación de células somáticas, del 20 de Mayo de 2020, de WHITEHEAD INSTITUTE FOR BIOMEDICAL RESEARCH: Un método de reprogramación de una célula somática de mamífero, que comprende: (a) poner en contacto la célula somática de mamífero con un activador de la vía Wnt seleccionado […]
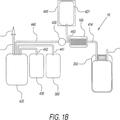 Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Ceramidasa y diferenciación celular, del 22 de Abril de 2020, de MOUNT SINAI SCHOOL OF MEDICINE: Un método in vitro para mejorar el fenotipo de una población de condrocitos, dicho método comprende: seleccionar una población de condrocitos de mamífero que […]
Medios de perfusión, del 1 de Abril de 2020, de Coherus Biosciences, Inc: Un método para la fabricación de una proteína que comprende la etapa de producir la proteína mediante el cultivo celular por perfusión de células […]
Andamios de biomatriz para la dispersión a escala industrial, del 11 de Marzo de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un metodo para producir un andamio de biomatriz a partir de tejido biologico seleccionado del grupo que comprende: pancreas, arbol biliar y duodeno para la […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en hepatocitos, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en hepatocitos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un medio […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en neuronas, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en neuronas, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un […]