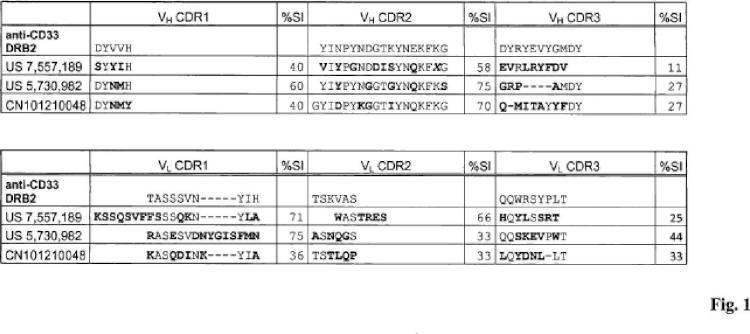
Anticuerpos anti-CD33 y su aplicación para el inmunotargeting en el tratamiento de enfermedades asociadas a CD33.
Anticuerpo anti-CD33 que contiene regiones determinantes de complementariedad (complementarity determining regions,
CDR), caracterizado porque las CDR comprenden las siguientes secuencias:
a) región variable de la cadena pesada (VH)
CDR1 DYVVH,
CDR2 YINPYNDGTKYNEKFKG,
CDR3 DYRYEVYGMDY, y
b) región variable de la cadena ligera (VL)
CDR1 TASSSVNYIH,
CDR2 TSKVAS,
CDR3 QQWRSYPLT.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/063990.
Solicitante: GEMoaB Monoclonals GmbH.
Nacionalidad solicitante: Alemania.
Dirección: Fiedlerstrasse 36 01307 Dresden ALEMANIA.
Inventor/es: BACHMANN,MICHAEL, STAMOVA,SLAVA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
PDF original: ES-2523502_T3.pdf


Fragmento de la descripción:
Anticuerpos anti-CD33 y su aplicación para el inmunotargeting en el tratamiento de enfermedades asociadas a CD33.
[0001] La invención se refiere a anticuerpos contra el antígeno asociado a tumores CD33 y a su aplicación para el immunotargeting de células positivas para CD33. Los anticuerpos según la invención son adecuados para la 5 aplicación en el campo de la medicina, la farmacia y la investigación biomédica.
[0002] El cáncer (neoplasia maligna) es una clase de enfermedad en la que un grupo de células se distingue por una división celular incontrolada, por una invasión y destrucción de tejidos contiguos y a veces por una metastatización. Estas características malignas del cáncer lo diferencian de los tumores benignos, que, si bien desplazan con su crecimiento el tejido adyacente, no se infiltran en éste y no metastatizan. La mayoría de los tipos 10 de cáncer forman tumores, pero algunos no, como las leucemias, que afectan al sistema hematopoyético. En el sentido de la invención, el término 'cáncer' designa tanto tumores malignos como hemoblastosis.
[0003] En las células cancerosas está inactivada la armonización de crecimiento, división y destrucción en el complejo celular. Surgen cuando se alteran determinados genes y estas alteraciones ya no pueden repararse, lo que lleva a la falta de funcionalidad de determinadas zonas de los genes, de manera que las células cancerosas se 15 estimulan a sí mismas a dividirse e ignoran las señales inhibidoras del crecimiento procedentes del entorno de la célula.
[0004] El sistema inmunitario intenta fundamentalmente combatir las células que crecen de manera incontrolada. Un problema para ello es el hecho de que las células cancerosas son en muchos aspectos iguales que las células normales del cuerpo, ya que proceden de las mismas. Por lo tanto, en la mayoría de los casos las medidas de 20 defensa del sistema inmunitario son insuficientes para controlar el crecimiento del tumor.
[0005] En la leucemia mieloide aguda (LMA) se ve afectada la mielopoyesis, o sea la parte del sistema hematopoyético responsable de la formación de granulocitos y monocitos. En la hematopoyesis, los mieloblastos representan una etapa previa inmadura de los leucocitos mieloides. En la LMA, diversas alteraciones genéticas que afectan a los genes relevantes para la división celular tienen como resultado un mieloblasto individual para la 25 formación de una célula que permanece en un estado inmaduro y se multiplica masivamente. Esta multiplicación de las etapas previas inmaduras en la médula ósea y también en la sangre caracteriza la LMA.
[0006] Las alteraciones pueden producirse en una serie de diferentes puntos del ciclo celular, de manera que la LMA presenta distintas características fenotípicas, genotípicas y clínicas. La clasificación moderna de la LMA se basa en la tesis de que las características y el comportamiento de las células tumorales dependen de en qué etapa 30 del ciclo celular se ha detenido la proliferación. En muchos pacientes de LMA pueden detectarse determinadas características citogenéticas específicas distintivas que, a menudo, son significativas en cuanto al pronóstico. Las alteraciones genéticas codifican proteínas de fusión anormales, en la mayoría de los casos factores de transcripción, que causan la proliferación incontrolada.
[0007] Las células tumorales se diferencias de las células sanas en la expresión de antígenos tumorales, o sea de 35 proteínas que expresan sólo las células tumorales. Éstas se forman como consecuencia del genoma alterado en las células cancerosas, o a causa de una expresión genética alterada. Los antígenos tumorales se hallan en la membrana celular exterior de las células tumorales, en el plasma celular y en el núcleo celular. Los antígenos tumorales son, como estructura diana, la base de la mayoría de los conceptos de la inmunoterapia del cáncer. Hasta la fecha se conocen más de 2.000 antígenos tumorales. 40
[0008] Como diana para la terapia del cáncer resultan ideales los antígenos específicos de tumores (TSA) , o sea antígenos que son producidos sólo por células cancerosas y no por células sanas. Sin embargo, la mayoría de los antígenos tumorales no son específicos de tumores, sino asociados a tumores (TAA) , es decir que son expresados también por células sanas. No obstante, en muchos tumores los antígenos tumorales están sobre-expresados. Debido a mutaciones en el genoma pueden aparecer también alteraciones estructurales en la secuencia de 45 proteínas. Muchos antígenos tumorales aparecen sólo en determinados tipos de tumor y, dentro de éstos, frecuentemente incluso sólo en determinados casos.
[0009] Los antígenos tumorales presentes en la LMA comprenden, entre otros, TAA asociados a una serie de otras enfermedades tumorales, como por ejemplo la telomerasa transcriptasa inversa, la proteína del tumor de Wilms 1 (WT1) y la survivina. Además se conocen también TAA asociados a otras enfermedades leucémicas, como el 50 CD168 y la fosfoproteína de fase M. También existen TAA que aparecen especialmente en conexión con la LMA, como el CD33, el CD45 y los mHAgs (minor histocompatibility antigens) .
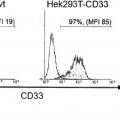
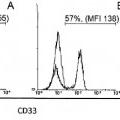
[0010] El CD33 es una proteína transmembrana glicosilada compuesta de 364 aminoácidos, que pertenece a la familia de las lectinas similares a Ig de unión a ácido siálico (SIGLECs) . Se expresa también en células precursoras hematopoyéticas en fase temprana, precursores mielomonocíticos y células mieloides, mientras que no está 55 presente en células madre de la médula ósea pluripotentes normales. Aproximadamente de un 85 a un 90% de los
pacientes de LMA dan positivo para CD33. Por lo tanto, el CD33 constituye una diana particularmente atractiva para una inmunoterapia y se utiliza ya como diana en una inmunoterapia dirigida.
[0011] La terapia convencional de la LMA es una quimioterapia para la inducción de una remisión, a la que pueden seguir otras quimioterapias o el trasplante de células madre hematopoyéticas. En los Estados Unidos se conjugó en el año 2000 un anticuerpo monoclonal con un citostático, gemtuzumab ozogamicina, para pacientes con LMA 5 recidivante que no son candidatos para la quimioterapia estándar.
[0012] Los anticuerpos son proteínas de la clase de las globulinas, que en los vertebrados se forman como reacción a determinadas sustancias, los antígenos. En la lucha contra las células cancerosas, los anticuerpos policlonales endógenos desempeñan sólo un papel muy pequeño. Esto es debido a que la mayoría de las células tumorales no presentan antígenos suficientemente alterados que sean reconocidos como extraños por el propio 10 sistema inmunitario, de manera que los anticuerpos endógenos no se enlazan a las células tumorales en cantidad suficiente. Los anticuerpos monoclonales son completamente idénticos en su estructura y están dirigidos sólo contra un epítopo de un antígeno.
[0013] Los anticuerpos monoclonales empleados para la terapia del cáncer actúan casi exclusivamente a través de la citotoxicidad celular dependiente de anticuerpos (antibody dependent cellular cytotoxicity, ADCC) . En este caso, 15 los anticuerpos reclutan mediante su parte Fc células efectoras citotóxicas, como por ejemplo células NK, macrófagos, linfocitos o granulocitos, que no presentan por sí mismas ninguna especificidad antigénica, con respecto a la célula tumoral. El daño producido directamente en la célula por anticuerpos monoclonales ligados, como el desencadenamiento de determinadas cascadas de señales intracelulares que inician la apoptosis por la reticulación cruzada de los antígenos tumorales debido a la unión del anticuerpo, es una rara excepción. 20
[0014] Para reforzar el efecto de los anticuerpos monoclonales en las enfermedades cancerosas se han desarrollado distintas estrategias de vectorización de medicamentos (drug targeting) , con el fin de utilizar los anticuerpos como portadores de principios activos más potentes, los así llamados inmunoconjugados o derivados de anticuerpos. Para ello se han ligado (conjugado) a los anticuerpos correspondientes principios activos como radionúclidos, toxinas (por ejemplo la toxina diftérica) , citoquinas o también citostáticos. 25
[0015] En principio es posible ligar a anticuerpos principios activos de gran potencia, que en caso de una administración sistémica libre causarían efectos colaterales injustificables debido a su toxicidad. Los derivados de anticuerpos constan de tres componentes: un anticuerpo o fragmento de anticuerpo, un principio activo y un elemento de unión (linker) entre el anticuerpo y el principio activo.
[0016] El documento WO 2004/043344 A2 da a conocer el anticuerpo anti-CD33 "My9-6"... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo anti-CD33 que contiene regiones determinantes de complementariedad (complementarity determining regions, CDR) , caracterizado porque las CDR comprenden las siguientes secuencias:
a) región variable de la cadena pesada (VH)
CDR1 DYVVH, 5
CDR2 YINPYNDGTKYNEKFKG,
CDR3 DYRYEVYGMDY, y
b) región variable de la cadena ligera (VL)
CDR1 TASSSVNYIH,
CDR2 TSKVAS, 10
CDR3 QQWRSYPLT.
2. Anticuerpo según la reivindicación 1, que contiene la siguiente estructura, en caso dado humanizada:
- una región variable de la cadena pesada con la secuencia según SEQ ID nº 13
- y una región variable de la cadena ligera con la secuencia según SEQ ID nº 14.
3. Anticuerpo según la reivindicación 1 o 2, que contiene adicionalmente, al menos, una de las siguientes 15 estructuras:
- una región constante de una cadena pesada de una IgG humana,
- una región CL de la cadena ligera kappa humana y/o
- una región bisagra IgG3 humana,
en caso dado en forma de un fragmento F (ab') 2. 20
4. Anticuerpo según una de las reivindicaciones 1 a 3 en forma de un fragmento scFv o en forma de un fragmento F (ab') 2.
5. Anticuerpo según una de las reivindicaciones 1 a 4, caracterizado porque está conjugado con un grupo efector u otro anticuerpo o fragmento de anticuerpo dirigido contra un antígeno distinto de CD33.
6. Anticuerpo según la reivindicación 5, estando el grupo efector seleccionado entre toxinas, enzimas, moléculas co-25 estimulantes, radionúclidos y ácidos nucleicos, en caso dado en forma de una proteína de fusión.
7. Anticuerpo según una de las reivindicaciones 1 a 6, caracterizado porque está conjugado con un ligando que se enlaza específicamente a células efectoras y con ello influye en su actividad.
8. Secuencia de ácidos nucleicos que codifica para un anticuerpo según la reivindicación 1 a 7.
9. Vector que contiene una secuencia de ácidos nucleicos según la reivindicación 8. 30
10. Célula huésped u organismo huésped no humano que contiene una secuencia de ácidos nucleicos según la reivindicación 8 o un vector según la reivindicación 9.
11. Composición farmacéutica que contiene un anticuerpo según una de las reivindicaciones 1 a 7 en asociación con un excipiente o diluyente farmacológicamente aceptable, en caso dado en una forma adecuada para la administración intravenosa. 35
12. Anticuerpo según una de las reivindicaciones 1 a 7 para la utilización como fármaco.
13. Procedimiento para la producción de un anticuerpo según una de las reivindicaciones 1 a 7, en el que:
a. se expone una célula huésped o un organismo huésped no humano según la reivindicación 10 a unas condiciones en las que tiene lugar una expresión y en caso dado una secreción del anticuerpo y, dado el caso,
b. se depura el anticuerpo al menos parcialmente. 40
Sucesos
Sucesos
Sucesos
Tiempo
Sin anticuerpo
Lisis específica [%]
Sin anticuerpo
Relación E:T
Lisis específica [%]
Sucesos
Sucesos
REFERENCIAS CITADAS EN LA DESCRIPCIÓN
La lista de referencias citada por el solicitante lo es solamente para utilidad del lector, no formando parte de los documentos de patente europeos. Aún cuando las referencias han sido cuidadosamente recopiladas, no pueden excluirse errores u omisiones y la OEP rechaza toda responsabilidad a este respecto.
Documentos de patente citado en la descripción
• WO 2004043344 A2 [0016]
• US 5730982 A [0017] [0019]
• EP 1656950 A1 [0017]
• US 7557189 B [0019]
• CN 101210048 [0019]
Bibliografía de patentes citada en la descripción
• E. J. FELDMAN. Phase III Randomized Multicenter Study of a Humanized Anti-CD33 Monoclonal Antibody, Lintuzumab, in Combination With Chemotherapy, Versus Chemotherapy Alone in Patients With Refractor y or First-Relapsed Acute Myeloid Leukemia.
J. Clin. Oncol., 2005, vol. 23 (18) , 4110-4116
• WALTER R et al. Blood, 2005, vol. 105 (3) ,
1295-1302 [0018]
• P. A. BAEUERLE. BiTE: Teaching antibodies to engage T cells for cancer therapy. Curr Opin Mol Ther, 2009, vol. 11.
2. 30 [0026]
• R. BARGOU. Tumor regression in cancer patients by ver y low doses of a T cell-engaging antibody. Science, 2008, vol. 321.
97. 977 [0027]
• K. BRISCHWEIN. MT110: a novel bispecific single-chain antibody construct with high efficacy in eradicating established tumors. Mol Immunol, 2006, vol. 43, 1129-1143 [0027]
Patentes similares o relacionadas:
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Proteínas de unión al antígeno ST2, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo aislado que se une a un antígeno ST2 que tiene la secuencia de aminoácidos 19-556 del SEQ ID NO: 1, comprendiendo dicho anticuerpo una secuencia de […]